Đề kiểm tra học kì I môn hóa lớp 10 (4 mã đề-có đáp án)
Xem thêm
Đề cương ôn tập học kì 2 môn hóa lớp 10
Đề cương ôn tập học kì 2 môn hóa lớp 11
3 đề kiểm tra học kì 2 môn hóa lớp 11
Đề thi học kì 2 môn hóa lớp 11 năm học 2019 – 2020
Đề kiểm tra học kì 2 môn hóa lớp 12
Đề kiểm tra học kì I môn hóa lớp 10 Mã đề 001
Cho biết nguyên tử khối của các nguyên tố: H=1; C=12; N = 14; O = 16; F=19; Na = 23; Mg = 24; Al = 27; S = 32; Cl = 35,5; K = 39; Ca = 40; Cr = 52, Mn = 55; Fe = 56; Cu = 64; Zn = 65; Br = 80; Sr = 88; Ag=108; Ba = 137.
Câu 1: Trong phòng thí nghiệm, clo thường được điều chế bằng cách oxi hóa hợp chất nào sau đây?
A. KCl. B. KMnO4. C. NaCl. D. HCl.
Câu 2: Khí HCl có thể được điều chế bằng cách cho tinh thể muối ăn tác dụng với chất nào sau đây?
A. H2SO4 loãng. B. HNO3. C. H2SO4 đậm đặc. D. NaOH.
Câu 3: Khí Cl2 không tác dụng với
A. khí O2. B. dung dịch NaOH.
C. H2O. D. dung dịch Ca(OH)2.
Câu 4: Dãy các chất nào sau đây đều tác dụng với axit clohiđric?
A. Fe2O3, KMnO4, Cu, Fe, AgNO3.
B. Fe, CuO, H2SO4, Ag, Mg(OH)2.
C. KMnO4, Cu, Fe, H2SO4, Mg(OH)2.
D. Fe2O3, KMnO4¸Fe, CuO, AgNO3.
Câu 5: Có phản ứng hoá học xảy ra như sau:
H2S + 4Cl2 + 4H2O → H2SO4 + 8HCl
Câu nào diễn tả đúng tính chất các chất phản ứng?
A. H2S là chất khử, H2O là chất oxi hoá.
B. Cl2 là chất oxi hoá. H2O là chất khử.
C. H2S là chất oxi hoá, Cl2 là chất khử.
D. Cl2 là chất oxi hoá. H2S là chất khử.
Câu 6: Cho các mệnh đề sau:
(a) Các halogen đều có số oxi hóa dương trong một số hợp chất.
(b) Halogen đứng trước đẩy được halogen đứng sau ra khỏi dung dịch muối.
(c) Các halogen đều tan được trong nước.
(d) Các halogen đều tác dụng được với hiđro.
Số mệnh đề không đúng là
A. 3. B. 2. C. 4. D. 1.
Câu 7: Để tinh chế brom bị lẫn tạp chất clo, người ta dẫn hỗn hợp qua
A. Dung dịch NaBr. B. Dung dịch NaI.
C. Dung dịch NaCl. D. Dung dịch H2SO4.
Câu 8: Cho hình vẽ mô tả thí nghiệm điều chế Clo từ MnO2 và dung dịch HCl:
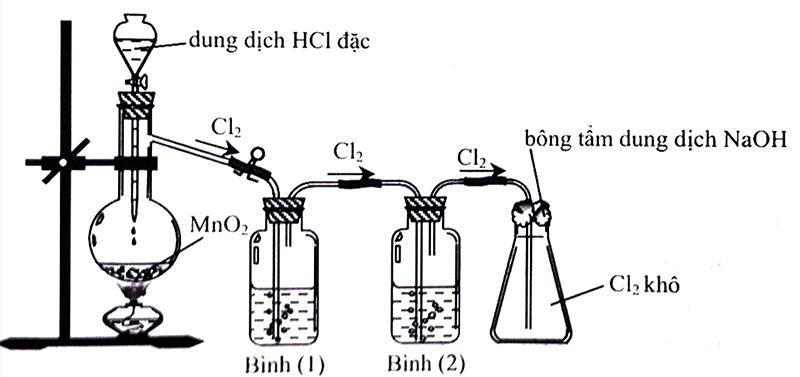
Khí Clo sinh ra thường lẫn hơi nước và khí hiđro clorua. Để thu được khí Clo khô thì bình (1) và bình (2) lần lượt đựng
A. Dung dịch H2SO4 đặc và dung dịch NaCl.
B. Dung dịch NaCl và dung dịch H2SO4 đặc.
C. Dung dịch H2SO4 đặc và dung dịch AgNO3.
D. Dung dịch NaOH và dung dịch H2SO4 đặc.
Câu 9: Hiện tượng sẽ quan sát được khi thêm dần dần nước Clo vào dung dịch KI có chứa sẵn một ít hồ tinh bột?
A. Có hơi màu tím bay lên.
B. Dung dịch chuyển màu vàng.
C. Dung dịch chuyển màu xanh đặc trưng.
D. Không có hiện tượng.
Câu 10: Phản ứng nào sau đây xảy ra không tạo muối FeCl2?
A. Fe + HCl. B. Fe3O4 + HCl.
C. Fe + Cl2. D. Fe + FeCl3.
Câu 11: Khí HCl có thể được điều chế bằng cách cho tinh thể muối ăn tác dụng với chất nào sau đây?
A. H2SO4 loãng. B. HNO3. C.NaOH. D. H2SO4 đậm đặc.
Câu 12: Dãy nào sau đây đều có tính oxi hoá và khử?
A. O2; S; SO2. B. S; SO2 ; Cl2. C. O3; H2S; SO2. D. H2SO4; S; Cl2.
Câu 13: Các khí sinh ra trong thí nghiệm phản ứng của saccarozơ (C12H22O11) với dung dịch H2SO4 đặc bao gồm:
A. H2S và CO2. B. H2S và SO2. C. SO3 và CO2. D. SO2 và CO2.
Câu 14: Trong các phản ứng sau, phản ứng nào sai?
A. Zn + 2HCl ZnCl2 + H2. B. Cu + 2HCl CuCl2 + H2.
C. CuO + 2HCl CuCl2 + H2O. D. AgNO3 + HCl AgCl + HNO3.
Câu 15: Để tinh chế brom bị lẫn tạp chất clo, người ta dẫn hỗn hợp qua
A. Dung dịch NaBr. B. Dung dịch NaI. C. Dung dịch NaCl. D. Dung dịch H2SO4.
Câu 16: Hiđro sunfua (H2S) là chất có
A. Tính axit mạnh. B. Tính oxi hóa mạnh.
C. Vừa có tính axit, vừa có tính bazơ. D. Tính khử mạnh.
Câu 17: Dãy gồm các chất đều tác dụng (trong điều kiện phản ứng thích hợp) với lưu huỳnh là
A. Hg, O2, HCl. B. Pt, Cl2, KClO3.
C. Zn, O2, F2. D. Na, Br2, H2SO4 loãng.
Câu 18: Trong các phản ứng sau đây, phản ứng nào axit H2SO4 là axit đặc?
A. H2SO4 + Na2CO3 → Na2SO4 + CO2 + H2O.
B. H2SO4 + Ca → CaSO4 + H2
C. 2H2SO4 + Cu → CuSO4 + 2H2O + SO2
D. 3H2SO4 + 2Al → Al2(SO4)3 + 3H2
Câu 19: Cho các phản ứng sau:
1. A + HCl → MnCl2 + B↑ + H2O 2. B + C → nước gia-ven
3. C + HCl → D + H2O 4. D + H2O → C + B↑+ E↑
Chất D là chất nào sau đây?
A. NaOH. B. NaCl. C. H2. D. Cl2.
Câu 20: Phản ứng nào sau đây không xảy ra?
A. H2S + Pb(NO3)2 → PbS+ 2HNO3.
B. CuS + 2HCl → H2S + CuCl2.
C. Na2S + Pb(NO3)2 PbS+ 2NaNO3.
D. FeS + HCl → H2S + FeCl2.
Câu 21: Hòa tan hoàn toàn 36,4 gam hỗn hợp X gồm kẽm và sắt, có khối lượng bằng nhau trong dung dịch axit sunfuric loãng, dư, sau phản ứng thu được dung dịch Y và V lít khí (đktc). Giá trị của V gần nhất với?
A. 12,55. B. 14,55. C. 13,44. D. 11,22.
Câu 22: Cho 5,4 gam Al và 6,4 gam Cu tác dụng với dung dịch H2SO4 đặc nóng, dư, sau phản ứng thu được dung dịch X và V lít (đktc) khí SO2, sản phẩm khử duy nhất. Giá trị của V là
A. 6,72. B. 3,36. C. 11,2. D. 8,96.
Câu 23: Cho 4,5 g hỗn hợp M gồm Mg, Al và Zn tác dụng hết với O2 dư thu được 6,5 gam hỗn hợp Y gồm các oxit. Cho Y phản ứng vừa đủ với V lít dung dịch HCl 1M. Giá trị của V là
A. 0,15. B. 0,25. C. 0,40. D. 0,30.
Câu 24: Cho 31,4g hỗn hợp hai muối NaHSO3và Na2CO3vào 400g dung dịch H2SO49,8%, đồng thời đun nóng dung dịch thu được 6,72 lít hỗn hợp khí A (đktc) và dung dịch X. Nồng độ phần trăm các chất tan trong X lần lượt là:
A. 6,86% và 4,73% B.11,28% và 3,36% C. 9,28% và 1,36% D. 15,28%và 4,36%
Câu 25: Hoà tan một oxit kim loại X hoá trị II bằng một lượng vừa đủ dung dịch H2SO4 10% ta thu được dung dịch muối có nồng độ 11,97%. X là kim loài nào sau đây:
A. Ca B. Fe C. Ba D. Mg
Câu 26: Cho 16,4 gam hỗn hợp MgCO3, Na2CO3, CaCO3 tan hết trong dung dịch HCl dư. Sau phản ứng, thu được hỗn hợp A gồm 3 muối clorua và 3,36 lít khí (đktc). Khối lượng của A là:
A. 17,74. B. 18,05. C. 17,45. D. 15,47.
Câu 27: Cho 12,1 gam hỗn hợp Zn, Fe, Mg tác dụng vừa đủ với m gam dung dịch HCl 10%. Cô cạn dung dịch sau phản ứng thu được 26,3 gam muối khan. Giá trị của m là?
A. 116 gam. B. 126 gam. C. 146 gam. D. 156 gam.
Câu 28: Nhiệt phân hoàn toàn 15,8 gam KMnO4, toàn bộ khí oxi sinh ra cho tác dụng hết với 11,7 gam kim loại R thu được chất rắn X. Cho X vào dung dịch H2SO4 loãng dư thu được 1,792 lít khí H2 (đktc). Kim loại R là
A. Zn B. Fe C. Al D. Mg
Câu 29: Đem 11,2 gam Fe để ngoài không khí, sau một thời gian thu được một hỗn hợp X gồm Fe và các oxit. Hòa tan hoàn toàn hỗn hợp đó trong dung dịch H2SO4 đặc, nóng dư, thu được dung dịch Y và 2,24 lít khí SO2 (đktc). Số mol H2SO4 đã tham gia phản ứng là
A. 0,4. B. 0,3. C. 0,5. D. 0,45.
Câu 30: Để cháy hoàn toàn hỗn hợp X gồm 3,84 gam Mg và 4,32 gam Al cần 5,824 lít hỗn hợp khí Y (đktc) gồm O2 và Cl2. Tính % thể tích Cl2 trong hỗn hợp Y?
A. 46,15%. B. 56,36%. C. 43,64%. D. 53,85%.
Các mã đề khác, mời thầy cô và các em tải đề thi tại đây:
Xem thêm
Đề cương ôn tập học kì 2 môn hóa lớp 10
Đề cương ôn tập học kì 2 môn hóa lớp 11
3 đề kiểm tra học kì 2 môn hóa lớp 11

Leave a Reply