Phương pháp quy đổi
I. Phương pháp quy đổi
1. Nội dung phương pháp quy đổi
- Cơ sở của phương pháp quy đổi là định luật bảo toàn khối lượng và bảo toàn nguyên tố.
- Định luật bảo toàn khối lượng: Trong phản ứng hóa học, tổng khối lượng chất tham gia phản ứng bằng tổng khối lượng sản phẩm tạo thành. Suy ra: Khi chuyển đổi hỗn hợp này thành hỗn hợp khác thì khối lượng được bảo toàn.
- Định luật bảo toàn nguyên tố: Trong phản ứng hóa học, các nguyên tố được bảo toàn. Suy ra: Khi chuyển đổi hỗn hợp này thành hỗn hợp khác thì nguyên tố được bảo toàn.
- Như vậy, khi chuyển đổi (quy đổi) hỗn hợp này thành hỗn hợp khác thì khối lượng và nguyên tố được bảo toàn.
- Phương pháp quy đổi là phương pháp chuyển đổi các chất phản ứng hoặc các chất sản phẩm thành các chất tương đương trên cơ sở bảo toàn khối lượng và bảo toàn nguyên tố.
2. Ưu điểm của phương pháp quy đổi
a. Xét các hướng giải bài tập sau:
Câu 41 – Mã 253: Hỗn hợp X gồm 1 mol aminoaxit no, mạch hở và 1 mol amin no, mạch hở. X có khả năng phản ứng tối đa với 2 mol HCl hoặc 2 mol NaOH. Đốt cháy hoàn toàn X thu được 6 mol CO2, x mol H2O và y mol N2. Các giá trị x, y tương ứng là
A. 8 và 1,0. B. 8 và 1,5. C. 7 và 1,0. D. 7 và 1,5.
(Đề thi tuyển sinh Đại học khối A năm 2010)

● Cách 2: Sử dụng phương pháp quy đổi
Theo giả thiết, X gồm amin no, mạch hở và amino axit no, mạch hở.
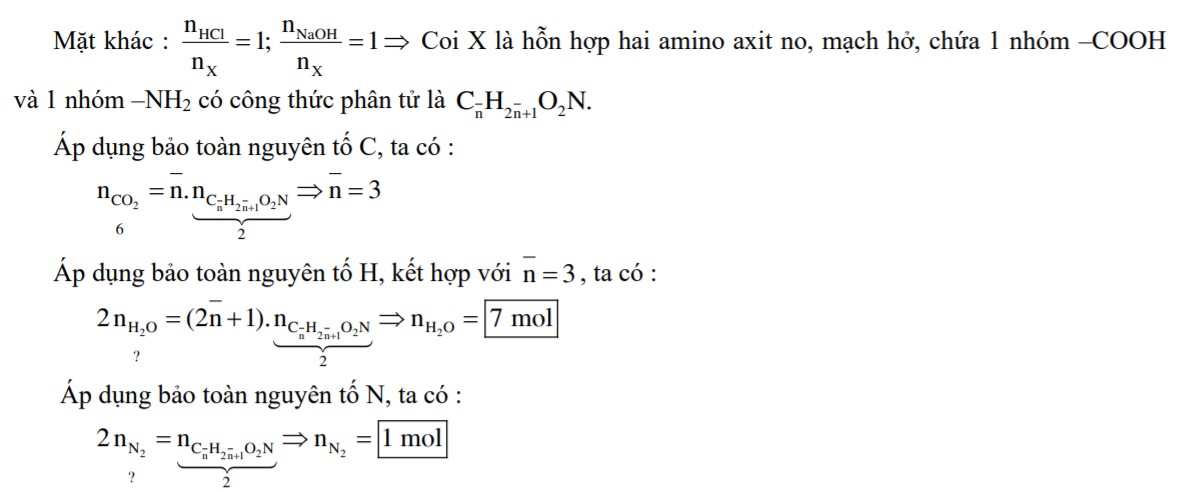
b. Nhận xét:
Với cách 1: Ta đi tìm công thức tổng quát của amin và amino axit. Việc xây dựng công thức của amin thì khá đơn giản vì đó là amin no, đơn chức (dạng quen thuộc). Nhưng xây dựng công thức của amino axit no, mạch hở chứa 1 nhóm –NH2 và 2 nhóm –COOH thì phức tạp hơn, chắc chắn có nhiều học sinh sẽ lúng túng (vì đây không phải là dạng công thức quen thuộc). Cách đơn giản nhất là lấy một ví dụ cụ thể, chẳng hạn là H2NCH(COOH)2, rồi từ đó suy ra công thức tổng quát. Sau khi xây dựng được công thức của các chất trong X, ta phải tiếp tục lập sơ đồ phản ứng cháy để tìm số mol của H2O và N2. Như vậy, làm theo cách 1 sẽ mất thời gian vào việc lập công thức và viết sơ đồ đốt cháy X để tính toán.
Với cách 2: Nhận thấy . Mặt khác đề cho các chất trong X là no, mạch hở nên coi X là hai amino axit no, mạch hở, phân tử có 1 nhóm –NH2 và 1 nhóm –COOH (dạng quen thuộc). Đến đây, sử dụng công thức trung bình cho hai chất và áp dụng bảo toàn nguyên tố thì dễ dàng tính được số mol của H2O và N2.
c. Kết luận:
Phương pháp quy đổi không giúp ta giải quyết được bài toán một cách triệt để, nhưng nhờ nó mà việc tính toán trong một số bài tập có chứa hỗn hợp nhiều chất trở nên đơn giản hơn, dễ dàng hơn và nhanh chóng hơn.
3. Phạm vi áp dụng của phương pháp quy đổi:
Phương pháp quy đổi có thể giải quyết được một số dạng bài tập hóa vô cơ hoặc hóa hữu cơ, có thể là phản ứng oxi hóa – khử hoặc phản ứng không oxi hóa – khử.
Một số dạng bài tập thường dùng phương pháp quy đổi là:
- Hỗn hợp (Fe, FeO, Fe2O3, Fe3O4); (Fe, S, FeS, FeS2), (Fe, Cu, FeS, FeS2, CuS, Cu2S); (Cu, FexOy),…tác dụng với dung dịch HNO3 hoặc H2SO4 đặc, nóng.
- Hỗn hợp (Mg, Ca, MgO, CaO); (K, Na, Na2O, K2O),… tác dụng với dung dịch HCl hoặc H2SO4 loãng.
- Hỗn hợp (FeO, Fe2O3, Fe3O4) phản ứng với dung dịch HCl hoặc H2SO4 loãng.
- Đốt cháy hỗn hợp các chất bằng hỗn hợp O2, O3.
- Đốt cháy hỗn hợp các chất hữu cơ.
- Hỗn hợp các chất trong đó có những chất có khối lượng phân tử bằng nhau và tính chất tương tự nhau.
II. Phân dạng bài tập và các ví dụ minh họa
1. Dạng 1: Quy đổi chất
Phương pháp giải
– Bước 1: Nhận dạng nhanh phương pháp giải bài tập
Khi gặp một trong các dấu hiệu sau đây thì ta nên sử dụng phương pháp quy đổi chất: (1) Bài tập có hỗn hợp nhiều chất được cấu tạo bởi 1, 2 hay 3 nguyên tố; (2) Bài tập có các chất phản ứng ở dạng tổng quát (FexOy, CxHy,…); (3) Bài tập có hỗn hợp nhiều chất trong đó có những chất có cùng khối lượng mol hoặc cùng công thức phân tử, công thức đơn giản nhất; (4) Bài tập có hỗn hợp các chất trong đó có những chất có mối liên quan với nhau về số mol.
– Bước 2: Tiến hành quy đổi: Đối với các dạng bài tập có dấu hiệu (1) hoặc (2) ta nên quy đổi hỗn hợp ban đầu hoặc chất ban đầu thành hỗn hợp các nguyên tử. Đối với bài tập có dấu hiệu (3) ta nên quy đổi những chất có cùng công thức phân tử, hoặc cùng khối lượng mol thành một chất; Đối với bài tập có dấu hiệu (4) thì tùy thuộc vào từng bài cụ thể mà ta lựa chọn cách quy đổi sao cho hợp lý nhất.
– Bước 3: Lập sơ đồ phản ứng biểu diễn quá trình chuyển hóa giữa các chất, để thấy rõ hơn bản chất hóa học của bài toán.
– Bước 4: Kết hợp với các phương pháp bảo toàn electron, bảo toàn nguyên tố, bảo toàn điện tích, bảo toàn khối lượng để thiết lập các phương trình toán học liên quan đến số mol, khối lượng, thể tích của các chất cần tìm, giải phương trình hoặc hệ phương trình để tìm kết quả.
► Các ví dụ minh họa ◄
a. Bài tập có hỗn hợp nhiều chất được cấu tạo bởi 1, 2 hay 3 nguyên tố
Ví dụ 1: Hỗn hợp X gồm Na, Ba, Na2O và BaO. Hòa tan hoàn toàn 21,9 gam X vào nước, thu được 1,12 lít khí H2 (đktc) và dung dịch Y, trong đó có 20,52 gam Ba(OH)2. Hấp thụ hoàn toàn 6,72 lít khí CO2 (đktc) vào Y, thu được m gam kết tủa. Giá trị của m là
A. 23,64. B. 15,76. C. 21,92. D. 39,40.
(Đề thi tuyển sinh Đại học khối A năm 2013)
Hướng dẫn giải
● Bước 1: Nhận dạng nhanh phương pháp giải bài tập
Đề bài cho biết hỗn hợp X gồm có 4 chất là Na, Ba, Na2O và BaO. Tuy nhiên, ta thấy X chỉ được tạo thành từ 3 loại nguyên tố là Na, Ba, O. Đây là dấu hiệu (1), chứng tỏ bài tập này sẽ sử dụng phương pháp quy đổi.
● Bước 2: Tiến hành quy đổi
Quy đổi hỗn hợp X gồm Na, Ba, Na2O và BaO thành hỗn hợp X’ gồm Na, Ba, O.
● Bước 3: Lập sơ đồ phản ứng biểu diễn quá trình chuyển hóa giữa các chất, để thấy rõ hơn bản chất hóa học của bài toán
Ta coi hỗn hợp đầu tiên là X’, còn X là hỗn hợp trung gian.
Căn cứ vào sơ đồ phản ứng, ta thấy: Chất khử là Na, Ba; chất oxi hóa là O và H2O; sản phẩm khử của H2O là H2.
● Bước 4: Kết hợp với các phương pháp bảo toàn electron, bảo toàn nguyên tố, bảo toàn điện tích, bảo toàn khối lượng để thiết lập các phương trình toán học liên quan đến số mol, khối lượng, thể tích của các chất cần tìm, giải phương trình hoặc hệ phương trình để tìm kết quả.
Theo giả thiết, ta có:
Theo bảo toàn electron và bảo toàn khối lượng, ta có:
Vậy dung dịch Y có 0,14 mol NaOH và 0,12 mol Ba(OH)2. Suy ra:
tạo ra cả
Vì phản ứng tạo ra cả hai muối, nên sử dụng kết quả đã chứng minh ở chuyên đề bảo toàn điện tích, ta có:
Ví dụ 2: Hỗn hợp X gồm CaO, Mg, Ca, MgO. Hòa tan 5,36 gam hỗn hợp X bằng dung dịch HCl vừa đủ thu được 1,624 lít H2 (đktc) và dung dịch Y trong đó có 6,175 gam MgCl2 và m gam CaCl2. Giá trị của m là
A. 7,4925 gam. B. 7,770 gam. C. 8,0475 gam. D. 8,6025 gam.
(Đề thi thử Đại học lần 4 – THPT Chuyên Vĩnh Phúc, năm học 2011 – 2012)
Hướng dẫn giải
Quy đổi hỗn hợp X thành hỗn hợp X’ gồm Ca, Mg, O.
Sơ đồ phản ứng:
Từ sơ đồ phản ứng, ta thấy: Chất khử là Ca, Mg; chất oxi hóa là H+ trong HCl và O; sản phẩm khử của H+ là H2;
Áp dụng bảo toàn electron, bảo toàn khối lượng và bảo toàn nguyên tố Ca, ta có:
O2 Education gửi các thầy cô link download file pdf đầy đủ tại đây PP7 – QUY ĐỔI
Xem thêm

Leave a Reply