Đề thi THPT QG 2021 file word có lời giải chi tiết đề số 6
|
ĐỀ MINH HỌA SỐ 06 |
KỲ THI TRUNG HỌC PHỔ THÔNG QUỐC GIA NĂM 2021 Bài thi: Khoa học tự nhiên; Môn: Hóa Học Thời gian làm bài: 50 phút, không kể thời gian phát đề |
Cho biết nguyên tử khối của các nguyên tố: H=1; O=16; S=32; F=19; Cl=35,5; Br=80; I=127; N=14; P=31; C=12; Si=28; Li=7; Na=23; K=39; Mg=24; Ca=40; Ba=137; Sr=88; Al=27;Fe=56, Cu=64; Pb=207; Ag=108.
Câu 1: Cho các chất có công thức cấu tạo sau đây:
(1) CH3CH2COOCH3; (2) CH3OOCCH3;
(3) HCOOC2H5; (4) CH3COC2H5.
Chất không thuộc loại este là
A. (2). B. (1). C. (4). D. (3).
Câu 2: Cho phương trình hóa học của hai phản ứng sau:
FeO + CO Fe + CO2
3FeO + 10HNO3 3Fe(NO3)3 + NO + 5H2O
Hai phản ứng trên chứng tỏ FeO là chất
A. vừa có tính oxi hóa, vừa có tính khử. B. chỉ có tính oxi hóa.
C. chỉ có tính bazơ. D. chỉ có tính khử.
Câu 3: Nước muối sinh lí để sát trùng, rửa vết thương trong y học có nồng độ
A. 5%. B. 9%. C. 1%. D. 0,9%.
Câu 4: Cho hỗn hợp các kim loại Fe, Mg, Zn vào cốc đựng dung dịch CuSO4 dư, thứ tự các kim loại tác dụng với muối là:
A. Mg, Zn, Fe. B. Mg, Fe, Zn. C. Fe, Zn, Mg. D. Zn, Mg, Fe.
Câu 5: Khi nói về peptit và protein, phát biểu nào sau đây là đúng?
A. Thủy phân hoàn toàn protein đơn giản thu được các -amino axit.
B. Tất cả các peptit và protein đều có phản ứng màu biure với Cu(OH)2.
C. Liên kết của nhóm CO với nhóm NH giữa hai đơn vị amino axit được gọi là liên kết peptit.
D. Oligopeptit là các peptit có từ 2 đến 10 liên kết peptit.
Câu 6: Cho dãy gồm các chất: metyl metacrylat; triolein; saccarozơ; xenlulozơ; glyxylalanin; tơ nilon-6,6. Số chất trong dãy bị thủy phân khi đun nóng trong môi trường axit là
A. 3. B. 4. C. 5. D. 6.
Câu 7: Thực hiện một số thí nghiệm với 4 chất hữu cơ, thu được kết quả như sau:
-
Chất
Thuốc thử
X
Y
Z
T
Cu(OH)2
Có xảy ra phản ứng
Có xảy ra phản ứng
Có xảy ra phản ứng
Không xảy ra phản ứng
Dung dịch AgNO3/NH3
Tạo kết tủa trắng bạc
Không xảy ra phản ứng
Không xảy ra phản ứng
Không xảy ra phản ứng
Dung dịch NaOH
Không xảy ra phản ứng
Có xảy ra phản ứng
Không xảy ra phản ứng
Có xảy ra phản ứng
Các chất X, Y, Z, T lần lượt là:
A. fructozơ, Ala-Gly-Val, saccarozơ, anilin. B. fructozơ, Ala-Gly-Val, tinh bột, anilin.
C. glucozơ, Gly-Ala-Val, xelulozơ, alanin. D. glucozơ, Gly-Ala-Val, saccarozơ, alanin.
Câu 8: Khi thủy phân đến cùng xenlulozơ thì thu được sản phẩm là
A. Fructozơ. B. Tinh bột. C. Glucozơ. D. Saccarozơ.
Câu 9: Dãy gồm các chất không tác dụng với dung dịch NaOH là
A. Al, NaHCO3, Al(OH)3. B. Al2O3, Na2CO3, AlCl3.
C. Al, FeCl2, FeCl3. D. NaAlO2, Na2CO3, NaCl.
Câu 10: Có 5 hỗn hợp, mỗi hỗn hợp gồm 2 chất rắn có số mol bằng nhau: Na2O và Al2O3; Cu và Fe2(SO4)3; KHSO4 và KHCO3; BaCl2 và CuSO4; Fe(NO3)2 và AgNO3. Số hỗn hợp có thể tan hoàn toàn trong nước (dư) chỉ tạo ra các chất tan trong nước là
A. 4. B. 2. C. 3. D. 5.
Câu 11: Chất X tan trong nước và tác dụng được với dung dịch H2SO4 loãng. Chất X là chất nào sau đây?
A. FeS. B. CuS. C. Na2S. D. PbS.
Câu 12: Nhiệt phân muối nào sau đây thu được kim loại?
A. Cu(NO3)2. B. AgNO3. C. NaNO3. D. Fe(NO3)2.
Câu 13: Oxi nào sau đây tác dụng với H2O tạo hỗn hợp axit?
A. SO3. B. P2O5. C. SO2. D. CrO3.
Câu 14: Nước cứng có chứa nhiều các ion nào sau đây?
A. Zn2+, Al3+. B. Cu2+, Fe2+. C. Ca2+, Mg2+. D. K+, Na+.
Câu 15: Ở thí nghiệm nào sau đây Fe chỉ bị ăn mòn hóa học?
A. Cho hợp kim Fe – Cu vào dung dịch CuSO4. B. Đốt cháy dây sắt trong không khí khô.
C. Để mẫu gang lâu ngày trong không khí ẩm. D. Cho Fe vào dung dịch AgNO3.
Câu 16: Amino axit nào sau đây có phân tử khối bé nhất?
A. Axit glutamic. B. Valin. C. Glyxin. D. Alanin.
Câu 17: Cấu hình electron lớp ngoài cùng của nguyên tử kim loại kiềm thổ là
A. ns2. B. ns2np1. C. ns1. D. ns2np2.
Câu 18: Dãy nào sau đây gồm các polime dùng làm chất dẻo?
A. polietilen; poli(vinyl clorua); poli(metyl metacrylat).
B. nilon-6; xenlulozơ triaxetat; poli(phenol-fomanđehit).
C. polibuta-1,3-đien; poli(vinyl clorua); poli(metyl metacrylat).
D. poli stiren; nilon-6,6; polietilen.
Câu 19: Cho dãy các kim loại Mg, Cr, K, Li. Kim loại mềm nhất trong dãy là
A. K. B. Mg. C. Cr. D. Li.
Câu 20: Phát biểu nào sau đây là sai?
A. Thủy phân đến cùng protein đơn giản luôn thu được α-amino axit.
B. Mặt cắt củ khoai tác dụng với I2 cho màu xanh tím.
C. Sản phẩm của phản ứng xà phòng hoá chất béo là axit béo và glixerol.
D. Cho Cu(OH)2 vào ống nghiệm chứa anbumin thấy tạo dung dịch màu tím.
Câu 21: Phát biểu sai là
A. Tất cả các kim loại đều có ánh kim.
B. Phần lớn các nguyên tử kim loại đều có từ 1- 3e lớp ngoài cùng.
C. Trong một chu kì, theo chiều Z tăng, tính kim loại tăng dần.
D. Kim loại có độ âm điện bé hơn phi kim.
Câu 22: Tính chất hóa học đặc trưng của kim loại là
A. Tính oxi hóa. B. Tính khử.
C. Tác dụng với phi kim. D. Tác dụng với axit.
Câu 23: Khi lên men 360 gam glucozơ với hiệu suất 100%, khối lượng ancol etylic thu được là
A. 138 gam. B. 92 gam. C. 276 gam. D. 184 gam.
Câu 24: Xà phòng hoá hoàn toàn 8,8 gam CH3COOC2H5 trong 150 ml dung dịch NaOH 1,0M. Cô cạn dung dịch sau phản ứng thu được m gam chất rắn khan. Giá trị của m là
A. 8,20. B. 12,30. C. 10,20. D. 14,80.
Câu 25: Cho m gam bột Al vào dung dịch NaOH (dư), sau phản ứng hoàn toàn thu được 6,72 lít khí H2 (ở đktc). Giá trị của m là
A. 5,4. B. 2,7. C. 16,2. D. 10,4.
Câu 26: Hai este A và B là đồng phân của nhau và đều do axit cacboxylic no, đơn chức và ancol no đơn chức tạo thành. Để xà phòng hóa hoàn toàn 33,3 gam hỗn hợp hai este trên cần vừa đủ 450 ml dung dịch NaOH 1M. Tên gọi của 2 este đó là:
A. etyl fomat và metyl axetat. B. etyl axetat và propyl fomat.
C. butyl fomat và etyl propionat. D. metyl axetat và metyl fomat.
Câu 27: Thủy phân hoàn toàn 1 mol pentapeptit X mạch hở thì thu được 3 mol glyxin, 1 mol alanin và 1 mol valin. Khi thủy phân không hoàn toàn X thì trong sản phẩm thấy có các đipeptit Ala-Gly, Gly-Ala và tripeptip Gly-Gly-Val. Công thức của X và phần trăm khối lượng của N trong X là:
A. Ala-Gly-Gly-Val-Gly; 11,2%. B. Gly-Ala-Gly-Gly-Val; 19,5%.
C. Gly-Gly-Val-Gly-Ala; 15%. D. Gly-Ala-Gly-Gly-Val; 20,29%.
Câu 28: Có một cốc đựng m gam dung dịch HNO3 và H2SO4. Hoà tan hết 3,64 gam kim loại M (có hoá trị không đổi) vào dung dịch trong cốc thì thu được 2,1504 lít (đktc) hỗn hợp 2 khí NO2 và X. Sau phản ứng, khối lượng các chất trong cốc giảm 1,064 gam. Kim loại M là
A. Cu. B. Fe. C. Al. D. Zn.
Câu 29: Cho 11,25 gam C2H5NH2 tác dụng với 200 ml dung dịch HCl a(M). Sau khi phản ứng hoàn toàn thu được dung dịch có chứa 22,2 gam chất tan. Giá trị của a là
A. 1,3. B. 1,5. C. 1,25. D. 1,36.
Câu 30: Cho 18,3 gam hỗn hợp gồm Ba và Na vào 1 lít dung dịch CuSO4 0,5M, sau khi các phản ứng xảy ra hoàn toàn, thu được m gam kết tủa và 4,48 lít khí H2 (đktc). Giá trị của m là
A. 40,5. B. 45,5. C. 50,8. D. 42,9.
Câu 31: Cho các phản ứng xảy ra theo sơ đồ sau:
Chất X là
A. metyl acrylat. B. etyl axetat. C. vinyl axetat. D. etyl fomat.
Câu 32: Hoà tan hoàn toàn 7,8 gam hỗn hợp Mg và Al bằng dung dịch HCl dư. Sau phản ứng thấy khối lượng dung dịch tăng thêm 7,0 gam so với ban đầu. Số mol axit đã tham gia phản ứng là
A. 0,8 mol. B. 0,08 mol. C. 0,04 mol. D. 0,4 mol.
Câu 33: Khử m gam Fe3O4 bằng khí H2, thu được hỗn hợp X gồm Fe và FeO, hỗn hợp X tác dụng vừa hết với 3 lít dung dịch H2SO4 0,2M (loãng). Giá trị của m là
A. 23,2. B. 34,8. C. 11,6. D. 46,4.
Câu 34: Đốt cháy hoàn toàn 15,84 gam hỗn hợp 2 este CH3COOC2H5 và C2H5COOCH3, cho toàn bộ sản phẩm cháy qua dung dịch nước vôi trong thấy khối lượng bình tăng m gam. Giá trị của m là
A. 12,96. B. 44,64. C. 31,68. D. 27,36.
Câu 35: Aspirin là loại dược phẩm có tác dụng giảm đau, hạ sốt, chống viêm,… Axit axetylsalixylic là thành phần chính của aspirin, nó được tổng hợp từ phenol. Phân tích nguyên tố cho thấy trong axit axetylsalixylic có chứa 60% C; 4,44% H; 35,56% O. Công thức cấu tạo thu gọn phù hợp với công thức phân tử của axit axelylsalixylic là
A. C6H4(COOH)(OCOC2H5) (thơm). B. C6H4(OH)(OCOCH3) (thơm).
C. C6H4(COOH)(OCOCH3) (thơm). D. C6H4(OH)(COOH) (thơm).
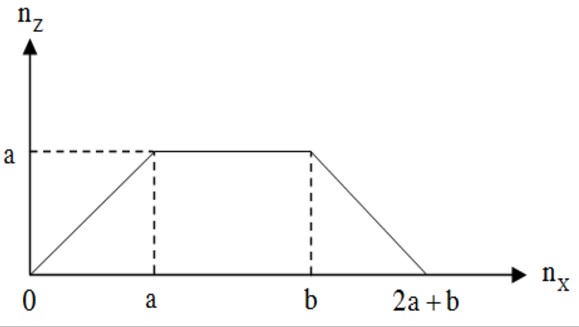
Câu 36: Khi nhỏ từ từ đến dư dung dịch HCl vào dung dịch chứa NaOH và NaAlO2 (hay Na[Al(OH)4]), kết quả thí nghiệm được biểu diễn bằng đồ thị bên:

Giá trị của x là
A. 3. B. 2. C. 1,6. D. 2,4.
Câu 37: Hỗn hợp X gồm 0,1 mol một α-amino axit no, mạch hở E chứa 1 nhóm –NH2, 1 nhóm –COOH và 0,025 mol pentapeptit mạch hở cấu tạo từ E. Đốt cháy hỗn hợp X cần a mol O2, sản phẩm cháy hấp thụ hết vào 1 lít dung dịch NaOH 1,2M thu được dung dịch Y. Rót từ từ dung dịch chứa 0,8a mol HCl vào dung dịch Y thu được 14,448 lít CO2 (đktc). Đốt 0,01a mol đipeptit mạch hở cấu tạo từ E cần V lít O2 (đktc). Giá trị của V là
A. 2,2491. B. 2,5760. C. 2,3520. D. 2,7783.
Câu 38: Đun hỗn hợp etylen glicol và axit cacboxylic X (phân tử chỉ có nhóm -COOH) với xúc tác H2SO4 đặc, thu được hỗn hợp sản phẩm hữu cơ, trong đó có chất hữu cơ Y mạch hở. Đốt cháy hoàn toàn 3,95 gam Y cần 4,00 gam O2, thu được CO2 và H2O theo tỉ lệ mol tương ứng 2 : 1. Biết Y có công thức phân tử trùng với công thức đơn giản nhất, Y phản ứng được với NaOH theo tỉ lệ mol tương ứng 1: 2. Phát biểu nào sau đây sai?
A. X có đồng phân hình học.
B. Tổng số nguyên tử hiđro trong hai phân tử X, Y bằng 8.
C. Y không có phản ứng tráng bạc.
D. Y tham gia được phản ứng cộng với Br2 theo tỉ lệ mol tương ứng 1 : 2.
Câu 39: Cho 7,65 gam hỗn hợp X gồm Al và Al2O3 (trong đó Al chiếm 60% khối lượng) tan hoàn toàn trong dung dịch Y gồm H2SO4 và NaNO3, thu được dung dịch Z chỉ chứa 3 muối trung hòa và m gam hỗn hợp khí T (trong T có 0,015 mol H2). Cho dung dịch BaCl2 dư vào Z đến khi các phản ứng xảy ra hoàn toàn, thu được 93,2 gam kết tủa. Còn nếu cho Z phản ứng với NaOH thì lượng NaOH phản ứng tối đa là 0,935 mol. Giá trị của m gần giá trị nào nhất sau đây?
A. 1,0. B. 1,5. C. 2,5. D. 3,0.
Câu 40: Hòa tan hoàn toàn m gam hỗn hợp gồm Na2O và Al2O3 vào nước, thu được dung dịch X. Thêm từ từ dung dịch HCl 1M vào X, khi hết 100 ml thì bắt đầu xuất hiện kết tủa; khi hết 300 ml hoặc 700 ml thì đều thu được a gam kết tủa. Giá trị của a và m lần lượt là
A. 15,6 và 55,4. B. 15,6 và 27,7. C. 23,4 và 56,3. D. 23,4 và 35,9.
———– HẾT ———-
O2 education gửi các thầy cô link download file word đề và lời giải chi tiết
Xem thêm
Tổng hợp đề thi THPT QG 2021 file word có lời giải chi tiết
Đề thi THPT QG 2021 file word có lời giải chi tiết đề số 1
Đề thi THPT QG 2021 file word có lời giải chi tiết đề số 2
Đề thi THPT QG 2021 file word có lời giải chi tiết đề số 3
Đề thi THPT QG 2021 file word có lời giải chi tiết đề số 4
Đề thi THPT QG 2021 file word có lời giải chi tiết đề số 5
Đề thi THPT QG 2021 file word có lời giải chi tiết đề số 6
Đề thi THPT QG 2021 file word có lời giải chi tiết đề số 7
Đề thi THPT QG 2021 file word có lời giải chi tiết đề số 8