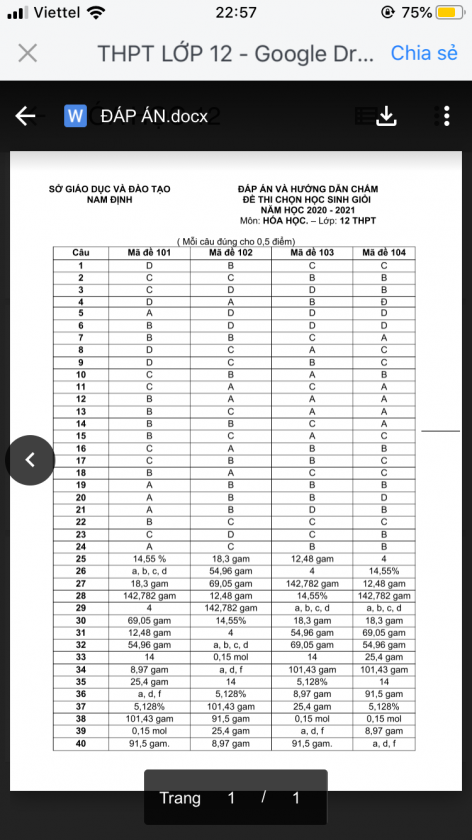
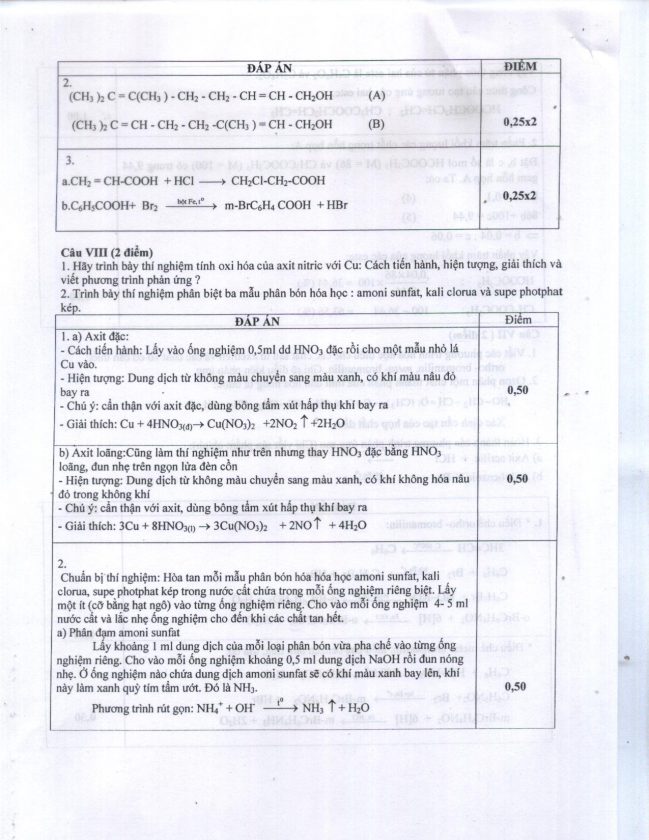
Đề thi hsg lớp 12 môn hóa THPT Hiệp Hòa Bắc Giang
|
TRƯỜNG THPT HIỆP HÒA SỐ 4 |
ĐỀ THI CHỌN HSG VĂN HÓA CẤP TRƯỜNG NĂM HỌC 2017-2018 MÔN : HÓA HỌC 12 (Thời gian: 120 phút) |
Họ, tên thí sinh:…………………………………………………………… . Số báo danh
Cho nguyên tử khối: Be = 9; C = 12; N = 14; O = 16; Na = 23; Mg = 24; Al = 27; S = 32; Cl = 35,5; K = 39; Ca = 40; Sr=88; Mn = 55; Fe = 56; Cu = 64; Zn = 65; Ag = 108; Cr=52; Ba = 137; Br = 80.
PHẦN TRẮC NGHIỆM ( 7 ĐIỂM )
Câu 1.Nhóm kim loại nào sau đây có thể được điều chế bằng: phương pháp thủy luyện, nhiệt luyện, điện phân
A. Mg, Ag B. Cu, Fe C. Al, Fe D. Cu, Mg
Câu 2. Hiện nay người ta đang khuyến khích dùng xăng sinh học thay thế xăng sản xuất từ nguyên liệu hóa thạch, xăng sinh học E5 là một loại bắt đầu được sử dụng. Tên của xăng có nghĩa là
A. Xăng chứa 95% xăng A92 trộn với 5% Etanol khan B. Xăng có chỉ số octan là 95
C. Xăng chứa 5% ete D. Xăng sinh học ở thế hệ thứ 5
Câu 3: Chất nào sau đây vừa phản ứng với dung dịch NaOH vừa phản ứng với HCl?
A. Na2CO3 B. Al2(SO4)3 C. P2O5 D. Ca(H2PO4)2
Câu 4. Oxit nào sau đây tác dụng với dung dịch HNO3 loãng, dư sản phẩm sinh ra có chất khí?
A. Al2O3. B. FeO. C. CaO. D. Na2O.
Câu 5. Polime nào sau đây được tổng hợp bằng phản ứng trùng hợp?
A. Polisaccarit. B. Polibutađien. C. Poli(etylen terephatalat). D. Nilon-6,6.
Câu 6. Việc làm nào sau đây không đúng về cơ sở khoa học
A.Trộn phân đạm ure với vôi bột để bón ruộng B. Dùng lọ nhựa chứa dung dịch HF
C. Thu khí NH3 sau khi điều chế bằng pp dời không khí D.Rửa lọ đựng phenol bằng dd HCl sau đó tráng nước
Câu 7. Sản phẩm của phản ứng este hóa giữa ancol etylic và axit fomic là
A. etyl axetat. B. etyl fomat. C. metyl fomat. D. etyl axetat.
Câu 8. Dung dịch chất nào sau đây không làm quỳ tím chuyển màu?
A. Etylamin. B. Anilin. C. Metylamin. D. Đimetylamin.
Câu 9. Trong các kim loại: Al, Cr, Fe và Zn, kim loại có tính khử mạnh nhất và yếu nhât lần lượt là
A. Cr và Al. B. Al và Fe. C. Fe và Cr. D. Zn và Fe.
Câu 10. Chất nào sau đây không phản ứng với NaOH trong dung dịch?
A. Ala-Val. B. Alanin. C. Metylamin. D. Metyl axetat.
Câu 11. Đá vôi là nguyên liệu có sẵn trong tự nhiên, được dùng làm vật liệu xây dựng, sản xuất vôi,… Nung 110 kg đá vôi (chứa 80% CaCO3 về khối lượng, còn lại là tạp chất trơ) đến khối lượng không đổi, thu được m kg chất rắn. Giá trị của m là
A. 88,00. B. 49,28. C. 71,28. D. 61,60.
Câu 12. Kim loại nào khi tác dụng được với chất: O2, Cl2, S, HCl (ở điều kiện thích hợp) đều bị đưa lên cùng số oxh ?
A. Cu và Cr. B. Ag và Al. C. Al và Zn D. Fe và Zn
Câu 13. Cho 5 gam hỗn hợp X gồm Cu và Fe vào dung dịch HCl dư. Sau khi phản ứng xảy ra hoàn toàn, thu được 1,12 lít khí H2 (đktc). Phần trăm khối lượng của Fe trong X là
A. 44,0%. B. 56,0%. C. 28,0%. D. 72,0%.
Câu 14. Cho 6,5 gam Zn tác dụng với V lit dung dịch HCl 0,11M, sau khi phản ứng xảy ra hoàn toàn thu dung dịch có pH = 2. Giá trị của V là
A.1lit B. 2 lit C.1,1lit D. 1,2 lit
Câu 15. Cho hỗn hợp gồm CH3COOC2H5 và CH3COONH4 tác dụng vừa đủ với 200 ml dung dịch NaOH 0,5M, thu được dung dịch chứa m gam muối. Giá trị của m là
A. 9,8. B. 4,9. C. 8,2. D. 4,1.
Câu 16. Cho hỗn hợp ( Zn, Cu, Ag ) vào dung dịch hỗn hợp ( Cu(NO3)2 và AgNO3 ), sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch X chứa hai ion kim loại. Hai ion kim loại đó là
A. Cu2+, Ag+. B. Zn2+, Cu2+. C. Zn2+, Ag+. D. Zn2+, Ag+.
Câu 17. Hòa tan hoàn toàn 2,35 gam K2O vào 77,65 gam nước, thu được dung dịch KOH có nồng độ x %. Giá trị của x là
A. 3,5. B. 4,0. C. 5,5. D. 6,0.
Câu 18. Cho axit axetic tác dụng với ancol no đơn chức, mạch hở X, thu được este Y. Trong Y, oxi chiếm 36,36 % về khối lượng. Công thức của Y là
A. C2H3COOCH3. B. CH3COOC3H5 . C. C2H5COOC2H3 . D. CH3COOC2H5.
Câu 19. Cho dãy các chất sau: triolein, axit aminoaxetic, Gly-Ala, etyl axetat. Số chất trong dãy có phản ứng với dung dịch NaOH (đun nóng) là
A. 2. B. 4. C. 1. D. 3.
Câu 20. Phát biểu nào sau đây đúng?
A. Protein đơn giản là những chất có tối đa 10 liên kết peptit.
B. Protein phản ứng với Cu(OH)2 trong môi trường kiềm tạo màu xanh tím.
C. Protein bị thủy phân nhờ xúc tác axit, bazơ hoặc enzim.
D. Protein đơn giản bị thủy phân (xúc tác) cuối cùng thành các -amino axit.
Câu 21. Xà phòng hóa hoàn toàn este X mạch hở trong dung dịch NaOH, thu được hỗn hợp các chất hữu cơ gồm: (COONa)2, CH3CHO và C2H5OH. Công thức phân tử của X là
A. C5H8O4. B. C6H10O4. C. C5H6O4. D. C6H8O4.
Câu 22. Cho hình vẽ mô tả thí nghiệm điều chế khí Z từ dung dịch X và chất rắn Y:
Hình vẽ trên minh họa cho phản ứng nào sau đây
A. K2SO3 (rắn) + H2SO4K2SO4 + SO2 + H2O
B. CuO (rắn) + CO (khí) Cu + CO2
C. NaOH + NH4Cl (rắn) NH3 + NaCl + H2O
D. Fe + H2SO4 (loãng) FeSO4 + H2
Câu 23. Cho một lương dư bột sắt vào dung dịch HNO3, sau khi phản ứng hoàn toàn, thu được 2,912 lít khí NO (sản phẩm khử duy nhất của N+5, ở đktc). Khối lương bột sắt đã phản ứng là
A. 7,80. B. 10,92. C. 4,16. D. 7,28.
Câu 24. Hỗn hợp E gồm ba amin no, đơn chức. Đốt cháy hoàn toàn m gam E bằng O2 , thu được CO2, H2O và 0,336 lít khí N2 (đktc). Mặt khác, để tác dụng với m gam E cần vừa đủ V ml dung dịch HCl 1M.Giá trị của V là
A. 22,5. B. 30,0. C. 7,5. D. 15,0.
Câu 25. Điện phân (với điện cực trơ, cường độ dòng điện không đổi) dung dịch muối sunfat của một kim loại R (có hóa trị không đổi). Sau thời gian t giây, khối lượng dung dịch giảm 8,0 gam và tại catot chỉ thu được x gam kim loại R. Sau thời gian 2t giây, khối lượng dung dịch giảm 9,8 gam và tại catot thoát ra 2,24 lít khí (đktc). Giá trị của x là
A. 8,64. B. 6,40. C. 6,48. D. 5,60.
Câu 26. Cho các phát biểu sau:
(a) Thủy phân vinyl axetat bằng NaOH đun nóng, thu được natri axetat và fomanđehit.
(b) Polietilen được điều chế bằng phản ứng trùng hợp.
(c) Ở điều kiện thường, anilin là chất khí.
(d) Xenlulozơ thuộc loại polisaccarit.
(e) Thủy phân hoàn toàn anbumin thu được hỗn hợp α-amino axit.
(g) Ở điều kiện thích hợp, triolein tham gia phản ứng cộng H2.
Số phát biểu đúng là
A. 3. B. 2. C. 4. D. 5.
Câu 27. Cho sơ đồ chuyển hóa:
![]()
Biết các chất Y, Z, T là các hợp chất của crom. Chất Z là
A. Cr(OH)3. B. K2CrO4 . C. KCrO2. D. Cr2(SO4)3.
Câu 28. Cho 1 mol triglixerit X tác dụng với dung dịch NaOH dư, thu được 1 mol glixerol, 1 mol natri panmitat và 2 mol natri oleat. Phát biểu nào sau đây sai?
A. Phân tử X có 3 liên kết π. B. Có 2 đồng phân cấu tạo thỏa mãn tính chất của X.
C. Công thức phân tử chất X là C55H102O6. D. 1 mol X làm mất màu tối đa 2 mol Br2 trong dung dịch.
Câu 29. Tiến hành các thí nghiệm sau:
(a) Điện phân NaCl nóng chảy. (b) Điện phân dung dịch CuSO4 (điện cực trơ).
(c) Cho mẩu Na vào dung dịch Al(NO3)3. (d) Cho Fe vào dung dịch CuSO4.
(e) Cho Ag vào dung dịch HCl. (g) Cho Cu vào dung dịch hỗn hợp Cu(NO3)2 và Na2SO4.
Số thí nghiệm thu được chất khí là
A. 4. B. 5. C. 2. D. 3.
Câu 30. Cho 1 mol chất X (C8H6O4, chứa vòng benzen) tác dụng hết với NaOH dư, thu được 2 mol chất Y, 1 mol chất Z và 2 mol H2O. Chất Z tác dụng với dung dịch H2SO4 loãng thu được chất hữu cơ T. Phát biểu nào sau đây sai?
A. Chất T tác dụng với NaOH theo tỉ lệ mol 1 : 1. B. Chất Y có phản ứng tráng bạc.
C. Phân tử chất Z có 2 nguyên tử oxi. D. Chất X tác dụng với NaOH theo tỉ lệ mol 1 : 4.
Câu 31. Cho các phát biểu sau:
(a) Tất cả các peptit đều có phản ứng màu biure.
(b) Muối phenylamoni clorua tan được trong nước.
(c) Ở điều kiện thường, metylamin và đimetylamin là những chất khí.
(d) Trong phân tử peptit mạch hở Gly-Ala-Val có 3 nguyên tử nitơ.
(e) Ở điều kiện thường, amino axit là những chất lỏng.
Số phát biểu đúng là
A. 2. B. 4. C. 5. D. 3.
Câu 32. Một octapeptit có công thức: Pro-Pro-Gly-Arg-Phe-Ser-Phe-Pro. Khi thuỷ phân không hoàn toàn peptit này thu được tối đa mấy loại peptit có aminoaxit đầu N là phenylalanin (Phe)?
A. 6. B. 5. C. 3. D. 4.
Câu 33. Khi nhỏ từ từ đến dư dung dịch HCl vào dung dịch hỗn hợp gồm x mol Ba(OH)2 và y mol Ba[Al(OH)4]2 (hoặc Ba(AlO2)2), kết quả thí nghiệm được biểu diễn trên đồ thị sau:
Giá trị của x và y lần lượt là
A. 0,10 và 0,30. B. 0,10 và 0,15. C. 0,05 và 0,15. D. 0,05 và 0,30.
Câu 34. Hơp chất hữu cơ X có công thức phân tử C2H10N4O6. Cho 18,6 gam X tác dụng với 250 ml dung dịch NaOH 1M cho đến khi phản ứng xảy ra hoàn toàn thì thu được dung dịch Y. Cô cạn Y thu được hơi có chứa một chất hữu cơ duy nhất làm xanh giấy quỳ ẩm và đồng thời thu được a gam chất rắn. Giá trị a là
A. 17 gam. B. 15 gam. C. 19 gam. D. 21 gam.
Câu 35. Trong các phát biểu sau
(1) Các phản ứng nhiệt phân muối amoni đều là phản ứng oxi hóa – khử
(2) NH3 vừa có tính khử vừa có tính bazơ
(3) Dung dịch muối Natri cacbonat làm quỳ tím chuyển màu xanh
(4) Axit, bazơ, muối đều là những chất điện li mạnh
(5) Thành phần chính của quặng photphorit là Ca3(PO4)2
(6) Silic tan được trong cả dung dịch HCl và dung dịch NaOH đặc, nóng
(7) Thành phần của quặng đolomit là CaCO3.MgCO3
Số phát biểu đúng là
A.3 B. 5 C. 6 D. 4
Câu 36. Cho 5 chất: Mg(OH)2, HCl, AgNO3, HNO3, Cl2. Số chất tác dụng được với dung dịch Fe(NO3)2 là
A. 5. B. 2. C. 3. D. 4.
Câu 37. Hỗn hợp X gồm hai este đơn chức. Cho m gam X tác dụng với lượng vừa đủ dung dịch NaOH đun nóng, thu được 17,0 gam một muối và 12,4 gam hỗn hợp Y gồm hai anđehit thuộc cùng dãy đồng đẳng. Tỉ khối hơi của hỗn hợp Y so với H2 là 24,8. Biết các phản ứng đều xảy ra hoàn toàn. Giá trị của m là
A. 25,15. B. 10,80. C. 19,40. D. 12,60.
Câu 38. Cho từ từ 100 ml dung dịch gồm HCl 0,2M và NaHSO4 0,6M vào 300 ml dung dịch gồm NaHCO3 0,1M và K2CO3 0,2M thu được V lít CO2 (đktc) và dung dịch X. Cho 100 ml dung dịch gồm KOH 0,6M và BaCl2 1,5M vào dung dịch X, thu được m gam kết tủa. Giá trị V và m là
A. 1,0752 và 22,254. B. 0,4480 và 25,800. C. 1,0752 và 23,4300. D. 0,4480 và 11,820.
Câu 39: X là este của amino axit, Y là peptit mạch hở. Cho m gam hỗn hợp M gồm X và Y tác dụng vừa đủ với dung dịch chứa 0,7 mol NaOH, đun nóng. Sau khi các phản ứng xảy ra hoàn toàn, thu được 13,8 gam một ancol đơn chức Z và hỗn hợp T chứa muối của glyxin, alanin, valin (trong đó có 0,5 mol muối của glyxin). Đốt cháy hoàn toàn T trong O2, thu được Na2CO3, N2, H2O và 1,45 mol CO2. Cho toàn bộ lượng Z trên tác dụng hết với Na, sinh ra 0,15 mol H2. Phần trăm khối lượng của Y trong M là
A. 58,37%. B. 98,85%. C. 40,10%. D. 49,43%.
Câu 40: Hòa tan hết 31,12 gam hỗn hợp X gồm Mg, Fe (a mol), Fe3O4, FeCO3 vào dung dịch hỗn hợp chứa H2SO4 và KNO3. Sau phản ứng thu được 4,48 lít hỗn hợp khí Y (đktc) gồm (CO2, NO, NO2, H2) có tỉ khối hơi so với H2 là 14,6 và dung dịch Z chỉ chứa các muối trung hòa với tổng khối lượng là m gam (không chứa ion Fe3+). Cho dung dịch BaCl2 dư vào thấy xuất hiện 140,965 gam kết tủa trắng. Mặt khác, cho dung dịch NaOH (dư) vào Z thì thấy có 43,4 gam NaOH phản ứng, đồng thời xuất hiện 42,9 gam kết tủa và có 0,56 lít khí (đktc) thoát ra. Biết các phản ứng xảy ra hoàn toàn. Giá trị của a gần nhất với giá trị nào sau đây?
A. 0,159. B. 0,165. C. 0,152. D. 0,171.
PHẦN TỰ LUẬN ( 3 ĐIỂM )
Câu 1( 0,8 điểm ): Nêu hiện tượng, viết pthh ( ghi rõ điều kiện ) cho các trường hợp sau
-
Cho Toluen vào dd KMnO4 rồi đun nóng
-
Dẫn khí xiclopropan vào dung dịch nước Br2 dư
-
Cho axit fomic vào dung dịch Cu(OH)2 một lúc sau đó đun nóng
-
Cho hỗn hợp rắn gồm ( Fe3O4 và Cu lấy theo tỉ lệ mol 2 : 1 ) vào dung dịch HCl
Câu 2( 0,5 điểm ): Hòa tan 0,775 gam đơn chất X mầu đỏ vào dung dịch HNO3 thu được 2,8 lit khí màu nâu ( đktc ). Và dung dịch chứa hai axit. Xác định X và viết các phương trình hóa học
Câu 3( 1 điểm ). Hỗn hợp khí X gồm hidrosunfua và một ankan A được trộn với nhau theo tỉ lệ thể tích 1 : 4 . Đốt cháy hoàn toàn hỗn hợp X bằng Oxi dư rồi cho toàn bộ sản phẩm cháy hấp thụ hết vào lượng dư dung dịch Ba(OH)2 thu được 17,93 gam kết tủa, cho lượng kết tủa này qua dung dịch chứa ( KmnO4 + HNO3 ) dư thấy còn lại 2,33 gam kết tủa. Viết các phương trình hóa học xảy ra và xác định ankan
Câu 4( 1,2 điểm ). Đốt cháy hoàn toàn 3,4 gam chất hữu cơ A thuần chức,lấy toàn bộ sản phẩm cháy hấp thu hoàn toàn vào dung dịch Ca(OH)2 dư thấy có 16 gam kết tủa trắng đồng thời khối lượng dung dịch giảm 7,16 gam
-
Tìm CTPT của A biết tỉ khối của A với NH3 bằng 10
-
Đun nóng 34 gam A trong 500 ml dung dịch NaOH 1M thấy tạo thành chất hữu cơ B. Phần dung dịch còn lại đem cô cạn thu được 41,6 gam chất rắn trong đó có một muối Natri của axit hữu cơ đơn chức, chất B phản ứng với Cu(OH)2 tạo dung dịch xanh lam. Xác định CTCT của A ( Biết các phản ứng xảy ra hoàn toàn )
———HẾT———
O2 Education gửi các thầy cô link download đề thi
Lần 3 năm 2017-2018 Đ£p £n Đề trắc nghiệm Đề tự luận
Xem thêm
- Tổng hợp đề thi HSG lớp 12 môn hoá học
- Tổng hợp bài tập vô cơ hay và khó có lời giải chi tiết
- Tổng hợp 50+ bài tập chất béo có lời giải chi tiết
- Tổng hợp bài tập hữu cơ hay và khó có lời giải chi tiết
- Tổng hợp đề thi học kì 2 lớp 12 môn hóa học
- Tổng hợp đề thi học kì 2 lớp 11 môn hóa học
- Tổng hợp đề thi học kì 2 lớp 10 môn hoá học
- Tổng hợp các chuyên đề hóa học lớp 10
- Tổng hợp các chuyên đề hóa học lớp 11
- Tổng hợp các chuyên đề hóa học lớp 12
- Tổng hợp đề thi giữa học kì 2 cả ba khối 10 11 12
- Tổng hợp đề thi THPT QG 2021 file word có lời giải chi tiết
- Tổng hợp các phương pháp giải bài tập môn hoá học