Đề thi thử tốt nghiệp THPT 2021 môn hóa file word có lời giải số 2
|
ĐỀ MINH HỌA SỐ 02 |
KỲ THI TRUNG HỌC PHỔ THÔNG QUỐC GIA NĂM 2021 Bài thi: Khoa học tự nhiên; Môn: Hóa Học Thời gian làm bài: 50 phút, không kể thời gian phát đề |
Cho biết nguyên tử khối của các nguyên tố: H=1; O=16; S=32; F=19; Cl=35,5; Br=80; I=127; N=14; P=31; C=12; Si=28; Li=7; Na=23; K=39; Mg=24; Ca=40; Ba=137; Sr=88; Al=27;Fe=56; Cu=64; Pb=207; Ag=108.
Câu 1: Kim loại nào sau đây có màu trắng hơi xám?
A. Au. B. Fe. C. Ag. D. Cu.
Câu 2: Kim loại nào sau đây có số oxi hóa +1 duy nhất trong hợp chất?
A. Al. B. Fe. C. Ca. D. K.
Câu 3: Vào mùa đông, nhiều gia đình sử dụng bếp than đặt trong phòng kín để sưởi ấm gây ngộ độc khí, có thể dẫn tới tử vong. Nguyên nhân gây ngộ độc là do khí nào sau đây?
A. H2. B. O3. C. N2. D. CO.
Câu 4: Trilinolein là chất béo không no, ở trạng thái lỏng. Công thức của trilinolein là
A. (C17H33COO)3C3H5. B. (C17H35COO)3C3H5. C. (C15H31COO)3C3H5. D. (C17H31COO)3C3H5.
Câu 5: Cho dung dịch NaOH vào dung dịch chất X, thu được kết tủa màu nâu đỏ. Chất X là
A. FeCl3. B. MgCl2. C. CuCl2. D. FeCl2.
Câu 6: Số liên kết peptit trong phân tử Gly-Ala-Ala-Gly là
A. 4. B. 1. C. 2. D. 3.
Câu 7: Hợp chất nào sau đây không có tính lưỡng tính?
A. AlCl3. B. NaHCO3. C. Al2O3. D. Al(OH)3.
Câu 8: Chất nào sau đây vừa phản ứng với dung dịch NaOH loãng, vừa phản ứng với dung dịch HCl?
A. CrCl3. B. CrCl2. C. Cr(OH)3. D. Na2CrO4.
Câu 9: Polime có cấu trúc mạng lưới không gian là
A. polietilen. B. poli (vinylclorua). C. cao su lưu hóa. D. amilopectin.
Câu 10: Tiến hành phản ứng khử oxit X thành kim loại bằng khí CO (dư) theo sơ đồ hình vẽ:

Oxit X là
A. Al2O3. B. K2O. C. CuO. D. MgO.
Câu 11: Chất nào sau đây không tan trong nước lạnh
A. glucozơ. B. tinh bột. C. fructozơ. D. saccarozơ.
Câu 12: Máu một số loại bạch tuộc, mực và giáp xác có màu xanh, đó là do trong máu của chúng có chứa nguyên tố X. Nguyên tố X là
A. S. B. Cu. C. P. D. Fe.
Câu 13: Cho 2,52 gam một kim loại tác dụng với dung dịch H2SO4 loãng tạo ra 6,84 gam muối sunfat. Kim loại đó là
A. Mg. B. Fe. C. Ca. D. Al.
Câu 14: Hòa tan m gam hỗn hợp X gồm Al và Na có tỉ lệ mol 1:2 vào nước dư, thu được 4,48 lít khí (đktc). Giá trị của m là
A. 7,3. B. 5,84. C. 6,15. D. 3,65.
Câu 15: Cho các chất sau đây: triolein, Ala-Gly-Ala, vinyl fomat, anbumin. Số chất bị thủy phân trong môi trường kiềm là
A. 4. B. 2. C. 3. D. 1.
Câu 16: Lên men m gam glucozơ thành ancol etylic với hiệu suất 50%, thu được 4,48 lít CO2. Giá trị của m là
A. 36,0. B. 18,0. C. 32,4. D. 16,2.
Câu 17: Cho hỗn hợp hai amino axit đều chứa 1 nhóm amino và 1 nhóm cacboxyl vào 440 ml dung dịch HCl 1M được dung dịch X. Để tác dụng hết với dung dịch X cần 840 ml dung dịch NaOH 1M. Vậy khi tạo thành dung dịch X thì
A. amino axit và HCl cùng hết. B. HCl còn dư.
C. dư amino axit. D. cả amino axit và HCl đều dư.
Câu 18: Hình vẽ sau đây mô tả thí nghiệm điều chế khí Y từ hỗn hợp rắn gồm CaC2 và Al4C3:

Khí Y là
A. C2H4. B. C2H6. C. CH4. D. C2H2.
Câu 19: Phản ứng nào sau đây có phương trình ion rút gọn là H+ + OH– → H2O?
A. NaHCO3 + NaOH → Na2CO3 + H2O. B. Ba(OH)2 + 2HCl → BaCl2 + 2H2O.
C. Ba(OH)2 + H2SO4 → BaSO4 + 2H2O. D. Cu(OH)2 + 2HCl → CuCl2 + 2H2O.
Câu 20: Thủy phân đisaccarit X, thu được 2 monosaccarit Y, Z. Oxi hóa Y hoặc Z bằng dung dịch AgNO3/NH3, thu được chất hữu cơ T. Hai chất X, T lần lượt là:
A. saccarozơ và axit gluconic. B. saccarozơ và amoni gluconat.
C. tinh bột và glucozơ. D. glucozơ và fructozơ.
Câu 21: Trong số các thí nghiệm sau, có mấy thí nghiệm chỉ xảy ra sự ăn mòn hóa học?
(1) Đốt cháy dây sắt trong không khí khô.
(2) Cho hợp kim Fe – Cu vào dung dịch CuSO4.
(3) Đốt dây kim loại Mg nguyên chất trong khí Cl2.
(4) Cho Fe vào dung dịch AgNO3.
A. 2. B. 3. C. 4. D. 1.
Câu 22: Thủy phân este mạch hở X, có công thức phân tử C4H6O2, thu được sản phẩm không có phản ứng tráng bạc. Số công thức cấu tạo phù hợp của X là
A. 5. B. 3. C. 4. D. 1.
Câu 23: Cho các chất sau: CrO3, Fe, Cr(OH)3, Cr. Số chất tan được trong dung dịch NaOH là
A. 1. B. 2. C. 3. D. 4.
Câu 24: Cho các polime sau: polistiren, amilozơ, amilopectin, poli(vinyl clorua), poli(metyl metacrylat), teflon. Số polime có thành phần nguyên tố giống nhau là
A. 5. B. 3. C. 4. D. 2.
Câu 25: Hấp thụ hoàn toàn 1,12 lít CO2 (đktc) vào 150 ml dung dịch KOH 1M, thu được dung dịch X. Cho từ từ dung dịch HCl 2,5M vào X đến khi bắt đầu có khí sinh ra thì hết V ml. Giá trị của V là
A. 80. B. 40. C. 60. D. 100.
Câu 26: Đốt cháy hoàn toàn 1 mol chất béo, thu được lượng CO2 và H2O hơn kém nhau 6 mol. Mặt khác, a mol chất béo trên tác dụng tối đa với 600 ml dung dịch Br2 1M. Giá trị của a là
A. 0,20. B. 0,15. C. 0,30. D. 0,18.
Câu 27: Thực hiện hai thí nghiệm sau:
– Thí nghiệm 1: Cho este X có công thức phân tử C5H8O4 tác dụng hoàn toàn với dung dịch NaOH (dư), thu được hai muối Y, Z (MY < MZ) và ancol T duy nhất
– Thí nghiệm 2: Thủy phân tinh bột thu được cacbonhiđrat X1. Lên men X1 thu được T
Nhận định nào sau đây đúng?
A. Este X được tạo bởi các axit cacboxylic và ancol tương ứng.
B. Z là muối của axit axetic.
C. Axit cacboxylic tạo muối Y và hợp chất T có cùng khối lượng phân tử.
D. Este X không tham gia phản ứng tráng gương.
Câu 28: Cho các phản ứng sau :
(a) H2S + SO2
(b) Cu + dung dịch H2SO4 (loãng)
(c) SiO2 + Mg
(d) Al2O3 + dung dịch NaOH
(e) H2S + FeCl3
(g)
Số phản ứng tạo ra đơn chất là
A. 4. B. 5. C. 6. D. 3.
Câu 29: Cho các phát biểu sau:
(a) Nhôm và hợp kim của nhôm có màu trắng bạc, đẹp nên được dùng cho xây dựng nhà cửa và trang trí nội thất.
(b) Cho dung dịch NaOH dư vào dung dịch Ca(HCO3)2 sau phản ứng thu được kết tủa trắng.
(c) Các kim loại kiềm có thể đẩy được các kim loại yếu hơn ra khỏi muối.
(d) Các kim loại kiềm có màu trắng bạc, có tính ánh kim.
(e) Nhôm nhẹ, dẫn điện tốt nên được dùng làm dây dẫn điện thay cho đồng. Do dẫn điện tốt, ít bị gỉ và không độc nên nhôm được dùng làm dụng cụ nhà bếp.
Số phát biểu đúng là
A. 3. B. 2. C. 5. D. 4.
Câu 30: Hỗn hợp X gồm hiđro và một hiđrocacbon. Nung nóng 14,56 lít hỗn hợp X (đktc) (có Ni xúc tác) đến khi phản ứng hoàn toàn, thu được hỗn hợp Y có khối lượng 10,8 gam. Biết tỉ khối của Y so với metan là 2,7 và Y có khả năng làm mất màu dung dịch brom. Công thức phân tử của hiđrocacbon là
A. C3H6. B. C4H6. C. C3H4. D. C4H8.
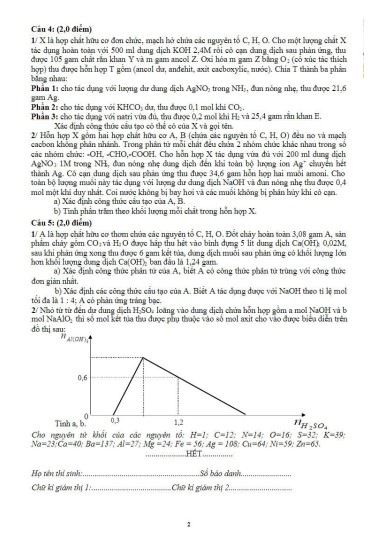
Câu 31: Nhỏ từ từ dung dịch Ba(OH)2 vào ống nghiệm chứa dung dịch H2SO4 và Al2(SO4)3. Đồ thị biểu diễn sự phụ thuộc khối lượng kết tủa theo số mol Ba(OH)2 như sau:

Giá trị gần nhất của a là
A. 150. B. 175. C. 185. D. 210.
Câu 32: Cho các phát biểu sau:
(a) Metyl metacrylat làm mất màu dung dịch brom.
(b) Metyl fomat và glucozơ có cùng công thức đơn giản nhất.
(c) Chỉ dùng quỳ tím có thể phân biệt ba dung dịch: valin, metylamin, axit glutamic.
(d) Hợp chất CH3COONH3CH3 là este của amino axit.
(e) Trong công nghiệp dược phẩm, saccarozơ được dùng để pha chế thuốc.
(g) Tơ nitron dai, bền với nhiệt, giữ nhiệt tốt, thường được dùng để dệt vải và may quần áo ấm.
Số phát biểu đúng là
A. 5. B. 2. C. 3. D. 4.
Câu 33: Điện phân dung dịch X chứa 3a mol Cu(NO3)2 và a mol KCl (với điện cực trơ, màng ngăn xốp) đến khi khối lượng catot tăng 12,8 gam thì dừng điện phân, thu được dung dịch Y. Cho 22,4 gam bột Fe vào Y, sau khi các phản ứng xảy ra hoàn toàn, thu được khí NO (sản phẩm khử duy nhất của N+5) và 16 gam hỗn hợp kim loại. Giả thiết hiệu suất điện phân là 100%. Giá trị của a là
A. 0,096. B. 0,128. C. 0,112. D. 0,080.
Câu 34: X là este 3 chức. Xà phòng hóa hoàn toàn 2,904 gam X bằng dung dịch NaOH, thu được chất hữu cơ Y có khối lượng 1,104 gam và hỗn hợp 3 muối của 1 axit cacboxylic thuộc dãy đồng đẳng của axit axetic và 2 axit cacboxylic thuộc dãy đồng đẳng của axit acrylic. Cho toàn bộ lượng Y tác dụng hết với Na, thu được 0,4032 lít H2 (đktc). Hỏi khi đốt cháy hoàn toàn 2,42 gam X thu được tổng khối lượng H2O và CO2 là bao nhiêu gam?
A. 6,10. B. 5,92. C. 5,04. D. 5,22.
Câu 35: Đốt cháy 10,08 gam Mg trong oxi một thời gian, thu được m gam hỗn hợp rắn X. Hòa tan hết X trong dung dịch gồm HCl 0,9M và H2SO4 0,6M, thu được dung dịch Y chỉ chứa các muối có khối lượng 3,825m gam. Mặt khác, hòa tan hết 1,25m gam X trong dung dịch HNO3 loãng dư, thu được dung dịch Z chứa 82,5 gam muối và hỗn hợp khí T gồm N2 và 0,015 mol khí N2O. Số mol HNO3 phản ứng là
A. 1,23 mol. B. 1,32 mol. C. 1,42 mol. D. 1,28 mol.
Câu 36: Tiến hành thí nghiệm sau:
Bước 1: Rót vào hai ống nghiệm mỗi ống 1 ml etyl axetat, sau đó thêm vào ống thứ nhất 1 ml dung dịch H2SO4 20%, ống thứ hai 1 ml dung dịch NaOH 30%. Bước 2: Lắc đều 2 ống nghiệm, đun cách thủy (trong nồi nước nóng) khoảng 5 – 6 phút ở 65 – 70oC. Phát biểu nào sau đây đúng?
A. Ở cả 2 ống nghiệm chất lỏng vẫn tách thành 2 lớp.
B. Ống nghiệm thứ nhất chất lỏng trở nên đồng nhất, ống thứ 2 chất lỏng tách thành 2 lớp.
C. Ở cả 2 ống nghiệm chất lỏng trở nên đồng nhất.
D. Ống nghiệm thứ nhất vẫn phân thành 2 lớp, ống thứ 2 chất lỏng trở thành đồng nhất.
Câu 37: Hòa tan hoàn toàn hai chất rắn X, Y (có số mol bằng nhau) vào nước thu được dung dịch Z. Tiến hành các thí nghiệm sau:
Thí nghiệm 1: Cho dung dịch KOH dư vào V ml dung dịch Z, thu được m1 gam kết tủa.
Thí nghiệm 2: Cho dung dịch K2CO3 dư vào V ml dung dịch Z, thu được m2 gam kết tủa.
Thí nghiệm 3: Cho dung dịch AgNO3 dư vào V ml dung dịch Z, thu được m3 gam kết tủa.
Biết các phản ứng xảy ra hoàn toàn và m1 < m2 < m3. Hai chất X, Y lần lượt là:
A. NaCl, FeCl2. B. NaNO3, Fe(NO3)2. C. KCl, Ba(HCO3)2. D. Ca(HCO3)2, CaCl2.
Câu 38: Hỗn hợp E gồm axit cacboxylic đơn chức X và hai este Y, Z, đều mạch hở (trong đó, X và Y là đồng phân cấu tạo của nhau). Đốt cháy hoàn toàn m gam E cần vừa đủ 1,2 mol oxi, thu được CO2 và 1,1 mol H2O. Mặt khác, cho 7,72 gam E tác dụng vừa đủ với 130 ml dung dịch KOH 1M, thu được dung dịch hỗn hợp muối và ancol đơn chức. Phần trăm khối lượng của Z trong E là
A. 61,14%. B. 33,33%. C. 44,44%. D. 16,67%.
Câu 39: Chia 47,1 gam hỗn hợp bột X gồm Zn, Fe và Mg thành 3 phần bằng nhau. Cho phần 1 vào 500 ml dung dịch HCl nồng độ a mol/lít, làm khô hỗn hợp sau phản ứng thu được 33,45 gam chất rắn khan. Cho phần 2 tác dụng với 450 ml dung dịch HCl nồng độ 2a mol/lít, làm khô hỗn hợp sau phản ứng thu được 40,55 gam chất rắn khan. Phần 3 tác dụng với lượng dư dung dịch AgNO3 thu được 86,4 gam chất rắn. Biết các phản ứng đều xảy ra hoàn toàn, các quá trình làm khô hỗn hợp không xảy ra phản ứng hóa học. Giá trị của a và phần trăm số mol của Mg có trong hỗn hợp X lần lượt là:
A. 0,5 và 22,93%. B. 1,0 và 42,86%. C. 0,5 và 42,96%. D. 1,0 và 22,93%.
Câu 40: 18,5 gam chất hữu cơ A (có công thức phân tử C3H11N3O6) tác dụng vừa đủ với 300 ml dung dịch NaOH 1M tạo thành nước, 1 chất hữu cơ đa chức bậc I và m gam hỗn hợp muối vô cơ. Giá trị gần đúng nhất của m là
A. 19,05. B. 25,45. C. 21,15. D. 8,45.
———– HẾT ———-
O2 Education gửi các thầy cô và các em link download đề thi
Xem thêm
- Tổng hợp đề thi THPT QG 2021 file word có lời giải chi tiết
- Tổng hợp bài tập vô cơ hay và khó có lời giải chi tiết
- Tổng hợp 50+ bài tập chất béo có lời giải chi tiết
- Tổng hợp bài tập hữu cơ hay và khó có lời giải chi tiết
- Tổng hợp đề thi học kì 2 lớp 12 môn hóa học
- Tổng hợp đề thi học kì 2 lớp 11 môn hóa học
- Tổng hợp đề thi học kì 2 lớp 10 môn hoá học
- Tổng hợp các chuyên đề hóa học lớp 10
- Tổng hợp các chuyên đề hóa học lớp 11
- Tổng hợp các chuyên đề hóa học lớp 12
- Tổng hợp đề thi giữa học kì 2 cả ba khối 10 11 12
- Tổng hợp các phương pháp giải bài tập môn hoá học
- Tổng hợp đề thi HSG lớp 12 môn hoá học