Đề thi giữa học kì 1 lớp 12 môn hoá đề số 17
|
TRƯỜNG THPT NĂM HỌC 2021- 2022 ĐỀ CHÍNH THỨC |
ĐỀ KIỂM TRA CHẤT LƯỢNG GIỮA HỌC KÌ I MÔN: HÓA HỌC – LỚP 12 Thời gian làm bài 40 phút ( không kể thời gian giao đề )
Đề thi gồm 02 trang |
Họ và tên thí sinh:…….………………………Số báo danh:……………………
Học sinh không được dùng bảng tuần hoàn các nguyên tố hoá học
Cho : C=12 , O=16 , Ag=108 , H=1 , N=14 , Cl=35,5 , Na=23
Câu 26: Metyl axetat là tên gọi của hợp chất no sau đây ?
A. HCOOC2H5 B. CH2=CH-COOCH3 C. CH3COOCH3 D. CH3COOCH=CH2
Câu 27:.Hợp chất hữu cơ có công thức cấu tạo thu gọn HCOOC6H5 có tên gọi là ?
A Phenyl fomiat B. Phenyl fomat C Phenyl fomic D. Phenyl fomitat
Câu 28: Công thức tổng quát của este no, đơn chức, mạch hở có dạng:
A. CnH2n+2O2 (n ≥ 2). B. CnH2nO2 (n ≥ 3). C. CnH2nO2 (n ≥ 2). D. CnH2n-2O2 (n ≥ 2).
Câu 29: Cacbohiđrat nào sau đây thuộc loại monosaccarit là:
A. Tinh bột. B. Xenlulozơ. C. Saccarozơ. D. Glucozơ.
Câu 30: Dung dịch saccarozơ phản ứng với chất nào sau đây ?
A. AgNO3/NH3,t0. B. Cu(OH)2/OH–. C. H2/Ni,t0. D. nước Br2
Câu 31: Hai chất đồng phân của nhau là:
A. Fructozơ và glucozơ. B. Xenlulozơ.và glucozơ.
C. Fructozơ và xenlulozơ. D. Saccarozơ và glucozơ
Câu 32: Chất có tính bazơ là
A. C2H5NH2. B. CH3COOH. C. C6H5COOH D. C6H5OH.
Câu 33: Số đồng phân amin có công thức phân tử C3H9N là
A. 2. B. 3. C. 5. D. 4.
Câu 34: Trong các chất sau, chất nào là amin bậc 2?
A. H2N-[CH2]6–NH2 B. CH3–CH(CH3)–NH2 C. CH3–NH–CH3 D. C6H5NH2
Câu 35: Amino axit là hợp chất hữu cơ trong phân tử
A. chứa nhóm cacboxyl và nhóm amino. B. chỉ chứa nhóm amino.
C. chỉ chứa nhóm cacboxyl. D. chỉ chứa nitơ hoặc cacbon.
Câu 36: Kết tủa xuất hiện khi nhỏ dung dịch brom vào
A. ancol etylic. B. benzen. C. anilin. D. axit axetic.
Câu 37: Trong các tên gọi dưới đây, tên nào không phù hợp với chất CH3–CH(NH2)–COOH ?
A. Axit 2-aminopropanoic. B. Axit-aminopropionic. C. Anilin. D. Alanin
Câu 38 : Thủy phân hoàn toàn 8,8g este đơn chức, mạch hở X với 100ml dung dịch NaOH 1M vừa đủ thu được 8,2 g muối hữu cơ Y và một ancol Z. Tên gọi của X là:
A. etyl fomat B. etyl propionat C. propyl axetat D. etyl axetat
Câu 39: Đốt cháy hoàn toàn 0,15 mol este thu được 19,8g CO2 và 0,45 mol H2O. Công thức phân tử este là
A. C2H4O2 B. C3H6O2 C. C4H8O2 D. C5H10O2
Câu 40: Cho m gam glucozơ tác dụng với dd AgNO3 /NH3 dư có đun nóng nhẹ. Sau phản ứng thu được 2,16 gam Ag. Giá trị của m là:
A. 64,8 g. B. 1,8 g. C. 54,0 g. D. 92,5 g.
Câu 41: Cho 4,5 gam etylamin (C2H5NH2 ) tác dụng vừa đủ với axit HCl. Khối lượng muối thu được là
A. 7,65 gam. B. 8,15 gam. C. 8,10 gam. D. 0,85 gam.
Câu 42: Tinh bột, xenlulozơ, saccarozơ đều có khả năng tham gia phản ứng
A. hoà tan Cu(OH)2. B. trùng ngưng. C. tráng gương. D. thủy phân
Trang : 1/2 – Mã đề : 123
Câu 43 : X là một α – amino axit no chỉ chứa 1 nhóm –NH2 và 1 nhóm –COOH. Cho X tác dụng vừa đủ với 100ml dd HCl 1M, thu được 12,55 gam muối. CTCT của X là:
A. H2N-CH2-COOH. B. CH3-CH(NH2)-COOH.
C. C2H5-CH(NH2)-COOH. D. H2N- CH2-CH2-COOH.
Câu 44: Khi thủy phân saccarozơ thì thu được
A. ancol etylic. B. Glucozơ và fructozơ. C. glucozơ. D. fructozơ.
Câu 45: Hợp chất X có CTPT C4H8O2. Khi thủy phân X trong dd NaOH thu được muối CHO2Na. CTCT của X là:
A. HCOOC3H7. B. C2H5COOCH3. C. CH3COOC2H5. D. C3H7COOH.
Câu 46: Cho sơ đồ phản ứng: Thuốc súng không khói ← X → Y → sobitol. Các hợp chất hữu cơ X, Y lần lượt là
A. tinh bột, glucozơ B. xenlulozơ, glucozơ
C. xenlulozơ, fructozơ D. saccarozơ, glucozơ
Câu 47: Cho các phát biểu sau:
(1) Glucozo được gọi là đường nho do có nhiều trong quả nho chín.
(2) Chất béo là dieste của glixerol với axit béo.
( 3) Hàm lượng glucozơ không đổi trong máu người là khoảng 0,1%.
(4) Ở nhiệt độ thường, triolein ở trạng thái rắn.
(5) Sau khi mổ cá, có thể dùng giấm ăn để giảm mùi tanh
(6) Tinh bột là một trong những lương thực cơ bản của con người.
Số phát biểu sai là A. 3. B. 1. C. 2. D. 4.
Câu 48 : Cho các kết luận về các thí nghiệm sau:
Thí nghiệm 1: Cho Cu(OH)2 vào dung dịch chứa glucozo thấy Cu(OH)2 tan tạo dung dịch màu tím.
Thí nghiệm 2: Cho dung dịch Br2 vào dung dịch anilin có kết tủa màu vàng .
Thí nghiệm 3: Cho glucozơ vào ống nghiệm chứa dung dịch chứa AgNO3/NH3 đun nóng thấy có lớp kim loại bám trên thành ống nghiệm.
Thí nghiệm 4: Đun nóng một lượng triolein với NaOH dư sau đó để nguội cho thêm dung dịch CuSO4 vào thấy dung dịch chuyển sang màu đỏ.
Thí nghiệm 5: Cho Cu(OH)2 vào dung dịch saccarozơ thấy dung dịch xuất hiện màu xanh lam
Thí nghiệm 6 : Nhỏ vài giọt anilin vào nước ta thấy anilin tan hoàn toàn
Số kết luận đúng là
A. 3 B. 4 C. 5 D. 2
Câu 49 : Thủy phân hoàn toàn a mol triglixerit X trong dung dịch NaOH vừa đủ, thu được glixerol và m gam hỗn hợp muối. Đốt cháy hoàn toàn a mol X cần vừa đủ 7,75 mol O2 và thu được 5,5 mol CO2. Mặt khác, a mol X tác dụng tối đa với 0,2 mol Br2 trong dung dịch. Giá trị của m là
A. 82,4. B. 97,6. C. 80,6. D . 88,6
Câu 50 : X là este của α-amino axit với ancol Y có công thức phân tử là C4H9O2N. Đun nóng 5,15 gam X với 200ml dung dịch NaOH 1M. Sau phản ứng hoàn toàn cô cạn dung dịch sau phản ứng thu được m gam chất rắn khan và ancol Y. Oxi hóa hoàn toàn Y thu được anđehit Y1. Cho Y1 tác dụng với dung dich AgNO3/NH3 dư thu được 21,6 gam Ag. Vậy giá trị của m là:
A. 15,1 gam B. 11,55 gam C. 12,45 gam D. 10,68 gam
Trang : 2/2 – Mã đề : 123
|
TRƯỜNG THPT NĂM HỌC 2021- 2022 ĐỀ CHÍNH THỨC |
ĐỀ KIỂM TRA CHẤT LƯỢNG GIỮA HỌC KÌ I MÔN: HÓA HỌC – LỚP 12 Thời gian làm bài 40 phút ( không kể thời gian giao đề )
Đề thi gồm 02 trang |
Họ và tên thí sinh:…….………………………Số báo danh:……………………
Học sinh không được dùng bảng tuần hoàn các nguyên tố hoá học
Cho : C=12 , O=16 , Ag=108 , H=1 , N=14 , Cl=35,5 , Na=23
Câu 26: Cacbohiđrat nào sau đây thuộc loại monosaccarit là:
A. Tinh bột. B. Xenlulozơ. C. Saccarozơ. D. Glucozơ.
Câu 27: Dung dịch saccarozơ phản ứng với chất nào sau đây ?
A. AgNO3/NH3,t0. B. Cu(OH)2/OH–. C. H2/Ni,t0. D. nước Br2
Câu 28: Hai chất đồng phân của nhau là:
A. Fructozơ và glucozơ. B. Xenlulozơ.và glucozơ.
C. Fructozơ và xenlulozơ. D. Saccarozơ và glucozơ
Câu 29: Chất có tính bazơ là
A. C2H5NH2. B. CH3COOH. C. C6H5COOH D. C6H5OH.
Câu 30: Metyl axetat là tên gọi của hợp chất no sau đây ?
A. HCOOC2H5 B. CH2=CH-COOCH3 C. CH3COOCH3 D. CH3COOCH=CH2
Câu 31:.Hợp chất hữu cơ có công thức cấu tạo thu gọn HCOOC6H5 có tên gọi là ?
A Phenyl fomiat B. Phenyl fomat C Phenyl fomic D. Phenyl fomitat
Câu 32: Công thức tổng quát của este no, đơn chức, mạch hở có dạng:
A. CnH2n+2O2 (n ≥ 2). B. CnH2nO2 (n ≥ 3). C. CnH2nO2 (n ≥ 2). D. CnH2n-2O2 (n ≥ 2).
Câu 33: Số đồng phân amin có công thức phân tử C3H9N là
A. 2. B. 3. C. 5. D. 4.
Câu 34: Trong các chất sau, chất nào là amin bậc 2?
A. H2N-[CH2]6–NH2 B. CH3–CH(CH3)–NH2 C. CH3–NH–CH3 D. C6H5NH2
Câu 35: Cho m gam glucozơ tác dụng với dd AgNO3 /NH3 dư có đun nóng nhẹ. Sau phản ứng thu được 2,16 gam Ag. Giá trị của m là:
A. 64,8 g. B. 1,8 g. C. 54,0 g. D. 92,5 g.
Câu 36: Cho 4,5 gam etylamin (C2H5NH2 ) tác dụng vừa đủ với axit HCl. Khối lượng muối thu được là
A. 7,65 gam. B. 8,15 gam. C. 8,10 gam. D. 0,85 gam.
Câu 37: Tinh bột, xenlulozơ, saccarozơ đều có khả năng tham gia phản ứng
A. hoà tan Cu(OH)2. B. trùng ngưng. C. tráng gương. D. thủy phân
Câu 38: Amino axit là hợp chất hữu cơ trong phân tử
A. chứa nhóm cacboxyl và nhóm amino. B. chỉ chứa nhóm amino.
C. chỉ chứa nhóm cacboxyl. D. chỉ chứa nitơ hoặc cacbon.
Câu 39: Kết tủa xuất hiện khi nhỏ dung dịch brom vào
A. ancol etylic. B. benzen. C. anilin. D. axit axetic.
Câu 40: Trong các tên gọi dưới đây, tên nào không phù hợp với chất CH3–CH(NH2)–COOH ?
A. Axit 2-aminopropanoic. B. Axit-aminopropionic. C. Anilin. D. Alanin
Câu 41 : Thủy phân hoàn toàn 8,8g este đơn chức, mạch hở X với 100ml dung dịch NaOH 1M vừa đủ thu được 8,2 g muối hữu cơ Y và một ancol Z. Tên gọi của X là:
A. etyl fomat B. etyl propionat C. propyl axetat D. etyl axetat
Câu 42: Đốt cháy hoàn toàn 0,15 mol este thu được 19,8g CO2 và 0,45 mol H2O. Công thức phân tử este là
A. C2H4O2 B. C3H6O2 C. C4H8O2 D. C5H10O2
Trang : 1/2 – Mã đề : 234
Câu 43 : X là một α – amino axit no chỉ chứa 1 nhóm –NH2 và 1 nhóm –COOH. Cho X tác dụng vừa đủ với 100ml dd HCl 1M, thu được 12,55 gam muối. CTCT của X là:
A. H2N-CH2-COOH. B. CH3-CH(NH2)-COOH.
C. C2H5-CH(NH2)-COOH. D. H2N- CH2-CH2-COOH.
Câu 44: Khi thủy phân saccarozơ thì thu được
A. ancol etylic. B. Glucozơ và fructozơ. C. glucozơ. D. fructozơ.
Câu 45: Hợp chất X có CTPT C4H8O2. Khi thủy phân X trong dd NaOH thu được muối CHO2Na. CTCT của X là:
A. HCOOC3H7. B. C2H5COOCH3. C. CH3COOC2H5. D. C3H7COOH.
Câu 46: Cho sơ đồ phản ứng: Thuốc súng không khói ← X → Y → sobitol. Các hợp chất hữu cơ X, Y lần lượt là
A. tinh bột, glucozơ B. xenlulozơ, glucozơ
C. xenlulozơ, fructozơ D. saccarozơ, glucozơ
Câu 47: Cho các phát biểu sau:
(1) Glucozo được gọi là đường nho do có nhiều trong quả nho chín.
(2) Chất béo là dieste của glixerol với axit béo.
( 3) Hàm lượng glucozơ không đổi trong máu người là khoảng 0,1%.
(4) Ở nhiệt độ thường, triolein ở trạng thái rắn.
(5) Sau khi mổ cá, có thể dùng giấm ăn để giảm mùi tanh
(6) Tinh bột là một trong những lương thực cơ bản của con người.
Số phát biểu sai là A. 3. B. 1. C. 2. D. 4.
Câu 48 : Thủy phân hoàn toàn a mol triglixerit X trong dung dịch NaOH vừa đủ, thu được glixerol và m gam hỗn hợp muối. Đốt cháy hoàn toàn a mol X cần vừa đủ 7,75 mol O2 và thu được 5,5 mol CO2. Mặt khác, a mol X tác dụng tối đa với 0,2 mol Br2 trong dung dịch. Giá trị của m là
A. 82,4. B. 97,6. C. 80,6. D . 88,6
Câu 49 : X là este của α-amino axit với ancol Y có công thức phân tử là C4H9O2N. Đun nóng 5,15 gam X với 200ml dung dịch NaOH 1M. Sau phản ứng hoàn toàn cô cạn dung dịch sau phản ứng thu được m gam chất rắn khan và ancol Y. Oxi hóa hoàn toàn Y thu được anđehit Y1. Cho Y1 tác dụng với dung dich AgNO3/NH3 dư thu được 21,6 gam Ag. Vậy giá trị của m là:
A. 15,1 gam B. 11,55 gam C. 12,45 gam D. 10,68 gam
Câu 50 : Cho các kết luận về các thí nghiệm sau:
Thí nghiệm 1: Cho Cu(OH)2 vào dung dịch chứa glucozo thấy Cu(OH)2 tan tạo dung dịch màu tím.
Thí nghiệm 2: Cho dung dịch Br2 vào dung dịch anilin có kết tủa màu vàng .
Thí nghiệm 3: Cho glucozơ vào ống nghiệm chứa dung dịch chứa AgNO3/NH3 đun nóng thấy có lớp kim loại bám trên thành ống nghiệm.
Thí nghiệm 4: Đun nóng một lượng triolein với NaOH dư sau đó để nguội cho thêm dung dịch CuSO4 vào thấy dung dịch chuyển sang màu đỏ.
Thí nghiệm 5: Cho Cu(OH)2 vào dung dịch saccarozơ thấy dung dịch xuất hiện màu xanh lam
Thí nghiệm 6 : Nhỏ vài giọt anilin vào nước ta thấy anilin tan hoàn toàn
Số kết luận đúng là
A. 3 B. 4 C. 5 D. 2
Trang : 2/2 – Mã đề : 234
|
TRƯỜNG THPT NĂM HỌC 2021- 2022 ĐỀ CHÍNH THỨC |
ĐỀ KIỂM TRA CHẤT LƯỢNG GIỮA HỌC KÌ I MÔN: HÓA HỌC – LỚP 12 Thời gian làm bài 40 phút ( không kể thời gian giao đề )
Đề thi gồm 02 trang |
Họ và tên thí sinh:…….………………………Số báo danh:……………………
Học sinh không được dùng bảng tuần hoàn các nguyên tố hoá học
Cho : C=12 , O=16 , Ag=108 , H=1 , N=14 , Cl=35,5 , Na=23
Câu 26: Công thức tổng quát của este no, đơn chức, mạch hở có dạng:
A. CnH2n+2O2 (n ≥ 2). B. CnH2nO2 (n ≥ 3). C. CnH2nO2 (n ≥ 2). D. CnH2n-2O2 (n ≥ 2).
Câu 27: Cacbohiđrat nào sau đây thuộc loại monosaccarit là:
A. Tinh bột. B. Xenlulozơ. C. Saccarozơ. D. Glucozơ.
Câu 28: Dung dịch saccarozơ phản ứng với chất nào sau đây ?
A. AgNO3/NH3,t0. B. Cu(OH)2/OH–. C. H2/Ni,t0. D. nước Br2
Câu 29: Metyl axetat là tên gọi của hợp chất no sau đây ?
A. HCOOC2H5 B. CH2=CH-COOCH3 C. CH3COOCH3 D. CH3COOCH=CH2
Câu 30:.Hợp chất hữu cơ có công thức cấu tạo thu gọn HCOOC6H5 có tên gọi là ?
A Phenyl fomiat B. Phenyl fomat C Phenyl fomic D. Phenyl fomitat
Câu 31: Hai chất đồng phân của nhau là:
A. Fructozơ và glucozơ. B. Xenlulozơ.và glucozơ.
C. Fructozơ và xenlulozơ. D. Saccarozơ và glucozơ
Câu 32: Trong các chất sau, chất nào là amin bậc 2?
A. H2N-[CH2]6–NH2 B. CH3–CH(CH3)–NH2 C. CH3–NH–CH3 D. C6H5NH2
Câu 33: Amino axit là hợp chất hữu cơ trong phân tử
A. chứa nhóm cacboxyl và nhóm amino. B. chỉ chứa nhóm amino.
C. chỉ chứa nhóm cacboxyl. D. chỉ chứa nitơ hoặc cacbon.
Câu 34: Chất có tính bazơ là
A. C2H5NH2. B. CH3COOH. C. C6H5COOH D. C6H5OH.
Câu 35: Số đồng phân amin có công thức phân tử C3H9N là
A. 2. B. 3. C. 5. D. 4.
Câu 36: Kết tủa xuất hiện khi nhỏ dung dịch brom vào
A. ancol etylic. B. benzen. C. anilin. D. axit axetic.
Câu 37: Trong các tên gọi dưới đây, tên nào không phù hợp với chất CH3–CH(NH2)–COOH ?
A. Axit 2-aminopropanoic. B. Axit-aminopropionic. C. Anilin. D. Alanin
Câu 38 : Thủy phân hoàn toàn 8,8g este đơn chức, mạch hở X với 100ml dung dịch NaOH 1M vừa đủ thu được 8,2 g muối hữu cơ Y và một ancol Z. Tên gọi của X là:
A. etyl fomat B. etyl propionat C. propyl axetat D. etyl axetat
Câu 39: Cho 4,5 gam etylamin (C2H5NH2 ) tác dụng vừa đủ với axit HCl. Khối lượng muối thu được là
A. 7,65 gam. B. 8,15 gam. C. 8,10 gam. D. 0,85 gam.
Câu 40: Tinh bột, xenlulozơ, saccarozơ đều có khả năng tham gia phản ứng
A. hoà tan Cu(OH)2. B. trùng ngưng. C. tráng gương. D. thủy phân
Câu 41: Đốt cháy hoàn toàn 0,15 mol este thu được 19,8g CO2 và 0,45 mol H2O. Công thức phân tử este là
A. C2H4O2 B. C3H6O2 C. C4H8O2 D. C5H10O2
Câu 42: Cho m gam glucozơ tác dụng với dd AgNO3 /NH3 dư có đun nóng nhẹ. Sau phản ứng thu được 2,16 gam Ag. Giá trị của m là:
A. 64,8 g. B. 1,8 g. C. 54,0 g. D. 92,5 g.
Trang : 1/2 – Mã đề : 345
Câu 43: Hợp chất X có CTPT C4H8O2. Khi thủy phân X trong dd NaOH thu được muối CHO2Na. CTCT của X là:
A. HCOOC3H7. B. C2H5COOCH3. C. CH3COOC2H5. D. C3H7COOH.
Câu 44: Cho sơ đồ phản ứng: Thuốc súng không khói ← X → Y → sobitol. Các hợp chất hữu cơ X, Y lần lượt là
A. tinh bột, glucozơ B. xenlulozơ, glucozơ
C. xenlulozơ, fructozơ D. saccarozơ, glucozơ
Câu 45 : X là một α – amino axit no chỉ chứa 1 nhóm –NH2 và 1 nhóm –COOH. Cho X tác dụng vừa đủ với 100ml dd HCl 1M, thu được 12,55 gam muối. CTCT của X là:
A. H2N-CH2-COOH. B. CH3-CH(NH2)-COOH.
C. C2H5-CH(NH2)-COOH. D. H2N- CH2-CH2-COOH.
Câu 46: Khi thủy phân saccarozơ thì thu được
A. ancol etylic. B. Glucozơ và fructozơ. C. glucozơ. D. fructozơ.
Câu 47: Cho các phát biểu sau:
(1) Glucozo được gọi là đường nho do có nhiều trong quả nho chín.
(2) Chất béo là dieste của glixerol với axit béo.
( 3) Hàm lượng glucozơ không đổi trong máu người là khoảng 0,1%.
(4) Ở nhiệt độ thường, triolein ở trạng thái rắn.
(5) Sau khi mổ cá, có thể dùng giấm ăn để giảm mùi tanh
(6) Tinh bột là một trong những lương thực cơ bản của con người.
Số phát biểu sai là A. 3. B. 1. C. 2. D. 4.
Câu 48 : Cho các kết luận về các thí nghiệm sau:
Thí nghiệm 1: Cho Cu(OH)2 vào dung dịch chứa glucozo thấy Cu(OH)2 tan tạo dung dịch màu tím.
Thí nghiệm 2: Cho dung dịch Br2 vào dung dịch anilin có kết tủa màu vàng .
Thí nghiệm 3: Cho glucozơ vào ống nghiệm chứa dung dịch chứa AgNO3/NH3 đun nóng thấy có lớp kim loại bám trên thành ống nghiệm.
Thí nghiệm 4: Đun nóng một lượng triolein với NaOH dư sau đó để nguội cho thêm dung dịch CuSO4 vào thấy dung dịch chuyển sang màu đỏ.
Thí nghiệm 5: Cho Cu(OH)2 vào dung dịch saccarozơ thấy dung dịch xuất hiện màu xanh lam
Thí nghiệm 6 : Nhỏ vài giọt anilin vào nước ta thấy anilin tan hoàn toàn
Số kết luận đúng là
A. 3 B. 4 C. 5 D. 2
Câu 49: X là este của α-amino axit với ancol Y có công thức phân tử là C4H9O2N. Đun nóng 5,15 gam X với 200ml dung dịch NaOH 1M. Sau phản ứng hoàn toàn cô cạn dung dịch sau phản ứng thu được m gam chất rắn khan và ancol Y. Oxi hóa hoàn toàn Y thu được anđehit Y1. Cho Y1 tác dụng với dung dich AgNO3/NH3 dư thu được 21,6 gam Ag. Vậy giá trị của m là:
A. 15,1 gam B. 11,55 gam C. 12,45 gam D. 10,68 gam
Câu 50 : Thủy phân hoàn toàn a mol triglixerit X trong dung dịch NaOH vừa đủ, thu được glixerol và m gam hỗn hợp muối. Đốt cháy hoàn toàn a mol X cần vừa đủ 7,75 mol O2 và thu được 5,5 mol CO2. Mặt khác, a mol X tác dụng tối đa với 0,2 mol Br2 trong dung dịch. Giá trị của m là
A. 82,4. B. 97,6. C. 80,6. D . 88,6
Trang : 2/2 – Mã đề : 345
|
TRƯỜNG THPT NĂM HỌC 2021- 2022 ĐỀ CHÍNH THỨC |
ĐỀ KIỂM TRA CHẤT LƯỢNG GIỮA HỌC KÌ I MÔN: HÓA HỌC – LỚP 12 Thời gian làm bài 40 phút ( không kể thời gian giao đề )
Đề thi gồm 02 trang |
Họ và tên thí sinh:…….………………………Số báo danh:……………………
Học sinh không được dùng bảng tuần hoàn các nguyên tố hoá học
Cho : C=12 , O=16 , Ag=108 , H=1 , N=14 , Cl=35,5 , Na=23
Câu 26: Chất có tính bazơ là
A. C2H5NH2. B. CH3COOH. C. C6H5COOH D. C6H5OH.
Câu 27: Metyl axetat là tên gọi của hợp chất no sau đây ?
A. HCOOC2H5 B. CH2=CH-COOCH3 C. CH3COOCH3 D. CH3COOCH=CH2
Câu 28: Công thức tổng quát của este no, đơn chức, mạch hở có dạng:
A. CnH2n+2O2 (n ≥ 2). B. CnH2nO2 (n ≥ 3). C. CnH2nO2 (n ≥ 2). D. CnH2n-2O2 (n ≥ 2).
Câu 29: Hai chất đồng phân của nhau là:
A. Fructozơ và glucozơ. B. Xenlulozơ.và glucozơ.
C. Fructozơ và xenlulozơ. D. Saccarozơ và glucozơ
Câu 30: Số đồng phân amin có công thức phân tử C3H9N là
A. 2. B. 3. C. 5. D. 4.
Câu 31: Trong các chất sau, chất nào là amin bậc 2?
A. H2N-[CH2]6–NH2 B. CH3–CH(CH3)–NH2 C. CH3–NH–CH3 D. C6H5NH2
Câu 32: Cho m gam glucozơ tác dụng với dd AgNO3 /NH3 dư có đun nóng nhẹ. Sau phản ứng thu được 2,16 gam Ag. Giá trị của m là:
A. 64,8 g. B. 1,8 g. C. 54,0 g. D. 92,5 g.
Câu 33: Cho 4,5 gam etylamin (C2H5NH2 ) tác dụng vừa đủ với axit HCl. Khối lượng muối thu được là
A. 7,65 gam. B. 8,15 gam. C. 8,10 gam. D. 0,85 gam.
Câu 34: Tinh bột, xenlulozơ, saccarozơ đều có khả năng tham gia phản ứng
A. hoà tan Cu(OH)2. B. trùng ngưng. C. tráng gương. D. thủy phân
Câu 35: Cacbohiđrat nào sau đây thuộc loại monosaccarit là:
A. Tinh bột. B. Xenlulozơ. C. Saccarozơ. D. Glucozơ.
Câu 36: Dung dịch saccarozơ phản ứng với chất nào sau đây ?
A. AgNO3/NH3,t0. B. Cu(OH)2/OH–. C. H2/Ni,t0. D. nước Br2
Câu 37: Amino axit là hợp chất hữu cơ trong phân tử
A. chứa nhóm cacboxyl và nhóm amino. B. chỉ chứa nhóm amino.
C. chỉ chứa nhóm cacboxyl. D. chỉ chứa nitơ hoặc cacbon.
Câu 38: Kết tủa xuất hiện khi nhỏ dung dịch brom vào
A. ancol etylic. B. benzen. C. anilin. D. axit axetic.
Câu 39: Trong các tên gọi dưới đây, tên nào không phù hợp với chất CH3–CH(NH2)–COOH ?
A. Axit 2-aminopropanoic. B. Axit-aminopropionic. C. Anilin. D. Alanin
Câu 40:.Hợp chất hữu cơ có công thức cấu tạo thu gọn HCOOC6H5 có tên gọi là ?
A Phenyl fomiat B. Phenyl fomat C Phenyl fomic D. Phenyl fomitat
Câu 41 : Thủy phân hoàn toàn 8,8g este đơn chức, mạch hở X với 100ml dung dịch NaOH 1M vừa đủ thu được 8,2 g muối hữu cơ Y và một ancol Z. Tên gọi của X là:
A. etyl fomat B. etyl propionat C. propyl axetat D. etyl axetat
Câu 42: Đốt cháy hoàn toàn 0,15 mol este thu được 19,8g CO2 và 0,45 mol H2O. Công thức phân tử este là
A. C2H4O2 B. C3H6O2 C. C4H8O2 D. C5H10O2
Trang : 1/2 – Mã đề : 456
Câu 43: Cho sơ đồ phản ứng: Thuốc súng không khói ← X → Y → sobitol. Các hợp chất hữu cơ X, Y lần lượt là
A. tinh bột, glucozơ B. xenlulozơ, glucozơ
C. xenlulozơ, fructozơ D. saccarozơ, glucozơ
Câu 44 : X là một α – amino axit no chỉ chứa 1 nhóm –NH2 và 1 nhóm –COOH. Cho X tác dụng vừa đủ với 100ml dd HCl 1M, thu được 12,55 gam muối. CTCT của X là:
A. H2N-CH2-COOH. B. CH3-CH(NH2)-COOH.
C. C2H5-CH(NH2)-COOH. D. H2N- CH2-CH2-COOH.
Câu 45: Khi thủy phân saccarozơ thì thu được
A. ancol etylic. B. Glucozơ và fructozơ. C. glucozơ. D. fructozơ.
Câu 46: Hợp chất X có CTPT C4H8O2. Khi thủy phân X trong dd NaOH thu được muối CHO2Na. CTCT của X là:
A. HCOOC3H7. B. C2H5COOCH3. C. CH3COOC2H5. D. C3H7COOH.
Câu 47 : Thủy phân hoàn toàn a mol triglixerit X trong dung dịch NaOH vừa đủ, thu được glixerol và m gam hỗn hợp muối. Đốt cháy hoàn toàn a mol X cần vừa đủ 7,75 mol O2 và thu được 5,5 mol CO2. Mặt khác, a mol X tác dụng tối đa với 0,2 mol Br2 trong dung dịch. Giá trị của m là
A. 82,4. B. 97,6. C. 80,6. D . 88,6
Câu 48 : X là este của α-amino axit với ancol Y có công thức phân tử là C4H9O2N. Đun nóng 5,15 gam X với 200ml dung dịch NaOH 1M. Sau phản ứng hoàn toàn cô cạn dung dịch sau phản ứng thu được m gam chất rắn khan và ancol Y. Oxi hóa hoàn toàn Y thu được anđehit Y1. Cho Y1 tác dụng với dung dich AgNO3/NH3 dư thu được 21,6 gam Ag. Vậy giá trị của m là:
A. 15,1 gam B. 11,55 gam C. 12,45 gam D. 10,68 gam
Câu 49: Cho các phát biểu sau:
(1) Glucozo được gọi là đường nho do có nhiều trong quả nho chín.
(2) Chất béo là dieste của glixerol với axit béo.
( 3) Hàm lượng glucozơ không đổi trong máu người là khoảng 0,1%.
(4) Ở nhiệt độ thường, triolein ở trạng thái rắn.
(5) Sau khi mổ cá, có thể dùng giấm ăn để giảm mùi tanh
(6) Tinh bột là một trong những lương thực cơ bản của con người.
Số phát biểu sai là A. 3. B. 1. C. 2. D. 4.
Câu 50 : Cho các kết luận về các thí nghiệm sau:
Thí nghiệm 1: Cho Cu(OH)2 vào dung dịch chứa glucozo thấy Cu(OH)2 tan tạo dung dịch màu tím.
Thí nghiệm 2: Cho dung dịch Br2 vào dung dịch anilin có kết tủa màu vàng .
Thí nghiệm 3: Cho glucozơ vào ống nghiệm chứa dung dịch chứa AgNO3/NH3 đun nóng thấy có lớp kim loại bám trên thành ống nghiệm.
Thí nghiệm 4: Đun nóng một lượng triolein với NaOH dư sau đó để nguội cho thêm dung dịch CuSO4 vào thấy dung dịch chuyển sang màu đỏ.
Thí nghiệm 5: Cho Cu(OH)2 vào dung dịch saccarozơ thấy dung dịch xuất hiện màu xanh lam
Thí nghiệm 6 : Nhỏ vài giọt anilin vào nước ta thấy anilin tan hoàn toàn
Số kết luận đúng là
A. 3 B. 4 C. 5 D. 2
Trang : 2/2 – Mã đề : 456
|
TRƯỜNG THPT NĂM HỌC 2021- 2022 ĐỀ CHÍNH THỨC |
ĐỀ KIỂM TRA CHẤT LƯỢNG GIỮA HỌC KÌ I MÔN: HÓA HỌC – LỚP 12 Thời gian làm bài 40 phút ( không kể thời gian giao đề ) Đề thi gồm 02 trang |
Học sinh không được dùng bảng tuần hoàn các nguyên tố hoá học
|
|
I. MỤC TIÊU:
– Kiểm tra khả năng lĩnh hội kiến thức của hs về toàn bộ nội dung trong chương thông qua 25 câu trắc nghiệm
– Gv: biết được khả năng của hs và điều chỉnh cách dạy cho phù hợp
II . CHUẨN BỊ MA CHẬN ĐỀ :
III. PHƯƠNG PHÁP: Hs làm trắc nghiệm 40 phút
IV. NỘI DUNG:
1.Ma trận đề:
|
Mức độ Nội dung |
Biết |
Hiểu |
Vận dụng |
Vận dụng cao |
|
|
Este |
4câu |
1câu |
2,0 điểm |
||
|
Chất béo |
1 câu |
0,4 điểm |
|||
|
Cacbohidrat |
4 câu |
3câu |
1 câu |
3,2 điểm |
|
|
Amin và aminoaxit |
3 câu |
3câu |
1 câu |
2,8 điểm |
|
|
Bài tâp tổng hợp |
1 câu |
2 câu |
1câu |
1,6 điểm |
|
|
Tổng |
12câu |
6câu |
5câu |
2 câu |
10 điểm |
|
TRƯỜNG THPT XUÂN TRƯỜNG C NĂM HỌC 2021- 2022 ĐỀ CHÍNH THỨC |
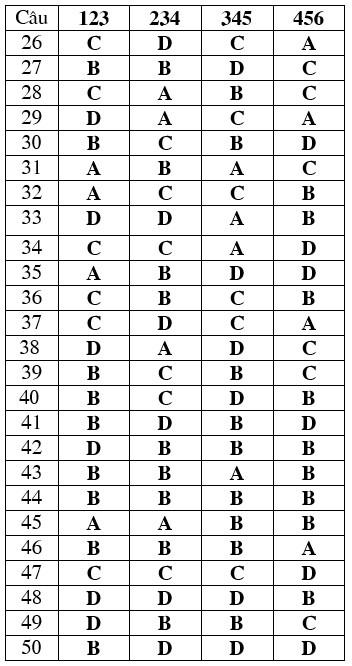
ĐÁP ÁN ĐỀ KIỂM TRA CHẤT LƯỢNG GIỮA HỌC KÌ I MÔN: HÓA HỌC – LỚP 12 Thời gian làm bài 40 phút ( không kể thời gian giao đề ) Đề thi gồm 02 trang |
|
C©u |
123 |
234 |
345 |
456 |
|
26 |
C |
D |
C |
A |
|
27 |
B |
B |
D |
C |
|
28 |
C |
A |
B |
C |
|
29 |
D |
A |
C |
A |
|
30 |
B |
C |
B |
D |
|
31 |
A |
B |
A |
C |
|
32 |
A |
C |
C |
B |
|
33 |
D |
D |
A |
B |
|
34 |
C |
C |
A |
D |
|
35 |
A |
B |
D |
D |
|
36 |
C |
B |
C |
B |
|
37 |
C |
D |
C |
A |
|
38 |
D |
A |
D |
C |
|
39 |
B |
C |
B |
C |
|
40 |
B |
C |
D |
B |
|
41 |
B |
D |
B |
D |
|
42 |
D |
B |
B |
B |
|
43 |
B |
B |
A |
B |
|
44 |
B |
B |
B |
B |
|
45 |
A |
A |
B |
B |
|
46 |
B |
B |
B |
A |
|
47 |
C |
C |
C |
D |
|
48 |
D |
D |
D |
B |
|
49 |
D |
B |
B |
C |
|
50 |
B |
D |
D |
D |
O2 Education gửi thầy cô link download đề thi
Xem thêm
- Tổng hợp đề thi giữa học kì 1 môn hóa cả 3 khối 10 11 12
- Tổng hợp đề thi học kì 1 lớp 12 môn hóa học
- Tổng hợp đề thi học kì 1 lớp 11 môn hóa học
- Tổng hợp đề thi học kì 1 lớp 10 môn hóa học
- Tổng hợp các chuyên đề hóa học lớp 10
- Tổng hợp các chuyên đề hóa học lớp 11
- Tổng hợp các chuyên đề hóa học lớp 12
- Tổng hợp đề thi HSG lớp 12 môn hoá học
- Tổng hợp đề thi môn hóa của bộ giáo dục từ năm 2007 đến nay
- Tổng hợp đề thi THPT QG 2021 file word có lời giải chi tiết
- Tổng hợp bài tập hữu cơ hay và khó có lời giải chi tiết
- Biện luận công thức phân tử muối amoni hữu cơ đầy đủ chi tiết
- Giải bài tập chất béo theo phương pháp dồn chất
- Tổng hợp 50+ bài tập chất béo có lời giải chi tiết
- Tổng hợp bài tập vô cơ hay và khó có lời giải chi tiết
- Tổng hợp đề thi môn hóa của bộ giáo dục từ năm 2007 đến nay
- Tổng hợp các phương pháp giải bài tập môn hoá học
- Tổng hợp thí nghiệm este chất béo hay và khó có đáp án chi tiết
