Phương pháp dùng chữ thay số (dùng các chữ cái thay cho các chữ số)
1. Các dạng toán sử dụng phương pháp dùng chữ thay số ở tiểu học
Ở một số bài toán, mà khi giải bài toán đó ta có thể dùng các chữ cái $a,b,c,$… $x,y,z$ hoặc $A, B, C, M, N,$… để biểu diễn số có một hoặc nhiều chữ số. Để giải quyết các dạng toán này, chúng ta sử dụng cấu tạo thập phân của một số, hoặc sử dụng tính chẵn lẻ, tính chất chữ số tận cùng của số tự nhiên, tính chia hết…
Xem thêm dạng toán Lập số tự nhiên và quy tắc đếm
1.1. Sử dụng cấu tạo thập phân của số
Để viết (biểu diễn) một số tự nhiên, chúng ta sử dụng mười chữ số là $0,1,2,3,4,5,6,7,8,9$ viết liền cạnh nhau. Trong đó, chữ số đầu tiên bên trái phải khác $0$. Đối với phương pháp này, chúng ta thường sử dụng các kí hiệu sau đây:
- $\overline{ab}$ để chỉ một số tự nhiên có 2 chữ số, chữ số hàng chục là $a$ (phải khác chữ số không $0$) và chữ số hàng đơn vị là $b$.
- $\overline{abc}$ để chỉ một số tự nhiên có 3 chữ số, chữ số hàng trăm là $a$, chữ số hàng chục là $b$, chữ số hàng đơn vị là $c$.
- $\overline{ab,cd}$ để chỉ số thập phân có 4 chữ số, phần nguyên có hai chữ số, phần thập phân có hai chữ số.
- $\overline{a00}$ là số tự nhiên có ba chữ số, chữ số hàng trăm là $a$, chữ số hàng chục và chữ số hàng đơn vị đều là $0$ (chữ số không). Hoặc $\overline{a00}$ là số tròn trăm mà chữ số hàng trăm là $a$.
- $\overline{ab0}$ là số tự nhiên có ba chữ số, chữ số hàng trăm là $a$, chữ số hàng chục là $b$, chữ số hàng đơn vị là $0$ (chữ số không) hoặc $\overline{ab0}$ là chữ số tròn chục mà chữ số hàng chục là $b$.
Phân tích cấu tạo của một số tự nhiên (Phân tích số theo các chỉ số hàng):
- $\overline{ab}=10\times a +b$ hoặc $\overline{ab}=\overline{a0} +b$.
- $\overline{abc}=100\times a + 10\times b + c$ hoặc $\overline{abc}=\overline{ab0}+c=\overline{a00}+\overline{b0}+c$ hoặc $\overline{abc} = \overline{a00} + \overline{bc}$.
- $\overline{a00}=100\times a$.
- $\overline{ab0}=100\times a + 10\times b$.
Ví dụ 1. Cho số tự nhiên có 2 chữ số, nếu lấy tổng các chữ số cộng với tích các chữ số của số đã cho thì bằng chính số đó. Tìm chữ số hàng đơn vị của số đã cho.
Hướng dẫn. Chúng ta sẽ lần lượt đi tóm tắt, biểu diễn số cần tìm bởi các chữ cái.
- Gọi số có 2 chữ số phải tìm là $\overline{ab}$ với $a,b$ là các chữ số từ 0 đến 9, trong đó $a\ne 0$ thì $\overline{ab}=10\times a + b$.
- Khi đó, tổng các chữ số của số đó là $a+b$, còn tích các chữ số của số đó là $a\times b$.
- Theo đề bài, chúng ta có $$10\times a + b = a + b + a \times b$$
Tiếp theo, chúng ta thực hiện phân tích số, làm xuất hiện những thành phần giống nhau ở bên trái và bên phải dấu bằng, rồi đơn giản những thành phần giống nhau đó để có biểu thức đơn giản nhất.
- Như vậy, chúng ta có $$10\times a + b = a + b + a \times b$$
- Cùng bớt $b$ ở hai biểu thức, ta được $$a \times 10 = a + a \times b$$
- Sử dụng tính chất Một số nhân với một tổng chúng ta viết lại thành $$a \times 10 = a \times (1 + b)$$
- Cùng chia hai biểu thức cho $a$, ta được $$10 = 1 + b$$
- Đến đây, dễ dàng suy ra $b = 10 – 1$ hay $b = 9$.
Kết luận: Vậy chữ số hàng đơn vị của số đó là: 9.
Ví dụ 2. Tìm số có ba chữ số, biết rằng phép chia số đó cho tổng các chữ số của nó là phép chia hết và được thương là 11.
Ví dụ 3. Tìm một số có 2 chữ số, biết rằng khi viết thêm số 21 vào bên trái số đó thì ta được một số lớn gấp 31 lần số cần tìm.
Hướng dẫn.
- Gọi số phải tìm là $\overline{ab}$, trong đó \( a > 0, a, b < 10 \)
- Khi viết thêm số 21 vào bên trái số $\overline{ab}$ ta được số mới là $\overline{21ab}$.
- Theo bài ra ta có: $$\overline{21ab}= 31\times \overline{ab}$$
- Sử dụng quy tắc phân tích số $\overline{21ab} = 2100 + \overline{ab}$, chúng ta có: $$ 2100 +\overline{ab} = 31\times \overline{ab} $$
- Như vậy, giả thiết của đề bài được viết lại như sau $$2100 + \overline{ab}= (30 + 1)\times \overline{ab}$$
- Áp dụng quy tắc một số nhân một tổng, chúng ta có: $$ 2100 + \overline{ab}= 30\times \overline{ab} + \overline{ab} $$
- Cùng bớt $\overline{ab}$ ở hai biểu thức $$2100 = \overline{ab}\times 30 $$
- Suy ra $\overline{ab} = 2100 : 30$ hay $\overline{ab} = 70$.
- hử lại, ta thấy $2170 : 70 = 31$ (đúng)
- Kết luận: Vậy số phải tìm là 70.
1.2. Sử dụng tính chất chẵn lẻ và chữ số tận cùng của số tự nhiên
- Số có tận cùng là 0, 2, 4, 6, 8 là số chẵn.
- Số có tận cùng là: 1, 3, 5, 7, 9 là các số lẻ.
- Tổng (hiệu) của 2 số chẵn là một số chẵn.
- Tổng (hiệu ) của 2 số lẻ là một số chẵn.
- Tổng (hiệu) của một số lẻ và một số chẵn là một số lẻ.
- Tổng của hai số tự nhiên liên tiếp là một số lẻ.
- Tích có ít nhất một thừa số chẵn là một số chẵn.
- Tích của a x a không thể có tận cùng là 2, 3, 7 hoặc 8.
Ví dụ 4. Tìm một số có 2 chữ số, biết rằng số đó gấp 6 lần chữ số hàng đơn vị của nó.
Hướng dẫn. Chúng ta sử dụng phương pháp dùng chữ thay số để giải bài toán này.
- Gọi số phải tìm là $\overline{ab}$ với $0 < a < 10, b < 10$.
- Theo đề bài ta có: $\overline{ab} = 6\times b$
- Sử dụng tính chất chẵn lẻ hoặc chữ số tận cùng.
- Vì $6\times b$ là một số chẵn nên $\overline{ab}$ là một số chẵn. Suy ra, $\overline{ab}$ phải tận cùng là $0,2,4,6,8$.
- Nếu $b = 0$ thì $\overline{ab} = 6\times b = 0$ (vô lý), do đó $b = 2, 4, 6$ hoặc $8$.
- Tìm giá trị bằng phương pháp thử chọn (có thể lập bảng giá trị để dễ nhìn hơn)
- Nếu $b = 2$ thì $\overline{ab}= 6\times 2 = 12$. (chọn)
- Nếu $b = 4$ thì $\overline{ab}= 6\times 4 = 24$. (chọn)
- Nếu $b = 6$ thì $\overline{ab}= 6\times 6 = 36$. (chọn)
- Nếu $b = 8$ thì $\overline{ab}= 6\times 8 = 48$. (chọn)
- Vậy ta được 4 số thoả mãn đề bài là: $12, 24, 36, 48$.
1.3. Sử dụng kỹ thuật tính khi thực hiện phép tính
Trong phép cộng, nếu cộng hai chữ số trong cùng một hàng thì có nhớ nhiều nhất là 1, nếu cộng 3 chữ số trong cùng một hàng thì có nhớ nhiều nhất là 2,…
Ví dụ 5. Tìm số $\overline{abc}$ biết rằng $$ \overline{abc}= \overline{ab}+ \overline{bc}+ \overline{ca}. $$
Hướng dẫn. Chúng ta có:
- $ \overline{abc}= \overline{ab}+ \overline{bc}+ \overline{ca} $
- $\overline{abc}= (\overline{ab}+\overline{ca}) + \overline{bc}$ (tính chất kết hợp và giao hoán của phép cộng)
- $\overline{abc}- \overline{bc}= \overline{ab}+\overline{ca}$ (tìm một số hạng của tổng)
- $\overline{a00}= \overline{aa}+ \overline{ca}$
- Chúng ta đặt phép tính như sau:
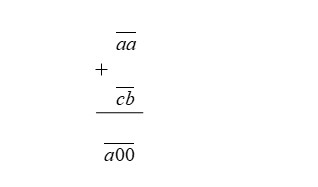
- Nhìn vào cách đặt tính ta thấy phép cộng có nhớ sang hàng trăm. Mà đây là phép cộng hai số hạng nên hàng trăm của tổng chỉ có thể bằng 1. Vậy $a = 1$.
- Với $a = 1$ thì ta có: $$100 = 11 + \overline{cb}$$
- Suy ra $\overline{cb}= 100 – 11$ hay $\overline{cb}= 89$.
- Điều trên đồng nghĩa với $c = 8 $ và $ b = 9$ và số cần tìm là $\overline{abc}= 198$.
- Thử lại: $19 + 98 + 81 = 198$ (đúng)
- Vậy số cần tìm $\overline{abc}$ là 198.
Ví dụ 6. Tìm số có 4 chữ số, biết rằng nếu xoá đi chữ số ở hàng đơn vị và hàng chục thì số đó sẽ giảm đi 1188 đơn vị.
- Gọi số phải tìm là $\overline{abcd}$ với $a > 0; a, b, c, d < 10$.
- Khi xoá đi $\overline{cd}$ ta được số mới là $\overline{ab}$.
- Theo đề bài ra ta có: $$ \overline{abcd}= 1188 + \overline{ab} $$
- Đặt phép tính theo hàng dọc, chúng ta có:
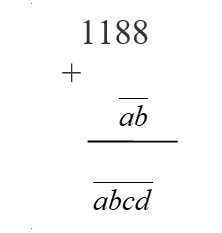
- Trong phép cộng, khi cộng 2 chữ số trong cùng một hàng thì có nhớ nhiều nhất là 1 nên $\overline{ab}$ chỉ có thể là 11 hoặc 12.
- Nếu $\overline{ab}= 11$ thì $\overline{abcd}= 1188 + 11 = 1199$.
- Nếu $\overline{ab}= 12$ thì $\overline{abcd}= 1188 + 12 = 1200$.
- Vậy ta tìm được 2 số thoả mãn đề bài là $1199$ và $1200$.
1.4. Xác định giá trị lớn nhất hoặc giá trị nhỏ nhất của một số hoặc một biểu thức
- Một số có 2; 3; 4; … chữ số thì tổng các chữ số có giá trị nhỏ nhất là 1 và giá trị lớn nhất lần lượt là: $9\times 2 = 18$; $9\times 3 = 27$; $9\times 4 = 36$…
- Trong tổng $(a + b)$ nếu thêm vào $a$ bao nhiêu đơn vị và bớt đi ở $b$ bấy nhiêu đơn vị (hoặc ngược lại) thì tổng vẫn không thay đổi. Do đó nếu $(a + b)$ không đổi mà khi $a$ đạt giá trị lớn nhất có thể thì $b$ sẽ đạt giá trị nhỏ nhất có thể và ngược lại. Giá trị lớn nhất của $a$ và $b$ phải luôn nhỏ hơn hoặc bằng tổng $(a + b)$.
- Trong một phép chia có dư thì số chia luôn lớn hơn số dư.
Ví dụ 7. Tìm số có 2 chữ số, biết rằng nếu số đó chia cho chữ số hàng đơn vị của nó thì được thương là 6 và dư 5.
Hướng dẫn.
- Gọi số phải tìm là $\overline{ab}$ với $0 < a < 10, b < 10$.
- Theo đề bài ra ta có: $\overline{ab}: b = 6$ dư 5 hay $$ \overline{ab}= b\times 6 + 5. $$
- Vì số chia luôn lớn hơn số dư nên $b > 5$, như vậy $5 < b < 10$.
- Nếu $b$ có giá trị nhỏ nhất là $6$ thì $\overline{ab}$ đạt giá trị nhỏ nhất là $6\times 6 + 5 = 41$. Nếu $b$ có giá trị lớn nhất là $9$ thì $\overline{ab}$ đạt giá trị lớn nhất là $9\times 6 + 5 = 59$. Suy ra $\overline{ab}$ lớn hơn hoặc bằng $41$ và nhỏ hơn hoặc bằng $59$. Nên $a$ chỉ có thể nhận giá trị $4$ hoặc $5$.
- Nếu $a = 4$ thì $\overline{4b}= b\times 6 + 5$.
- Nếu $a = 5$ thì $\overline{5b}= b\times 6 + 5$.
- Tiếp theo, chúng ta sử dụng cấu tạo thập phân của số. Xét các khả năng sau:
- Nếu $\overline{4b}= b\times 6 + 5$ thì \begin{align}
40 + b &= b\times 6 + 5\\
35 + 5 + b &= b\times 5 + b + 5\\
35 &= b\times 5
\end{align}
hay $b = 35 : 5 = 7$. Ta được số cần tìm là 47. - Nếu $\overline{5b}= b\times 6 + 5$ thì \begin{align}
50 + b &= b\times 6 + 5\\
45 + 5 + b &= b\times 5 + b + 5\\
45& = b\times 5
\end{align}
hay $b = 45 : 5 = 9$ và tìm được số 59.
- Nếu $\overline{4b}= b\times 6 + 5$ thì \begin{align}
- Thử lại
- $7\times 6 + 5 = 47$ (chọn)
- $9\times 6 + 5 = 59$ (chọn)
- Vậy ta tìm được 2 số thoả mãn yêu cầu của đề bài là 47 và 59.
1.5. Tìm số khi biết mối quan hệ giữa các chữ số
Ví dụ 8. Tìm số có 3 chữ số, biét chữ số hàng trăm gấp đôi chữ số hàng chục, chữ số hàng chục gấp 3 lần chữ số hàng đơn vị.
Hướng dẫn.
- Gọi số phải tìm là $\overline{abc}$ với $0 < a < 10; b, c < 10$.
- Vì $a = 2\times b$ và $b = 3\times c$ nên $a = 2\times 3\times c = 6\times c$, mà $0 < a < 10$ nên $0 < 6\times c < 10$.
- Suy ra $0 < c < 2$. Và do đó $c$ chỉ có thể nhận giá trị là $1$.
- Khi đó $b = 1\times 3 = 3$ và $a = 3\times 2 = 6$.
- Vậy số phải tìm là $631$.
Ví dụ 9. Tìm số có 3 chữ số, biết rằng nếu số đó cộng với tổng các chữ số của nó thì bằng 555.
Hướng dẫn.
- Gọi số phải tìm là $\overline{abc}$ điều kiện $a > 0; a, b, c < 10$.
- Theo đầu bài ta có: $$ \overline{abc}+ a + b + c = 555 $$.
- Nhìn vào biểu thức trên, ta thấy đây là phép cộng không có nhớ sang hàng trăm nên $a = 5$.
- Khi đó ta có: \begin{align}
\overline{5bc}+ 5 + b + c &= 555\\
500 + \overline{bc} + 5 + b + c &= 555\\
505 + \overline{bb} + c + c &= 555\\
\overline{bb}+ c\times 2 &= 555 – 505\\
\overline{bb}+ c\times 2 &= 50
\end{align} - Nếu $c$ đạt giá trị lớn nhất là $9$ thì $\overline{bb}$ đạt giá trị nhỏ nhất là $50 – 9\times 2 = 32$, do đó $b > 2$.
- Vì $\overline{bb} + c\times 2 = 50$ nên $\overline{bb}< 50$ nên $b < 5$. Do đó, $b = 3$ hoặc $b=4$.
- Vì $c\times 2$ và $50$ đều là số chẵn nên $b$ phải là số chẵn. Do đó $b = 4$.
- Khi đó ta có: \begin{align}
44 + c\times 2 &= 50\\
c\times 2 &= 50 – 44\\
c\times 2 &= 6 \\
c &= 6 : 2 = 3
\end{align} - Vậy $\overline{abc}= 543$.
- Thử lại $543 + 5 + 4 + 3 = 555$ (đúng)
- Vậy số phải tìm là $543$.
2. Bài tập về phương pháp dùng chữ thay số ở tiểu học
Bài 1. Tìm một số có 2 chữ số, biết rằng khi viết thêm chữ số 4 vào bên trái số đó, ta được một số gấp 9 lần số phải tìm.
Bài 2. Tìm một số có 2 chữ số, khi viết thêm chữ số 9 vào bên trái số đó ta được một số gấp 13 lần số phải tìm.
Bài 3. Tìm một số có 3 chữ số, biết rằng khi viết thêm chữ số 5 vào bên phải số đó ta được một số hơn số phải tìm 1112 đơn vị.
Bài 4. Tìm một số có 2 chữ số, biết rằng khi viết thêm chữ số 5 vào bên phải số đó ta được một số hơn số phải tìm 230 đơn vị.
Bài 5. Cho một số có 2 chữ số. Nếu viết thêm chữ số 1 vào đằng trước và đằng sau số đó thì số đó tăng lên 21 lần. Tìm số đã cho.
Bài 6. Tìm số có 4 chữ số, biết rằng khi viết thêm chữ số 5 vào bên phải số đó ta được số lớn gấp 5 lần số nhận được khi ta viết thêm chữ số 1 vào bên trái số đó.
Bài 7. Cho số có 3 chữ số, nếu viết thêm chữ số 1 vào bên phải số đó, viết thêm chữ số 2 vào bên trái số đó ta đều được số có 4 chữ số mà số này gấp 3 lần số kia.
Bài 8. Cho một số có 3 chữ số, nếu xoá đi chữ số hàng trăm thì số đó giảm đi 3 lần. Tìm số đó.
Bài 9. Tìm một số có 4 chữ số, nếu xoá đi chữ số hàng nghìn thì số đó giảm đi 9 lần.
Bài 10. Tìm một số có 3 chữ số, nếu viết thêm chữ số 0 xen giữa chữ số hàng trăm và chữ số hàng chục ta được một số lớn gấp 7 lần số đó.
Bài 11. Tìm một số có 3 chữ số, biết rằng nếu viết thêm chữ số 0 xen giữa chữ số hàng trăm và chữ số hàng chục thì ta được một số lớn gấp 6 lần số cần tìm.
Bài 12. Cho một số có 2 chữ số, nếu xen giữa 2 chữ số của số đó ta viết thêm chính số đó thì ta được một số có 4 chữ số gấp 99 lần số đã cho. Hãy tìm số đó.
Bài 13. Tìm một số tự nhiên có 2 chữ số, biết rằng nếu viết thêm chữ số 0 xen giữa chữ số hàng chục và chữ số hàng đơn vị của số đó ta được số gấp 10 lần số cần tìm, nếu viết thêm chữ số 1 vào bên trái số vừa nhận được thì số đó lại tăng lên 3 lần.
Bài 14. Tìm một số có 4 chữ số, biết rằng nếu xoá đi chữ số hàng chục và chữ số hàng đơn vị thì số đó sẽ giảm đi 1188 đơn vị.
Bài 15. Tìm một số có 4 chữ số, biết rằng nếu xoá đi chữ số hàng chục và chữ số hàng đơn vị thì số đó sẽ giảm đi 4455 đơn vị.
Bài 16. Có 2 miếng bìa, mỗi miếng bìa viết một số có 2 chữ số, hiệu 2 số viết trên 2 miếng bìa là 25, ghép 2 miếng bìa lại ta được một số có 4 chữ số. Tổng các số có 4 chữ số ghép được chia cho 101 ta được thương là71. Tìm số viết trên mỗi miếng bìa.
Bài 17. Cho 2 số có 2 chữ số có tổng của 2 số đó bằng 35. Ta đem số lớn ghép vào bên trái số nhỏ, rồi đem số lớn ghép vào bên phải số nhỏ thì được 2 số có 4 chữ số. Hiệu 2 số có 4 chữ số đó là 1485. Tìm 2 số đã cho.
Bài 18. Cho số có 4 chữ số, có chữ số hàng đơn vị là 8. Nếu chuyển chữ số hàng đơn vị lên đầu thì sẽ được số mới lớn hơn số đã cho 4059 đơn vị. Tìm số đã cho.
Bài 19. Tìm số có 6 chữ số, biết chữ số tận cùng là 4, nếu chuyển vị trí chữ số này từ cuối lên đầu nhưng không thay đổi thứ tự các chữ số còn lại thì ta được một số lớn gấp 4 lần số đã cho.
Bài 20. Tìm một số có 6 chữ số, biết rằng nếu chuyển vị trí từ hàng cao nhất xuống hàng thấp nhất nhưng không thay đổi thứ tự các chữ số còn lại thì ta được một số lớn gấp 3 lần số đã cho.
Bài 21. Cho số có 3 chữ số. Nếu chuyển vị trí chữ số hàng trăm thành chữ số hàng đơn vị , không thay đổi vị trí các chữ số còn lại thì được một số mới bằng $\frac{3}{4}$ số đã cho. Tìm số đó.
Bài 22. Tìm số có 2 chữ số. Nếu đổi vị trí các chữ số của số ấy ta được một số mới, số mới này đem chia cho số đã cho thì được thương là 3 và số dư là 13.
Bài 23. Tìm số có 4 chữ số. Nếu viết số đó theo thứ tự ngược lại thì vẫn được số đó. Tổng các chữ số của số đó bằng 24. Số gồm 2 chữ số bên trái lớn hơn số gồm 2 chữ số bên phải là 36.
Bài 24. Năm sinh của hai ông Vũ Hữu và Lương Thế Vinh là một số có 4 chữ số, tổng các chữ số bằng 10. Nếu viết năm sinh theo thứ tự ngược lại thì năm sinh không đổi. Em hãy tìm năm sinh của hai ông.
Bài 25. Thế kỷ 20 dân tộc ta có 2 sự kiện lịch sử trọng đại. Hai năm sảy ra sự kiện lịch sử trọng đại đó có các chữ số của năm này giống các chữ số của năm kia, chỉ khác nhau ở vị trí các chữ số ở hàng chục và hàng đơn vị. Biết rằng tổng các chữ số ở 1 năm bằng 19 và nếu tăng chữ số hàng chục lên 3 đơn vị thì chữ số hàng chục gấp đôi các chữ số ở hàng đơn vị. Em hãy tính xem hai năm đó là hai năm nào?
Bài 26. Tìm một số có 2 chữ số, biết rằng số đó gấp 5 lần tổng các chữ số của nó.
Bài 27. Tìm một số có 3 chữ số, biết rằng số đó gấp 11 lần tổng các chữ số của nó.
Bài 28. Tìm một số có 2 chữ số, biết rằng số đó gấp 21 lần hiệu của chữ số hàng chục và hàng đơn vị.
Bài 29. Tìm một số có 2 chữ số, biết rằng số đó gấp 21 lần tích các chữ số của nó.
Bài 30. Tìm một số có 2 chữ số, biết rằng số đó gấp 5 lần tích các chữ số của nó.
Bài 31. Cho số có 2 chữ số, nếu lấy số đó chia cho tổng các chữ số của nó thì được thương là 5 và dư 12. Tìm số đó.
Bài 32. Cho số có 2 chữ số, nếu lấy số đó chia cho hiệu các chữ số của nó thì được thương là 28 dư 1. Tìm số đó.
Bài 33. Cho số có 2 chữ số, nếu lấy số đó chia cho hiệu của các chữ số hàng chục và hàng đơn vị thì được thương là 26 dư 1. Tìm số đó.
Bài 34. Cho số có 2 chữ số mà chữ số hàng chục chia hết cho chữ số hàng đơn vị. Tìm số đã cho, biết rằng khi chia số đó cho thương của chữ số hang chục và hàng đơn vị thì được thương là 20 và dư 2.
Bài 35. Cho số có 2 chữ số, nếu lấy số đó chia cho tích các chữ số của nó thì được thương là 5 dư 2 và chữ số hàng chục gấp 3 lần chữ số hàng đơn vị. Tìm số đó.
Bài 36. Tìm số có 4 chữ số, biết rằng số đó cộng với số có 2 chữ số tạo bởi chữ số hàng nghìn và hàng trăm và số có 2 chữ số tạo bởi chữ số hàng chục và hàng đơn vị của số đó được tổng là 7968.
Bài 37. Tìm 2 số, biết rằng số lớn gấp 4 lần số nhỏ và nếu bớt 2 đơn vị ở số lớn và thêm 2 đơn vị vào số nhỏ thì được 2 số tròn chục.
Bai 38. Cho một số có 2 chữ số, biết rằng chữ số hàng chục gấp 3 lần chữ số hàng đơn vị, nếu đổi vị trí các chữ số cho nhau thì số đó giảm đi 54 đơn vị. Tìm số đó.
Bài 39. Cho một số có 2 chữ số, trong đó chữ số hàng chục bằng $\frac{1}{3}$ chữ số hàng đơn vị. Nếu đổi vị trí các chữ số cho nhau thì số đó tăng thêm 36 đơn vị. Hãy tìm số đó.
Bài 40. Cho một số có 4 chữ số, chữ số hàng trăm gấp 2 lần chữ số hàng nghìn, chữ số hàng chục lớn hơn chữ số hàng nghìn nhưng nhỏ hơn chữ số hàng trăm. Chữ số hàng đơn vị bằng tổng 3 chữ số trên. Tìm số đó.
Bài 41. Tìm một số có 4 chữ số, biết rằng tích 2 chữ số ngoài cùng bằng 40, tích 2 chữ số ở giữa bằng 18 và chữ số hàng nghìn lớn hơn chữ số hàng chục bao nhiêu thì chữ số hàng đơn vị cũng hơn chữ số hàng trăm bấy nhiêu.
Bài 42. Tìm một số chẵn có 4 chữ số, biết số tạo nên bởi chữ số hàng trăm và hàng chục gấp 4 lần chữ số hàng đơn vị và gấp 3 lần chữ số hàng nghìn.
Bài 43.
- Tìm số $\overline{abc}$ biết. $\overline{abcd}- \overline{bcd}\times 2 = \overline{ac}$
- Tìm số tự nhiên $\overline{abc}$ biết. $a + \overline{abc}+ \overline{abc} = \overline{bcb}$
- Tìm số $\overline{abcd}$ biết. $\overline{dcba}+ \overline{dcb}+ \overline{dc}+ d = 4321$
- Tìm số $\overline{abcd}$ biết. $\overline{abcd}- \overline{abc}- \overline{ab}- a = 2086$
Bài 44. Tìm số $\overline{abcd}$ biết $(\overline{ab}\times c + d)\times d = 1977$.
Bài 45. Cho một số có 5 chữ số mà tổng các chữ số ấy bằng 5. Chữ số hàng vạn bằng số chữ số 0 có mặt trong số ấy. Chữ số hàng nghìn bằng số chữ số 1, chữ số hàng trăm bằng số chữ số 2, chữ số hàng chục bằng số chữ số 3, chữ số hàng đơn vị bằng số chữ số 4 có mặt trong số ấy. Tìm số đã cho.












