Hóa học – Đầu năm lớp 10 thì ôn gì?
Để học tốt môn Hóa ở THPT, các em học sinh vừa vào lớp 10 nên ôn tập gì, học cái gì, cách học như thế nào? Bài viết này O2 Education sẽ bật mí một số bí quyết để chinh phục môn Hóa ngay từ lớp 10. Tài liệu dạng file PDF mời các em tải ở cuối bài viết.
Xem thêm Tài liệu ôn tập đầu năm hóa học 11
1. Phương pháp và thái độ học tập môn Hóa học lớp 10
Để học tốt hoá học lớp 10, các em học sinh cần.
- Yêu thích bộ môn.
- Ôn lại các kiến thức lớp 8, lớp 9.
- Ở lớp chú ý nghe giảng, đánh dấu phần khó, phần mới để về nhà xem lại.
- Về nhà sử dụng giấy nháp để tóm tắt và viết các phương trình hóa học, làm các bt trong SGK, SBT và mở rộng các bài tập trong sách tham khảo.
2. Ôn tập kiến thức hóa ở THCS
Hóa học lớp 10 tiếp nối và phát triển tiếp mạch kiến thức hóa học THCS. Do đó, trong phần này, chúng tôi sẽ tóm tắt lại kiến thức môn hóa ở cấp 2 để các em học sinh nắm chắc trước khi bước chương trình hóa học lớp 10.
2.1. Tên, STT, KHHH, hóa trị, nguyên tử khối của 26 nguyên tố thường gặp
- 20 nguyên tố đầu + Fe, Cu, Zn, Ag (Z=47), Ba (Z=56), Pb (Z=82)
- Chú ý: Kim loại và phi kim ở trạng thái rắn phân tử gồm 1 nguyên tử như C,S, P, Si… Phi kim ở trạng thái lỏng, khí phân tử gồm 2 nguyên tử như H2, N2, O2, F2, Cl2, Br2…
2.2. Hoá trị và cách lập công thức phân tử của hợp chất.
a. Hoá trị của một số kim loại và gốc axit thường gặp
- Hoá trị là con số biểu thị khả năng liên kết của nguyên tử nguyên tố này với nguyên tử nguyên tố khác.
- Kí hiệu bằng các số La Mã
- Hóa trị của các kim loại (trong dãy hoạt động hóa học của kim loại)
- Giới thiệu 6 axit thường gặp HCl, HNO3, H2SO4, H2CO3, H2CO3, H3PO4, …
- Bảng hóa trị

Dãy hoạt động hóa học của kim loại
K Ba Ca Na Mg Al Zn Fe Ni Sn Pb H2 Cu Hg Ag Pt Au
Trong dãy hđ hh của kim loại có K, Na, Ag hóa trị I; Al, Fe hóa trị III, còn lại đều hóa trị II (không xét Au, Pt)
b. Lập công thức phân tử của hợp chất
– A có hoá trị x, B có hoá trị y =>
- + Với xy hợp chất giữa A và B có công thức AyBx. VD: Al2O3, P2O5, Al2(SO4)3.
- + Với x = y hợp chất giữa A và B có công thức AB. VD: CaCO3, NaCl, FeO, MgSO4.
- + Với x = a.y (aN*) hợp chất giữa A và B có công thức ABn VD: MgCl2, Fe(NO3)3, SO2.
– Hợp chất AnBm với A có hoá trị x, B có hoá trị y ta có n.x = m.y
Vận dụng: Lập công thức phân tử của các chất có tên gọi sau (cho dưới dạng tên): NaCl, Ca(NO3)3, Fe2(SO4)3, SO3, Ag2S, Ba(HCO3)3, Mg3(PO4)2, Al(NO3)3, ZnCl2, CuSO4…
2.3. Một số hợp chất vô cơ thường gặp.
a. Axit
- – Định nghĩa: Axit là hợp chất mà phân tử gồm một hay nhiều nguyên tử hiđro liên kết với gốc axit.
- – Tính tan: Hầu hết các axit đều tan trong nước.
- – Phân loại:
- Dựa vào độ mạnh yếu
- Dựa vào thành phần axit có oxi và axit không có oxi
- Dựa vào tính chất hoá học chung:
- Làm đổi màu chất chỉ thị (quỳ tím hoá đỏ)
- Tác dụng với bazơ, oxit bazơ, kim loại (trước H), muối (sau pư có…)
Nhắc lại dãy hoạt động hoá học của kim loại.
Viết phương trình hóa học minh hoạ (lưu ý trường hợp HNO3, H2SO4 đặc, loãng)
| STT | Tên axit | CTPT | Gốc axit | STT | Tên axit | CTPT | Gốc axit |
| 1 | Sunfu hiđric | H2S | Sunfua | 12 | Nitric | HNO3 | Nitrat |
| 2 | Flo hiđric | HF | Florua | 13 | Nitrơ | HNO2 | Nirit |
| 3 | Brôm hiđric | HBr | Bromua | 14 | Silixic | H2SiO3 | Silicat |
| 4 | Iốt hiđric | HI | Iotua | 15 | Cacbonic | H2CO3 | Cacbonat |
| 5 | Clo hiđric | HCl | Clorua | 16 | Photphoric | H3PO4 | Photphat |
| 6 | Hipoclorơ | HClO | Hipoclorit | 17 | Photphorơ | H3PO3 | Photphit |
| 7 | Clorơ | HClO2 | Clorit | 18 | Xian hiđric | HCN | Xianua |
| 8 | Cloric | HClO3 | Clorat | 19 | Aluminic* | HAlO2 | Aluminat |
| 9 | Pecloric | HClO4 | Peclorat | 20 | Zincic* | H2ZnO2 | Zincat |
| 10 | Sunfuric | H2SO4 | Sunfat | 21 | Axetic | CH3COOH | Axetat |
| 11 | Sunfurơ | H2SO3 | Sunfit |
b. Bazơ
- – Định nghĩa: Bazơ là hợp chất mà phân tử gồm nguyên tử kim loại liên kết với một hay nhiều nhóm hiđroxit (nhóm OH).
- – Tính tan: + Bazơ của kim loại mạnh Li, K, Ba, Ca, Na tan trong nước
- + Bazơ của kim loại còn lại đều không tan trong nước
- – Tính chất hoá học chung: + Làm đổi màu chất chỉ thị (quỳ tím, phenolphtalein)
- + Tác dụng với axit, oxit axit, muối (sau pư có …)
- Viết phương trình hóa học minh hoạ.
c. Muối
- – Định nghĩa: Muối là hợp chất mà phân tử gồm một hay nhiều nguyên tử kim loại (hoặc NH4+) liên kết với một hay nhiều gốc axit.
- – Tính tan:
- Các muối K+, Na+, NH4+, NO3– , CH3COO– đều tan trong nước
- Các muối khác
| STT | MUỐI | ĐẶC ĐIỂM TÍNH TAN TRONG NƯỚC |
| 1 | Clorua () | Hầu hết đều tan (trừ AgCl không tan và PbCl2 ít tan) |
| 2 | Sunfat () | Hầu hết đều tan (trừ PbSO4 và BaSO4 không tan; CaSO4, Ag2SO4 ít tan) |
| 3 | Sunfit () | Hầu hết đều không tan (trừ Li2SO3, K2SO3, Na2SO3, (NH4)2SO3 tan) |
| 4 | Cacbonat () | Hầu hết đều không tan (trừ Li2CO3, K2CO3, Na2CO3, (NH4)2CO3 tan) |
| 5 | Photphat () | Hầu hết đều không tan (trừ K3PO4, Na3PO4, (NH4)3PO4 tan) |
| 6 | Hiđroxit () | Hầu hết đều không tan (trừ LiOH, KOH, Ba(OH)2, NaOH tan và Ca(OH)2 ít tan) |
– Tính chất hoá học chung: Tác dụng với axit, bazơ, muối (sau pư có…)
Viết phương trình hóa học minh hoạ
d. Oxit
- – Định nghĩa: Oxit là hợp chất của oxi với nguyên tố khác
- – Phân loại:
- + Oxit axit thường là oxit của phi kim, Vd:
- + Oxit bazơ thường là oxit của kim loại, Vd:
- + Oxit lưỡng tính là oxit vừa có tính chất của oxit axit, vừa có tính chất của oxit bazơ
- + Oxit trung tính – là oxit không có khả năng tạo muối
- – Tính chất hoá học
- + Oxit axit tác dụng với nước, dung dịch bazơ, oxit bazơ. pthh minh hoạ
- + Oxit bazơ tác dụng với nước, dung dịch axit, oxit axit. pthh minh hoạ
2.4. Cách viết pthh của một phản ứng trao đổi.
a. Các bước viết pthh của phản ứng trao đổi
- Bước 1: Xét xem phương trình có sự tham gia của axit hay không. Nếu có chuyển sang bước 2. Nếu không có thì cả hai chất tham gia đều phải tan (nếu có chất không tan thì phản ứng không xảy ra)
- Bước 2: Ghép để tạo thành chất mới (đầu chất này ghép với đuôi chất kia và ngược lại).
- Bước 3: Xét các chất sau phản ứng phải có ít nhất một trong các chất kết tủa, khí hoặc nước (đại diện cho điện li yếu với lớp 10). Nếu có ít nhất một trong các chất kể trên thì pt có xảy ra, cân bằng phương trình. Nếu không có các chất này thì phản ứng không xảy ra.
b. Điều kiện của phản ứng trao đổi
- – Đk cần: Nếu không có sự tham gia của axit trong phản ứng thì cả hai chất đều phải tan.
- – Đk đủ: Sau phản ứng phải có ít nhất một trong các chất: kết tủa, khí, H2O (đại diện cho điện li yếu).
Chú ý:
- Trừ phản ứng có sự tham gia của axit (không cần xét tính tan) các phản ứng còn lại các chất tham gia phản ứng đều phải tan.
- Khi viết pthh của phản ứng trao đổi thì không viết các chất H2CO3, H2SO3, NH4OH, AgOH mà viết tương ứng các chất CO2 + H2O, SO2 + H2O, NH3 + H2O, Ag2O + H2O
Vận dụng: Hoàn thành các phương trình hóa học của các phản ứng sau (nếu có):
- Canxi cacbonat + Natri clorua
- Bari clorua + Natri cacbonat
- Bari nitrat + Đồng (II) sunfat
- Magie nitrat + Kẽm sunfat
- Sắt (II) nitrat + natri hiđroxit
- Sắt (III) sunfat + Kali hiđroxit
- Amoni clorua + Natri hiđroxit
- Đồng (II) clorua + Kali sunfua
- Canxi hiđrocacbonat + axit nitric
- Sắt (III) nitrat + Magie hiđroxit
- Magie sunfit + Axit clohiđric
- Sắt (II) sunfua + axit clohiđric
- Amoni clorua + bạc nitrat
- Nhôm clorua + dd amoniac
- Amoni sunfat + Bari hiđroxit
- Nhôm nitrat + Natri hiđroxit
- Natri hiđroxit + axit sunfuric
- Bari hiđroxit + axit clohiđric
- Sắt (III) hiđroxit + axit nitric
- Magie hiđroxit + axit sunfuric
- Nhôm oxit + axit nitric 21. Sắt (II) oxit + axit clohiđric
- Sắt từ oxit + axit clohiđric 23. Khí cacbonic + Natri hiđoxit
- Khí sunfurơ + Kali hiđroxit 25. Điphotpho pentaoxit + Natri hiđoxit
CaCO3 + NaCl BaCl2 + Na2CO3 Ba(NO3)2 + CuSO4 FeSO4 + NaOH
CaCO3 + H2SO4 CuCl2 + K2S Mg(NO3)2 + ZnSO4 MgSO3 + HCl
Fe2(SO4)3 + KOH FeS + HCl Ca(HCO3)2 + HNO3 AlCl3 + NaOH
NH4Cl + AgNO3 NH4Cl + NaOH NaOH + HCl Mg(OH)2 + HNO3
Fe3O4 + HCl Fe2O3 + H2SO4 CO2 + KOH SO2 + KOH
Al2O3 + HCl CaO + HNO3 P2O5 + NaOH
2.5. Các công thức tính số mol (n) và nồng độ
a. Các công thức tính số mol
- $n=\frac{m}{M}$, trong đó m: khối lượng chất (gam); M: khối lượng mol (đvC – u). Ví dụ:
- Tính số mol của 0,69 gam Na (0,03 mol); 14,2 gam khí clo (0,2 mol)
- Tính khối lượng của 0,12 mol photpho (3,72 gam); 0,05 mol kẽm (3,25 gam)
- Tính KLNT của nguyên tố Cd biết 0,06 mol Cd nặng 6,72 gam (112 đvC)
- Tính KLNT của nguyên tố oxi biết 0,07 mol oxi nặng 2,24 gam ( MO2 = 32 => MO = 16 đvC)
- $n=\frac{V}{22,4}$, trong đó V là thể tích chất khí ở điều kiện tiêu chuẩn (đktc) – điều kiện 00C, 1atm, 22,4 là thể tích 1 mol chất khí ở đktc. Ví dụ:
- Tính số mol của 4,48 lít khí hiđro ở đktc (0,2 mol); 0,56 lít khí N2 ở đktc (0,025 mol)
- Tính thể tích của 0,05 mol khí clo ở đktc (1,12 lít); 0,03 mol khí CO2 ở đktc (0,672 lít)
- Tính thể tích của 7,1 gam khí clo ở đktc
- Tính khối lượng của 3,36 lít khí oxi ở đktc
- $n=C_M.V$ với CM là nồng độ mol/l của chất (mol/l hoặc M), V là thể tích dung dịch (lít). Ví dụ,
- Tính số mol của NaCl có trong 300ml dung dịch NaCl 0,5M
- Tính nồng độ mol/l của dung dịch HCl biết 300ml dung dịch HCl đó có chứa 0,15 mol HCl
- \(n=\frac{C \% \cdot m_{ dd }}{100 M}=\frac{C \% \cdot d \cdot V}{100 M}\) với C% là nồng độ % (%), mdd là khối lượng dung dịch (gam), M khối lượng mol (đvC – u), D là khối lượng riêng của dung dịch, V là thể tích dung dịch (ml).
Ví dụ:- Tính số mol của KOH có trong 50 gam dung dịch KOH 14% (0,125mol)
- Tính khối lượng của dung dịch MgCl2 biết dd này chứa 0,15 mol MgCl2 và nồng độ của MgCl2 trong dd là 23,75%.
- Tính số mol của NaCl có trong 300ml dung dịch NaCl 14,625% (D=1,2g/ml) (0,9mol)
- Tính khối lượng riêng của dung dịch KCl biết 200ml dung dịch KCl 25% có chứa 0,75 mol KCl (0,1175g/ml)
- \(n=\frac{P . V}{R T}\), trong đó P: áp suất chất khí (atm, 1atm = 760 mmHg), V là thể tích chất khí (lít), R là hằng số chất khí, T nhiệt độ Kenvin T = t0C + 273. Ví dụ,
- Tính số mol của 2,46 lít khí oxi ở 270C, 2 atm
Chú ý: Công thức số 1 áp dụng cho cả chất rắn, lỏng, khí. Công thức số 2, 5 chỉ áp dụng cho chất khí. Công thức 3, 4 áp dụng cho dung dịch.
b. Các công thức về nồng độ dung dịch.
- Các khái niệm:
- Dung dịch là hỗn hợp đồng nhất của dung môi và chất tan.
- Dung môi là chất lỏng có thể hoà tan chất khác.
- Chất tan là chất có khả năng tạo thành dung dịch với một dung môi thích hợp.
- Vd: Hoà tan NaCl vào nước để thu được dung dịch NaCl thì NaCl là chất tan, nước là dung môi.
- Nồng độ % (C%) là số gam chất tan có trong 100 gam dung dịch (đơn vị %).
- Với mct là khối lượng chất tan (g), mdd = mct + mdm là khối lượng dung dịch (g)
- Vd: Dung dịch NaCl 5% tức là cứ 100 gam dung dịch có 5 gam NaCl
- Vận dụng: Hoà tan 25g KOH vào 100g H2O tính nồng độ % của dd thu được. (20%)
- Nồng độ mol/l (CM) là số mol chất tan có trong 1 lít dung dịch. (đơn vị M hoặc mol/l)
- Với n là số mol chất tan (mol), V là thể tích dung dịch (lít)
- Vd : Dung dịch H2SO4 1,5M tức là trong 1 lít dung dịch có 1,5 mol H2SO4
- Vận dụng: Hoà tan 8 gam NaOH trong 800ml H2O tính nồng độ mol/l của dung dịch thu được. (0,25M)
c. Khối lượng riêng của dung dịch (D)
- Cho biết một thể tích dung dịch đó (ml, lít, m3, cm3) nặng bao nhêu (gam, kg…)
- Đơn vị: thường dùng g/ml hay g/cm3 ngoài ra kg/m3…
- Đổi đơn vị thể tích 1ml = 1cm3; 1lit = 1 dm3; 1m3 = 1000 lít
- Với mdd là khối lượng dung dịch (g), Vdd là thể tích dung dịch (ml)
- Vd: Ddd HCl = 1,25 g/ml tức là 1ml dung dịch HCl nặng 1,25 gam.
- Vận dụng: 640 ml dung dịch CuSO4 20% có khối lượng 800g. Tính khối lượng riêng của dung dịch CuSO4 (1,25 g/ml).
Chú ý: Khối lượng riêng của H2O là 1g/ml.
d. Mối liên hệ giữa nồng độ % và nồng độ mol/l
e. Nguyên tắc thống kê khối lượng và thể tích dung dịch sau khi pha.
| Hoà tan | Chất rắn vào chất lỏng | Chất khí vào chất lỏng | Chất lỏng vào chất lỏng |
| Khối lượng | mdd = mct + mdm | mdd = mct + mdm | mdd = mct + mdm |
| Thể tích | Vdd = Vdm | Vdd = Vdm | Vdd = Vct + Vdm |
Chú ý: Khi hoà tan có xảy ra phản ứng có chất kết tủa hoặc chất khí thì mdd = mct + mdm – mkết tủa, bay hơi
Bài tập vận dụng
VD1: Hoà tan hoàn toàn 7,45 gam KCl vào 200ml H2O thu được dung dịch A. Tính nồng độ %, nồng độ mol/l của dung dịch A.
VD2: Hoà tan hoàn toàn 0,2 mol NaOH vào 500ml H2O thu được dung dịch B. Tính nồng độ %, nồng độ mol/l của dung dịch B.
VD3: Hoà tan hoàn toàn 2,8 gam KOH và 5,85 gam NaCl vào 600 ml H2O thu được dung dịch C. Tính nồng độ %, nồng độ mol/l của dung dịch C.
VD4: Hoà tan hoàn toàn 4,6 gam Na vào 100 gam H2O thu được dung dịch D. Tính nồng độ %, nồng độ mol/l của dung dịch D.
VD5: Hoà tan hoàn toàn 2,74 gam Ba vào 200 gam H2O thu được dung dịch E. Tính nồng độ %, nồng độ mol/l của dung dịch E.
VD6: Hoà tan hoàn toàn 5,85 gam K và 13,7 gam Ba vào 400ml H2O thu được dung dịch F. Tính nồng độ %, nồng độ mol/l của dung dịch F.
f. Quy tắc đường chéo
Trộn m1 gam dd A nồng độ C1% với m2 gam dd A nồng độ C2% thu được (m1+m2) gam dd A nồng độ C%. (với C1 < C < C2)
 Trộn V1 lít dd A nồng độ C1M với V2 lít dd A nồng độ C2M thu được (V1+V2) lít dd A nồng độ CM. (với C1M < CM < C2M)
Trộn V1 lít dd A nồng độ C1M với V2 lít dd A nồng độ C2M thu được (V1+V2) lít dd A nồng độ CM. (với C1M < CM < C2M)
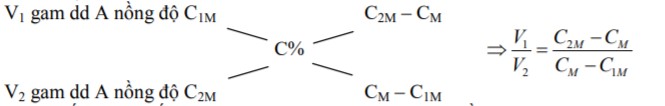
Quy ước: Nếu thêm chất tan thì coi như thêm dung dịch với nồng độ 100%
Nếu thêm dung môi thì coi như thêm dung dịch với nồng độ 0%
Bài tập vận dụng
- VD1: Cần cho bao nhiêu gam muối ăn vào 300g H2O để thu được dung dịch muối ăn 10% (33,33g)
- VD2: Cần bao nhiêu gam đường và bao nhiêu gam nước để pha được 900g dung dịch nước đường 15% (135&765)
- VD3: Cần thêm bao nhiêu gam nước vào 600 g dung dịch NaCl 15% để thu được dung dịch NaCl 8% (525g)
- VD4: Cần trộn bao nhiêu gam dung dịch H2SO4 5% với bao nhiêu gam dung dịch H2SO4 30% để thu được 1800g dung dịch H2SO4 20%.(720&1080)
2.6. Giải bài toán tính theo phương trình phản ứng.
a. Bài toán các chất lấy vừa đủ.
Dấu hiệu: Cho dữ kiện tính được số mol của 1 chất tham gia phản ứng.
Cách làm: Từ số mol chất đã cho tìm ra số mol của chất đề bài hỏi và áp dụng công thức tính số mol tương ứng để trả lời các đại lượng.
VD1: Hoà tan 11,2 gam Fe trong dung dịch axit HCl 1M vừa đủ thu được dung dịch A và V lít khí ở đktc.
- Tính V và khối lượng muối có trong dung dịch A. (4,48lit – 25,4 g)
- Tính thể tích dung dịch HCl đã dùng. (0,4 lit)
- Viết phương trình hóa học xảy ra (nếu có) khi cho dung dịch A tác dụng với các dung dịch NaOH, AgNO3, MgSO4, K2CO3.
VD2: Hoà tan hoàn toàn a gam Mg trong dung dịch H2SO4 0,5M vừa đủ thu được dung dịch B và 3,36 lít khí H2 (đktc).
- Tính a và khối lượng muối tan có trong dung dịch B.
- Tính thể tích dung dịch H2SO4 đã dùng.
- Viết các phương trình hóa học xảy ra (nếu có) khi cho dung dịch D tác dụng với các dung dịch KOH, BaCl2, FeCl3, Na2SO3.
VD3: Để trung hoà 100ml dung dịch axit HCl 1M cần dùng vừa đủ 200ml dung dịch NaOH. Sau phản ứng thu được dung dịch C.
- Tính nồng độ mol/l của dung dịch HCl đã dùng. (0,5M)
- Cô cạn dung dịch C thu được bao nhiêu gam muối khan. (5,85g)
- Dung dịch C tác dụng được với dung dịch nào sau đây: KNO3, H2SO4, AgNO3.
VD4: Hoà tan 0,65 gam Zn trong 100ml dung dịch HCl 0,2M. Tính thể tích khí H2 thoát ra ở 270C, 273 atm và khối lượng muối trong dung dịch thu được sau phản ứng.
b. Bài toán có chất hết chất dư.
Dấu hiệu: Cho dữ kiện tính được số mol của cả 2 chất tham gia phản ứng.
Cách làm: Xét phân số mol của các chất tham gia để chỉ ra chất hết, chất dư. Sản phẩm, số mol các chất phản ứng tính theo chất hết.
Xét phản ứng a A + b B c C + d D
Phân số mol Nếu > => A dư, B hết (sản phẩm tính theo chất B)
VD1: Cho 8,4 gam sắt tác dụng với 3,36 lít khí clo (đktc) tính khối lượng mỗi chất sau phản ứng
(16,25 gam – 2,8 gam)
(tương tự 16,2g Al tác dụng với 6,72 lít O2 (đktc)
VD2: Cho 0,54 gam nhôm tác dụng với 200ml dung dịch HCl 0,4M thu được V lít khí H2 ở đktc và dung dịch X. Tính V và nồng độ mol/l của mỗi chất trong dung dịch X biết thể tích dung dịch X thay đổi không đáng kể so với dung dịch ban đầu. (0,672 lít)
VD3: Tính thể tích khí H2 thu được ở đktc khi cho 10,8 gam nhôm tác dụng với 180g dung dịch H2SO4 24,5% (10,08 lít)
VD4: Trộn 400ml dung dịch BaCl2 5,2% với 100ml dung dịch H2SO4 20% (D=1,12g/ml)
- Tính khối lượng kết tủa bari sunfat thu được (23,3g)
- Tinh số mol các chất trong dung dịch thu được (suy ra nđ% axit dư = 2,6069, muối dư 1,49375, nđ mol/l)
c. Bài toán hỗn hợp, lập hệ phương trình để giải.
Dấu hiệu: Bài toán cho 1 hỗn hợp 2 chất và 2 dữ kiện số liệu.
Cách làm: Gọi x, y là số mol mỗi chất trong hỗn hợp. Lập hệ 2 pt 2 ẩn.
VD1: Hòa tan hết 11 gam hỗn hợp gồm Al, Fe trong dd HCl vừa đủ thu được 8,96 lít (đktc) khí A và dd B.
- Tính số mol của mỗi chất trong hỗn hợp.
b. Tính số mol HCl đã tham gia phản ứng…
VD2: Hòa tan hết 9 gam hỗn hợp gồm Mg, Al trong V lít dd H2SO4 0,5M vừa đủ thu được 10,08 lít (đktc) khí A và dd B.
- Tính phần trăm khối lượng của mỗi chất trong hỗn hợp.
b. Tính V và nồng độ mỗi chất trong dung dịch B
d. Phản ứng xảy ra không hoàn toàn sau phản ứng các chất đều dư.
VD1: Sau khi nung 9,4 gam Cu(NO3)2 ở nhiệt độ cao thu được 6,16 gam chất rắn. Tính thể tích các khí thoát ra ở đktc.
LG: 2Cu(NO3)2 2CuO + 4NO2 + O2
Giả sử Cu(NO3)2 bị nhiệt phân hết => chất rắn sau phản ứng là CuO. nCuO = nCu(NO3)2=0,05 mol => mCR= 4 gam 6,16 gam.
Vậy giả sử là sai, Cu(NO3)2 còn dư sau phản ứng. Chất rắn có CuO, Cu(NO3)2 dư.
Gọi số mol Cu(NO3)2 phản ứng là x. Sau phản ứng nCuO = x, nCu(NO3)2 dư = 0,05 – x.
mCR = mCuO + mCu(NO3)2 = 80x + 188(0,05-x) = 6,16 => x = 0,03
=> VNO2 = ½ x.22,4=0,336 lít , VO2 = 2x.22,4 = 1,344 lít
VD2: Nung nóng một hỗn hợp gồm 0,65 gam bột kẽm và 0,48 gam bột lưu huỳnh sau một thời gian thu được chất rắn A. Cho A tác dụng với dung dịch HCl dư thu được 0,224 lít khí (đktc) và 0,32 gam chất rắn B. Nếu cho chất rắn A ở trên tác dụng hết với dung dịch CuSO4 dư thu được 0,32 gam kim loại màu đỏ và một phần chất rắn không tan. Bỏ qua sự thuỷ phân của muối. Tính hiệu suất phản ứng kẽm và lưu huỳnh.
Link download file pdf ÔN TẬP HÓA HỌC ĐẦU NĂM LỚP 10
Website còn có bài tập trắc nghiệm cho tất cả các chương – chủ đề của cả 3 khối, các thầy cô và các em có thể xem cụ thể từng khối lớp tại các link sau
- Tổng hợp các chuyên đề hóa học lớp 10
- Tổng hợp các chuyên đề hóa học lớp 11
- Tổng hợp các chuyên đề hóa học lớp 12
Hoặc các thầy cô có thể xem các tài liệu khác của website
- Phương pháp tư duy dồn chất xếp hình giải bài tập hóa học hữu cơ
- Tổng hợp bài tâp phương pháp dồn chất xếp hình
- 200 câu lý thuyết đếm hóa học lớp 12 có đáp án ôn thi TN THPT
- Tổng hợp kĩ thuật phương pháp giải bài tập peptit đầy đủ chi tiết
- Tổng hợp bài tập hữu cơ hay và khó có lời giải chi tiết
- Biện luận công thức phân tử muối amoni hữu cơ đầy đủ chi tiết
- Giải bài tập chất béo theo phương pháp dồn chất
- Tổng hợp 50+ bài tập chất béo có lời giải chi tiết
- Tổng hợp bài tập vô cơ hay và khó có lời giải chi tiết
- Tổng hợp đề thi môn hóa của bộ giáo dục từ năm 2007 đến nay
- Tổng hợp các phương pháp giải bài tập môn hoá học
- Tổng hợp giáo án chủ đề STEM trong môn hóa học
- Tổng hợp đề thi THPT QG 2021 file word có lời giải chi tiết
- Tổng hợp đề thi HSG lớp 12 môn hoá học
- Tổng hợp đề thi giữa học kì 1 môn hóa cả 3 khối 10 11 12
- Tổng hợp đề thi học kì 1 lớp 12 môn hóa học
- Tổng hợp đề thi học kì 1 lớp 11 môn hóa học
- Tổng hợp đề thi học kì 1 lớp 10 môn hóa học
- Tổng hợp đề thi giữa học kì 2 cả ba khối 10 11 12
- Tổng hợp đề thi học kì 2 lớp 12 môn hóa học
- Tổng hợp đề thi học kì 2 lớp 11 môn hóa học
- Tổng hợp đề thi học kì 2 lớp 10 môn hoá học

Leave a Reply