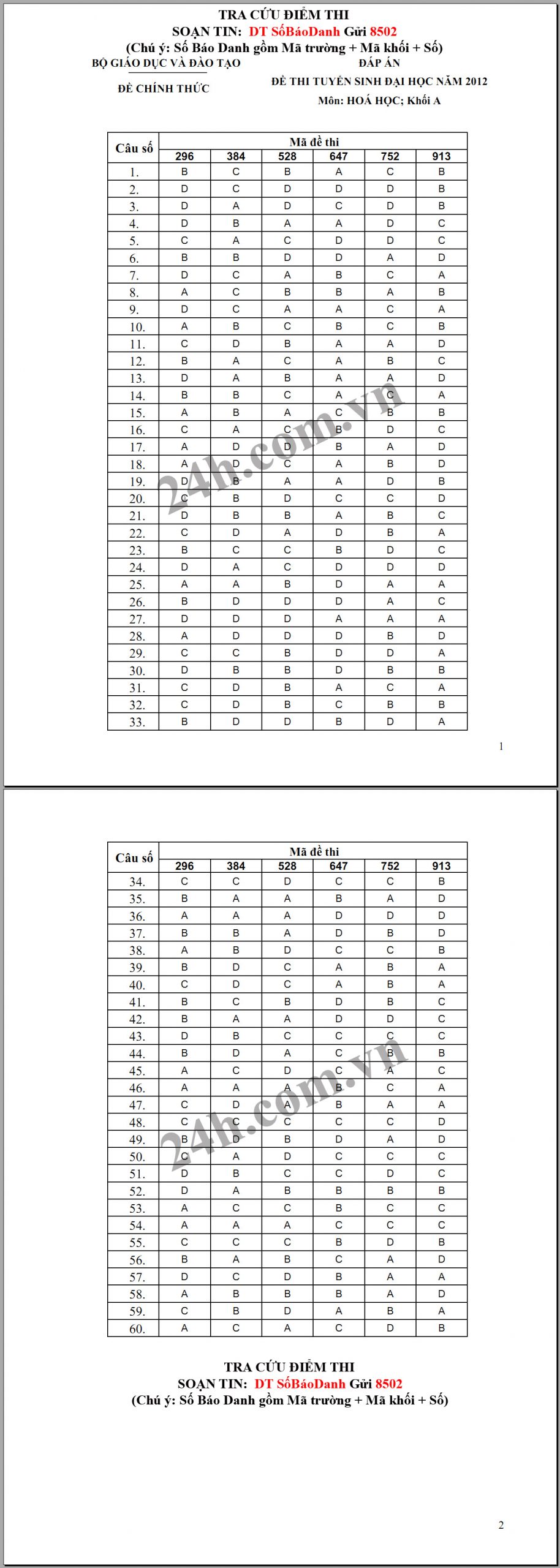
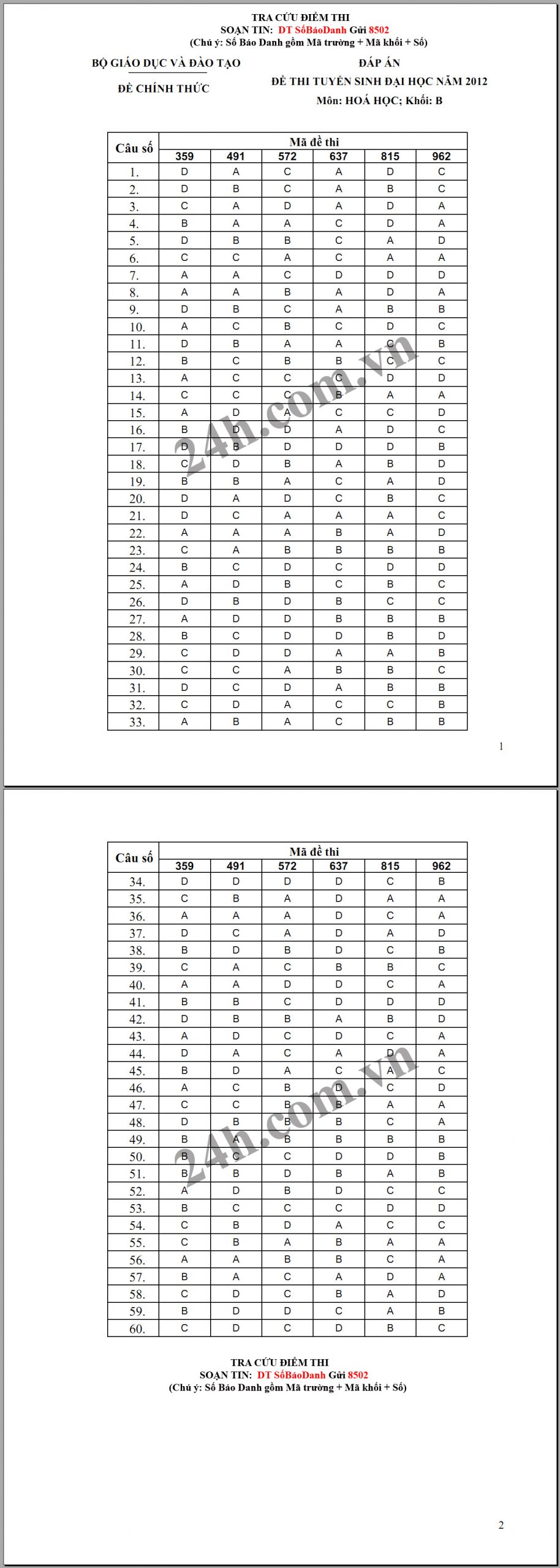
Đề thi đại học khối A B môn hóa học năm 2009 và đáp án chi tiết
BỘ GIÁO DỤC VÀ ĐÀO TẠO
ĐỀ CHÍNH THỨC
(Đề thi có 06 trang) |
ĐỀ THI TUYỂN SINH ĐẠI HỌC NĂM 2009
Môn thi: HOÁ HỌC; Khối: A
Thời gian làm bài: 90 phút, không kể thời gian phát đề. |
| Mã đề thi 596 |
Họ, tên thí sinh:……………………………………………………………..…
Số báo danh:………………………………………………………………….
Cho biết khối lượng nguyên tử (theo đvC) của các nguyên tố:
H = 1; C = 12; N = 14; O = 16; Na = 23; Mg = 24; Al = 27; S = 32; Cl = 35,5; K = 39; Ca = 40;
Cr = 52; Mn = 55; Fe = 56; Cu = 64; Zn = 65; Br = 80; Ag = 108; Sn = 119; Ba = 137; Pb = 207.
I. PHẦN CHUNG CHO TẤT CẢ THÍ SINH (40 câu, từ câu 1 đến câu 40)
Câu 1: Cấu hình electron của ion X2+ là 1s22s22p63s23p63d6. Trong bảng tuần hoàn các nguyên tố hoá
học, nguyên tố X thuộc
A. chu kì 4, nhóm IIA. B. chu kì 4, nhóm VIIIB.
C. chu kì 3, nhóm VIB. D. chu kì 4, nhóm VIIIA.
Câu 2: Cho luồng khí CO (dư) đi qua 9,1 gam hỗn hợp gồm CuO và Al2O3 nung nóng đến khi phản
ứng hoàn toàn, thu được 8,3 gam chất rắn. Khối lượng CuO có trong hỗn hợp ban đầu là
A. 0,8 gam. B. 2,0 gam. C. 4,0 gam. D. 8,3 gam.
Câu 3: Dung dịch X chứa hỗn hợp gồm Na2CO3 1,5M và KHCO3 1M. Nhỏ từ từ từng giọt cho đến
hết 200 ml dung dịch HCl 1M vào 100 ml dung dịch X, sinh ra V lít khí (ở đktc). Giá trị của V là
A. 2,24. B. 4,48. C. 3,36. D. 1,12.
Câu 4: Dãy các kim loại đều có thể được điều chế bằng phương pháp điện phân dung dịch muối của
chúng là:
A. Al, Fe, Cr. B. Mg, Zn, Cu. C. Ba, Ag, Au. D. Fe, Cu, Ag.
Câu 5: Cho hỗn hợp khí X gồm HCHO và H2 đi qua ống sứ đựng bột Ni nung nóng. Sau khi phản ứng
xảy ra hoàn toàn, thu được hỗn hợp khí Y gồm hai chất hữu cơ. Đốt cháy hết Y thì thu được 11,7 gam
H2O và 7,84 lít khí CO2 (ở đktc). Phần trăm theo thể tích của H2 trong X là
A. 46,15%. B. 35,00%. C. 53,85%. D. 65,00%.
Câu 6: Cho các hợp kim sau: Cu-Fe (I); Zn-Fe (II); Fe-C (III); Sn-Fe (IV). Khi tiếp xúc với dung
dịch chất điện li thì các hợp kim mà trong đó Fe đều bị ăn mòn trước là:
A. II, III và IV. B. I, II và IV. C. I, II và III. D. I, III và IV.
Câu 7: Xà phòng hoá một hợp chất có công thức phân tử C10H14O6 trong dung dịch NaOH (dư), thu
được glixerol và hỗn hợp gồm ba muối (không có đồng phân hình học). Công thức của ba muối đó là:
A. CH3-COONa, HCOONa và CH3-CH=CH-COONa.
B. CH2=CH-COONa, CH3-CH2-COONa và HCOONa.
C. HCOONa, CH≡C-COONa và CH3-CH2-COONa.
D. CH2=CH-COONa, HCOONa và CH≡C-COONa.
Câu 8: Lên men m gam glucozơ với hiệu suất 90%, lượng khí CO2 sinh ra hấp thụ hết vào dung dịch
nước vôi trong, thu được 10 gam kết tủa. Khối lượng dung dịch sau phản ứng giảm 3,4 gam so với
khối lượng dung dịch nước vôi trong ban đầu. Giá trị của m là
A. 20,0. B. 30,0. C. 13,5. D. 15,0.
Câu 9: Thuốc thử được dùng để phân biệt Gly-Ala-Gly với Gly-Ala là
A. dung dịch HCl. B. Cu(OH)2 trong môi trường kiềm.
C. dung dịch NaCl. D. dung dịch NaOH.
Câu 10: Cho hỗn hợp gồm Fe và Zn vào dung dịch AgNO3 đến khi các phản ứng xảy ra hoàn toàn,
thu được dung dịch X gồm hai muối và chất rắn Y gồm hai kim loại. Hai muối trong X là
A. Zn(NO3)2 và Fe(NO3)2. B. AgNO3 và Zn(NO3)2.
C. Fe(NO3)2 và AgNO3. D. Fe(NO3)3 và Zn(NO3)2.
Trang 1/6 – Mã đề thi 596
Câu 11: Có ba dung dịch: amoni hiđrocacbonat, natri aluminat, natri phenolat và ba chất lỏng: ancol
etylic, benzen, anilin đựng trong sáu ống nghiệm riêng biệt. Nếu chỉ dùng một thuốc thử duy nhất là dung
dịch HCl thì nhận biết được tối đa bao nhiêu ống nghiệm?
A. 4. B. 5. C. 3. D. 6.
Câu 12: Cho 0,448 lít khí CO2 (ở đktc) hấp thụ hết vào 100 ml dung dịch chứa hỗn hợp NaOH
0,06M và Ba(OH)2 0,12M, thu được m gam kết tủa. Giá trị của m là
A. 1,182. B. 3,940. C. 2,364. D. 1,970.
Câu 13: Nếu cho 1 mol mỗi chất: CaOCl2, KMnO4, K2Cr2O7, MnO2 lần lượt phản ứng với lượng dư
dung dịch HCl đặc, chất tạo ra lượng khí Cl2 nhiều nhất là
A. K2Cr2O7. B. MnO2. C. KMnO4. D. CaOCl2.
Câu 14: Cho 10 gam amin đơn chức X phản ứng hoàn toàn với HCl (dư), thu được 15 gam muối. Số
đồng phân cấu tạo của X là
A. 5. B. 8. C. 7. D. 4.
Câu 15: Xà phòng hóa hoàn toàn 66,6 gam hỗn hợp hai este HCOOC2H5 và CH3COOCH3 bằng dung
dịch NaOH, thu được hỗn hợp X gồm hai ancol. Đun nóng hỗn hợp X với H2SO4 đặc ở 140 oC, sau
khi phản ứng xảy ra hoàn toàn thu được m gam nước. Giá trị của m là
A. 18,00. B. 8,10. C. 16,20. D. 4,05.
Câu 16: Hợp chất hữu cơ X tác dụng được với dung dịch NaOH và dung dịch brom nhưng không tác
dụng với dung dịch NaHCO3. Tên gọi của X là
A. axit acrylic. B. anilin. C. metyl axetat. D. phenol.
Câu 17: Xà phòng hoá hoàn toàn 1,99 gam hỗn hợp hai este bằng dung dịch NaOH thu được 2,05 gam
muối của một axit cacboxylic và 0,94 gam hỗn hợp hai ancol là đồng đẳng kế tiếp nhau. Công thức của
hai este đó là
A. HCOOCH3 và HCOOC2H5. B. CH3COOC2H5 và CH3COOC3H7.
C. C2H5COOCH3 và C2H5COOC2H5. D. CH3COOCH3 và CH3COOC2H5.
Câu 18: Dãy gồm các chất đều tác dụng được với dung dịch HCl loãng là:
A. AgNO3, (NH4)2CO3, CuS. B. FeS, BaSO4, KOH.
C. Mg(HCO3)2, HCOONa, CuO. D. KNO3, CaCO3, Fe(OH)3.
Câu 19: Poli(metyl metacrylat) và nilon-6 được tạo thành từ các monome tương ứng là
A. CH3-COO-CH=CH2 và H2N-[CH2]5-COOH.
B. CH2=C(CH3)-COOCH3 và H2N-[CH2]6-COOH.
C. CH2=C(CH3)-COOCH3 và H2N-[CH2]5-COOH.
D. CH2=CH-COOCH3 và H2N-[CH2]6-COOH.
Câu 20: Cho 0,25 mol một anđehit mạch hở X phản ứng với lượng dư dung dịch AgNO3 trong NH3,
thu được 54 gam Ag. Mặt khác, khi cho X phản ứng với H2 dư (xúc tác Ni, to) thì 0,125 mol X phản
ứng hết với 0,25 mol H2. Chất X có công thức ứng với công thức chung là
A. CnH2n-3CHO (n ≥ 2). B. CnH2n+1CHO (n ≥0).
C. CnH2n-1CHO (n ≥ 2). D. CnH2n(CHO)2 (n ≥ 0).
Câu 21: Cho hỗn hợp gồm 1,12 gam Fe và 1,92 gam Cu vào 400 ml dung dịch chứa hỗn hợp gồm
H2SO4 0,5M và NaNO3 0,2M. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch X và khí
NO (sản phẩm khử duy nhất). Cho V ml dung dịch NaOH 1M vào dung dịch X thì lượng kết tủa thu
được là lớn nhất. Giá trị tối thiểu của V là
A. 120. B. 400. C. 360. D. 240.
Câu 22: Khi đốt cháy hoàn toàn m gam hỗn hợp hai ancol no, đơn chức, mạch hở thu được V lít khí
CO2 (ở đktc) và a gam H2O. Biểu thức liên hệ giữa m, a và V là:
A. m = 2a – V
22,4
. B. m = 2a – V
11,2
. C. m = a – V
5,6
. D. m = a + V
5,6
.
Câu 23: Một hợp chất X chứa ba nguyên tố C, H, O có tỉ lệ khối lượng mC : mH : mO = 21 : 2 : 4.
Hợp chất X có công thức đơn giản nhất trùng với công thức phân tử. Số đồng phân cấu tạo thuộc loại
hợp chất thơm ứng với công thức phân tử của X là
A. 5. B. 3. C. 4. D. 6.
Trang 2/6 – Mã đề thi 596
Câu 24: Dãy gồm các chất đều điều chế trực tiếp (bằng một phản ứng) tạo ra anđehit axetic là:
A. C2H5OH, C2H2, CH3COOC2H5. B. CH3COOH, C2H2, C2H4.
C. C2H5OH, C2H4, C2H2. D. HCOOC2H3, C2H2, CH3COOH.
Câu 25: Cho 3,024 gam một kim loại M tan hết trong dung dịch HNO3 loãng, thu được 940,8 ml khí
NxOy (sản phẩm khử duy nhất, ở đktc) có tỉ khối đối với H2 bằng 22. Khí NxOy và kim loại M là
A. NO2 và Al. B. N2O và Al. C. NO và Mg. D. N2O và Fe.
Câu 26: Hiđrocacbon X không làm mất màu dung dịch brom ở nhiệt độ thường. Tên gọi của X là
A. xiclohexan. B. xiclopropan. C. etilen. D. stiren.
Câu 27: Nung 6,58 gam Cu(NO3)2 trong bình kín không chứa không khí, sau một thời gian thu được
4,96 gam chất rắn và hỗn hợp khí X. Hấp thụ hoàn toàn X vào nước để được 300 ml dung dịch Y.
Dung dịch Y có pH bằng
A. 3. B. 1. C. 4. D. 2.
Câu 28: Cho 6,72 gam Fe vào 400 ml dung dịch HNO3 1M, đến khi phản ứng xảy ra hoàn toàn, thu
được khí NO (sản phẩm khử duy nhất) và dung dịch X. Dung dịch X có thể hoà tan tối đa m gam Cu.
Giá trị của m là
A. 3,84. B. 1,92. C. 0,64. D. 3,20.
Câu 29: Cho bốn hỗn hợp, mỗi hỗn hợp gồm hai chất rắn có số mol bằng nhau: Na2O và Al2O3; Cu
và FeCl3; BaCl2 và CuSO4; Ba và NaHCO3. Số hỗn hợp có thể tan hoàn toàn trong nước (dư) chỉ tạo
ra dung dịch là
A. 1. B. 3. C. 2. D. 4.
Câu 30: Cho 3,68 gam hỗn hợp gồm Al và Zn tác dụng với một lượng vừa đủ dung dịch H2SO4 10%,
thu được 2,24 lít khí H2 (ở đktc). Khối lượng dung dịch thu được sau phản ứng là
A. 101,48 gam. B. 101,68 gam. C. 88,20 gam. D. 97,80 gam.
Câu 31: Cho dãy các chất và ion: Zn, S, FeO, SO2, N2, HCl, Cu2+, Cl–. Số chất và ion có cả tính oxi
hóa và tính khử là
A. 7. B. 5. C. 4. D. 6.
Câu 32: Hỗn hợp khí X gồm anken M và ankin N có cùng số nguyên tử cacbon trong phân tử. Hỗn
hợp X có khối lượng 12,4 gam và thể tích 6,72 lít (ở đktc). Số mol, công thức phân tử của M và N lần
lượt là
A. 0,2 mol C2H4 và 0,1 mol C2H2. B. 0,2 mol C3H6 và 0,1 mol C3H4.
C. 0,1 mol C2H4 và 0,2 mol C2H2. D. 0,1 mol C3H6 và 0,2 mol C3H4.
Câu 33: Nguyên tử của nguyên tố X có cấu hình electron lớp ngoài cùng là ns2np4. Trong hợp chất
khí của nguyên tố X với hiđro, X chiếm 94,12% khối lượng. Phần trăm khối lượng của nguyên tố X
trong oxit cao nhất là
A. 60,00%. B. 27,27%. C. 50,00%. D. 40,00%.
Câu 34: Cho phương trình hoá học: Fe3O4 + HNO3 → Fe(NO3)3 + NxOy + H2O
Sau khi cân bằng phương trình hoá học trên với hệ số của các chất là những số nguyên, tối giản thì
hệ số của HNO3 là
A. 23x – 9y. B. 45x – 18y. C. 46x – 18y. D. 13x – 9y.
Câu 35: Đun nóng hỗn hợp hai ancol đơn chức, mạch hở với H2SO4 đặc, thu được hỗn hợp gồm các
ete. Lấy 7,2 gam một trong các ete đó đem đốt cháy hoàn toàn, thu được 8,96 lít khí CO2 (ở đktc) và
7,2 gam H2O. Hai ancol đó là
A. CH3OH và CH2=CH-CH2-OH. B. CH3OH và C3H7OH.
C. C2H5OH và CH2=CH-CH2-OH. D. C2H5OH và CH3OH.
Câu 36: Trường hợp nào sau đây không xảy ra phản ứng hoá học?
A. Sục khí H2S vào dung dịch FeCl2. B. Sục khí Cl2 vào dung dịch FeCl2.
C. Sục khí H2S vào dung dịch CuCl2. D. Cho Fe vào dung dịch H2SO4 loãng, nguội.
Câu 37: Hoà tan hoàn toàn 12,42 gam Al bằng dung dịch HNO3 loãng (dư), thu được dung dịch X và
1,344 lít (ở đktc) hỗn hợp khí Y gồm hai khí là N2O và N2. Tỉ khối của hỗn hợp khí Y so với khí H2
là 18. Cô cạn dung dịch X, thu được m gam chất rắn khan. Giá trị của m là
A. 34,08. B. 38,34. C. 97,98. D. 106,38.
Trang 3/6 – Mã đề thi 596
Câu 38: Cho 1 mol amino axit X phản ứng với dung dịch HCl (dư), thu được m1 gam muối Y. Cũng 1 mol
amino axit X phản ứng với dung dịch NaOH (dư), thu được m2 gam muối Z. Biết m2 – m1 = 7,5. Công thức
phân tử của X là
A. C4H10O2N2. B. C4H8O4N2. C. C5H9O4N. D. C5H11O2N.
Câu 39: Hoà tan hết m gam ZnSO4 vào nước được dung dịch X. Cho 110 ml dung dịch KOH 2M vào X,
thu được a gam kết tủa. Mặt khác, nếu cho 140 ml dung dịch KOH 2M vào X thì cũng thu được a gam kết
tủa. Giá trị của m là
A. 20,125. B. 12,375. C. 22,540. D. 17,710.
Câu 40: Cho hỗn hợp X gồm hai ancol đa chức, mạch hở, thuộc cùng dãy đồng đẳng. Đốt cháy hoàn
toàn hỗn hợp X, thu được CO2 và H2O có tỉ lệ mol tương ứng là 3 : 4. Hai ancol đó là
A. C2H5OH và C4H9OH. B. C2H4(OH)2 và C3H6(OH)2.
C. C2H4(OH)2 và C4H8(OH)2. D. C3H5(OH)3 và C4H7(OH)3.
_________________________________________________________________________________
II. PHẦN RIÊNG [10 câu]
Thí sinh chỉ được làm một trong hai phần (phần A hoặc B)
A. Theo chương trình Chuẩn (10 câu, từ câu 41 đến câu 50)
Câu 41: Cho các hợp chất hữu cơ: C2H2; C2H4; CH2O; CH2O2 (mạch hở); C3H4O2 (mạch hở, đơn
chức). Biết C3H4O2 không làm chuyển màu quỳ tím ẩm. Số chất tác dụng được với dung dịch AgNO3
trong NH3 tạo ra kết tủa là
A. 2. B. 5. C. 3. D. 4.
Câu 42: Cho cân bằng sau trong bình kín: 2NO2 (k) YZZ ZZX N2O4 (k).
(màu nâu đỏ) (không màu) |
Biết khi hạ nhiệt độ của bình thì màu nâu đỏ nhạt dần. Phản ứng thuận có
A. Δ H < 0, phản ứng tỏa nhiệt. B. Δ H > 0, phản ứng thu nhiệt.
C. Δ H > 0, phản ứng tỏa nhiệt. D. Δ H < 0, phản ứng thu nhiệt.
Câu 43: Hợp chất X mạch hở có công thức phân tử là C4H9NO2. Cho 10,3 gam X phản ứng vừa đủ
với dung dịch NaOH sinh ra một chất khí Y và dung dịch Z. Khí Y nặng hơn không khí, làm giấy quỳ
tím ẩm chuyển màu xanh. Dung dịch Z có khả năng làm mất màu nước brom. Cô cạn dung dịch Z thu
được m gam muối khan. Giá trị của m là
A. 10,8. B. 8,2. C. 9,4. D. 9,6.
Câu 44: Cacbohiđrat nhất thiết phải chứa nhóm chức của
A. amin. B. anđehit. C. xeton. D. ancol.
Câu 45: Cho hỗn hợp X gồm hai axit cacboxylic no, mạch không phân nhánh. Đốt cháy hoàn toàn 0,3 mol
hỗn hợp X, thu được 11,2 lít khí CO2 (ở đktc). Nếu trung hòa 0,3 mol X thì cần dùng 500 ml dung dịch
NaOH 1M. Hai axit đó là:
A. HCOOH, HOOC-CH2-COOH. B. HCOOH, HOOC-COOH.
C. HCOOH, C2H5COOH.
Câu 46: Phát biểu nào sau đây là đúng? |
D. HCOOH, CH3COOH. |
A. Amophot là hỗn hợp các muối (NH4)2HPO4 và KNO3.
B. Phân lân cung cấp nitơ hoá hợp cho cây dưới dạng ion nitrat (NO3-) và ion amoni (NH4+).
C. Phân hỗn hợp chứa nitơ, photpho, kali được gọi chung là phân NPK.
D. Phân urê có công thức là (NH4)2CO3.
Câu 47: Hoà tan hoàn toàn 14,6 gam hỗn hợp X gồm Al và Sn bằng dung dịch HCl (dư), thu được 5,6 lít
khí H2 (ở đktc). Thể tích khí O2 (ở đktc) cần để phản ứng hoàn toàn với 14,6 gam hỗn hợp X là
A. 1,68 lít. B. 3,92 lít. C. 4,48 lít. D. 2,80 lít.
Câu 48: Đốt cháy hoàn toàn 0,2 mol một ancol X no, mạch hở cần vừa đủ 17,92 lít khí O2 (ở đktc).
Mặt khác, nếu cho 0,1 mol X tác dụng vừa đủ với m gam Cu(OH)2 thì tạo thành dung dịch có màu
xanh lam. Giá trị của m và tên gọi của X tương ứng là
A. 4,9 và glixerol. B. 4,9 và propan-1,3-điol.
C. 9,8 và propan-1,2-điol. D. 4,9 và propan-1,2-điol.
Trang 4/6 – Mã đề thi 596
Câu 49: Cho hỗn hợp gồm 1,2 mol Mg và x mol Zn vào dung dịch chứa 2 mol Cu2+ và 1 mol Ag+
đến khi các phản ứng xảy ra hoàn toàn, thu được một dung dịch chứa ba ion kim loại. Trong các giá
trị sau đây, giá trị nào của x thoả mãn trường hợp trên?
A. 1,5. B. 1,8. C. 1,2. D. 2,0.
Câu 50: Có năm dung dịch đựng riêng biệt trong năm ống nghiệm: (NH4)2SO4, FeCl2, Cr(NO3)3,
K2CO3, Al(NO3)3. Cho dung dịch Ba(OH)2 đến dư vào năm dung dịch trên. Sau khi phản ứng kết
thúc, số ống nghiệm có kết tủa là
A. 3. B. 2. C. 5. D. 4.
B. Theo chương trình Nâng cao (10 câu, từ câu 51 đến câu 60)
Câu 51: Phát biểu nào sau đây là đúng?
A. Các ancol đa chức đều phản ứng với Cu(OH)2 tạo dung dịch màu xanh lam.
B. Anilin tác dụng với axit nitrơ khi đun nóng, thu được muối điazoni.
C. Etylamin phản ứng với axit nitrơ ở nhiệt độ thường, sinh ra bọt khí.
D. Benzen làm mất màu nước brom ở nhiệt độ thường.
Câu 52: Cho dãy chuyển hoá sau:
Phenol ⎯+⎯⎯ X→ Phenyl axetat ⎯⎯⎯⎯⎯⎯ + NaOH (d to -)→ Y (hợp chất thơm)
Hai chất X, Y trong sơ đồ trên lần lượt là:
A. anhiđrit axetic, natri phenolat. B. axit axetic, phenol.
C. anhiđrit axetic, phenol. D. axit axetic, natri phenolat.
Câu 53: Dãy gồm các dung dịch đều tham gia phản ứng tráng bạc là:
A. Glucozơ, glixerol, mantozơ, axit fomic.
B. Fructozơ, mantozơ, glixerol, anđehit axetic.
C. Glucozơ, mantozơ, axit fomic, anđehit axetic.
D. Glucozơ, fructozơ, mantozơ, saccarozơ.
Câu 54: Một bình phản ứng có dung tích không đổi, chứa hỗn hợp khí N2 và H2 với nồng độ tương
ứng là 0,3M và 0,7M. Sau khi phản ứng tổng hợp NH3 đạt trạng thái cân bằng ở t oC, H2 chiếm 50%
thể tích hỗn hợp thu được. Hằng số cân bằng KC ở t oC của phản ứng có giá trị là
A. 0,500. B. 3,125. C. 0,609. D. 2,500.
Câu 55: Nung nóng m gam PbS ngoài không khí sau một thời gian, thu được hỗn hợp rắn (có chứa
một oxit) nặng 0,95m gam. Phần trăm khối lượng PbS đã bị đốt cháy là
A. 74,69%. B. 95,00%. C. 64,68%. D. 25,31%.
Câu 56: Dãy gồm các chất và thuốc đều có thể gây nghiện cho con người là
A. cocain, seduxen, cafein. B. heroin, seduxen, erythromixin.
C. penixilin, paradol, cocain. D. ampixilin, erythromixin, cafein.
Câu 57: Chất hữu cơ X có công thức phân tử C5H8O2. Cho 5 gam X tác dụng vừa hết với dung dịch
NaOH, thu được một hợp chất hữu cơ không làm mất màu nước brom và 3,4 gam một muối. Công
thức của X là
A. CH3COOC(CH3)=CH2. B. HCOOCH=CHCH2CH3.
C. HCOOCH2CH=CHCH3.
Câu 58: Trường hợp xảy ra phản ứng là |
D. HCOOC(CH3)=CHCH3. |
A. Cu + H2SO4 (loãng) → B. Cu + HCl (loãng) + O2 →
| C. Cu + Pb(NO3)2 (loãng) → |
D. Cu + HCl (loãng) → |
| Câu 59: Cho suất điện động chuẩn của các pin điện hoá: Zn-Cu là 1,1V; Cu-Ag là 0,46V. Biết thế |
điện cực chuẩn o +
E = +0,8 Ag Ag V. Thế điện cực chuẩn |
EoCu Cu 2+ có giá trị lần lượt là |
EoZn Zn 2+ và A. -1,56V và +0,64V. B. -0,76V và +0,34V. C. -1,46V và -0,34V. D. +1,56V và +0,64V.
Trang 5/6 – Mã đề thi 596
Câu 60: Cho sơ đồ chuyển hóa:
CH3CH2Cl ⎯⎯⎯ KCN→X H O 3o +
⎯⎯⎯→ t Y
Công thức cấu tạo của X, Y lần lượt là:
A. CH3CH2CN, CH3CH2CHO. B. CH3CH2NH2, CH3CH2COOH.
C. CH3CH2CN, CH3CH2COONH4. D. CH3CH2CN, CH3CH2COOH.
———————————————————- HẾT ———-
Trang 6/6 – Mã đề thi 596
BỘ GIÁO DỤC VÀ ĐÀO TẠO
ĐỀ CHÍNH THỨC
(Đề thi có 06 trang) |
ĐỀ THI TUYỂN SINH ĐẠI HỌC NĂM 2009
Môn: HOÁ HỌC; Khối: B
Thời gian làm bài: 90 phút, không kể thời gian phát đề |
| Mã đề thi 148 |
Họ, tên thí sinh:……………………………………………………………..…
Số báo danh:………………………………………………………………….
Cho biết khối lượng nguyên tử (theo đvC) của các nguyên tố:
H = 1; C = 12; N = 14; O = 16; F = 19; Na = 23; Mg = 24; Al = 27; P =31; S = 32; Cl = 35,5; K = 39;
Ca = 40; Mn = 55; Fe = 56; Cu = 64; Zn = 65; Br = 80; Ag = 108; I = 127; Ba = 137; Au = 197.
I. PHẦN CHUNG CHO TẤT CẢ THÍ SINH (40 câu, từ câu 1 đến câu 40)
Câu 1: Khi cho a mol một hợp chất hữu cơ X (chứa C, H, O) phản ứng hoàn toàn với Na hoặc với
NaHCO3 thì đều sinh ra a mol khí. Chất X là
A. etylen glicol. B. axit ađipic.
C. ancol o-hiđroxibenzylic. D. axit 3-hiđroxipropanoic.
Câu 2: Điện phân có màng ngăn 500 ml dung dịch chứa hỗn hợp gồm CuCl2 0,1M và NaCl 0,5M
(điện cực trơ, hiệu suất điện phân 100%) với cường độ dòng điện 5A trong 3860 giây. Dung dịch thu
được sau điện phân có khả năng hoà tan m gam Al. Giá trị lớn nhất của m là
A. 4,05. B. 2,70. C. 1,35. D. 5,40.
Câu 3: Cho các nguyên tố: K (Z = 19), N (Z = 7), Si (Z = 14), Mg (Z = 12). Dãy gồm các nguyên tố
được sắp xếp theo chiều giảm dần bán kính nguyên tử từ trái sang phải là:
A. N, Si, Mg, K. B. K, Mg, Si, N. C. K, Mg, N, Si. D. Mg, K, Si, N.
Câu 4: Hoà tan m gam hỗn hợp gồm Al, Fe vào dung dịch H2SO4 loãng (dư). Sau khi các phản ứng
xảy ra hoàn toàn, thu được dung dịch X. Cho dung dịch Ba(OH)2 (dư) vào dung dịch X, thu được kết
tủa Y. Nung Y trong không khí đến khối lượng không đổi, thu được chất rắn Z là
A. hỗn hợp gồm BaSO4 và FeO. B. hỗn hợp gồm Al2O3 và Fe2O3.
C. hỗn hợp gồm BaSO4 và Fe2O3. D. Fe2O3.
Câu 5: Cho 2,24 gam bột sắt vào 200 ml dung dịch chứa hỗn hợp gồm AgNO3 0,1M và Cu(NO3)2
0,5M. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch X và m gam chất rắn Y. Giá trị của
m là
A. 2,80. B. 2,16. C. 4,08. D. 0,64.
Câu 6: Trộn 100 ml dung dịch hỗn hợp gồm H2SO4 0,05M và HCl 0,1M với 100 ml dung dịch hỗn
hợp gồm NaOH 0,2M và Ba(OH)2 0,1M, thu được dung dịch X. Dung dịch X có pH là
A. 13,0. B. 1,2. C. 1,0. D. 12,8.
Câu 7: Khi nhiệt phân hoàn toàn 100 gam mỗi chất sau: KClO3 (xúc tác MnO2), KMnO4, KNO3 và
AgNO3. Chất tạo ra lượng O2 lớn nhất là
A. KClO3. B. KMnO4. C. KNO3. D. AgNO3.
Câu 8: Cho chất xúc tác MnO2 vào 100 ml dung dịch H2O2, sau 60 giây thu được 33,6 ml khí O2 (ở
đktc). Tốc độ trung bình của phản ứng (tính theo H2O2) trong 60 giây trên là
A. 5,0.10 mol/(l.s). –4 B. 5,0.10 mol/(l.s). –5 C. 1,0.10 mol/(l.s). –3 D. 2,5.10 mol/(l.s). –4
Câu 9: Điện phân nóng chảy Al2O3 với anot than chì (hiệu suất điện phân 100%) thu được m kg Al ở
catot và 67,2 m3 (ở đktc) hỗn hợp khí X có tỉ khối so với hiđro bằng 16. Lấy 2,24 lít (ở đktc) hỗn hợp
khí X sục vào dung dịch nước vôi trong (dư) thu được 2 gam kết tủa. Giá trị của m là
A. 108,0. B. 75,6. C. 54,0. D. 67,5.
Câu 10: Hỗn hợp X gồm hai este no, đơn chức, mạch hở. Đốt cháy hoàn toàn một lượng X cần dùng
vừa đủ 3,976 lít khí O2 (ở đktc), thu được 6,38 gam CO2. Mặt khác, X tác dụng với dung dịch NaOH,
thu được một muối và hai ancol là đồng đẳng kế tiếp. Công thức phân tử của hai este trong X là
A. C2H4O2 và C5H10O2. B. C2H4O2 và C3H6O2.
C. C3H4O2 và C4H6O2. D. C3H6O2 và C4H8O2.
Trang 1/6 – Mã đề thi 148
Câu 11: Khi nhiệt phân hoàn toàn từng muối X, Y thì đều tạo ra số mol khí nhỏ hơn số mol muối
tương ứng. Đốt một lượng nhỏ tinh thể Y trên đèn khí không màu, thấy ngọn lửa có màu vàng. Hai
muối X, Y lần lượt là:
A. KMnO4, NaNO3. B. Cu(NO3)2, NaNO3. C. CaCO3, NaNO3. D. NaNO3, KNO3.
Câu 12: Có các thí nghiệm sau:
(I) Nhúng thanh sắt vào dung dịch H2SO4 loãng, nguội.
(II) Sục khí SO2 vào nước brom.
(III) Sục khí CO2 vào nước Gia-ven.
(IV) Nhúng lá nhôm vào dung dịch H2SO4 đặc, nguội.
Số thí nghiệm xảy ra phản ứng hoá học là
A. 2. B. 1. C. 3. D. 4.
Câu 13: Cho hỗn hợp X gồm hai hợp chất hữu cơ no, đơn chức tác dụng vừa đủ với 100 ml dung
dịch KOH 0,4M, thu được một muối và 336 ml hơi một ancol (ở đktc). Nếu đốt cháy hoàn toàn lượng
hỗn hợp X trên, sau đó hấp thụ hết sản phẩm cháy vào bình đựng dung dịch Ca(OH)2 (dư) thì khối
lượng bình tăng 6,82 gam. Công thức của hai hợp chất hữu cơ trong X là
A. CH3COOH và CH3COOC2H5. B. C2H5COOH và C2H5COOCH3.
C. HCOOH và HCOOC2H5. D. HCOOH và HCOOC3H7.
Câu 14: Cho 0,02 mol amino axit X tác dụng vừa đủ với 200 ml dung dịch HCl 0,1M thu được 3,67 gam
muối khan. Mặt khác 0,02 mol X tác dụng vừa đủ với 40 gam dung dịch NaOH 4%. Công thức của X
là
A. H2NC2H3(COOH)2. B. H2NC3H5(COOH)2. C. (H2N)2C3H5COOH. D. H2NC3H6COOH.
Câu 15: Cho hai hợp chất hữu cơ X, Y có cùng công thức phân tử là C3H7NO2. Khi phản ứng với
dung dịch NaOH, X tạo ra H2NCH2COONa và chất hữu cơ Z; còn Y tạo ra CH2=CHCOONa và khí
T. Các chất Z và T lần lượt là
A. CH3OH và NH3. B. CH3OH và CH3NH2.
C. CH3NH2 và NH3.
Câu 16: Cho các phản ứng sau: |
D. C2H5OH và N2. |
(a) 4HCl + PbO2 → PbCl2 + Cl2 + 2H2O.
(b) HCl + NH4HCO3 → NH4Cl + CO2 + H2O.
(c) 2HCl + 2HNO3 → 2NO2 + Cl2 + 2H2O.
(d) 2HCl + Zn → ZnCl2 + H2.
Số phản ứng trong đó HCl thể hiện tính khử là
A. 2. B. 3. C. 1. D. 4.
Câu 17: Hợp chất hữu cơ X tác dụng được với dung dịch NaOH đun nóng và với dung dịch AgNO3
trong NH3. Thể tích của 3,7 gam hơi chất X bằng thể tích của 1,6 gam khí O2 (cùng điều kiện về nhiệt
độ và áp suất). Khi đốt cháy hoàn toàn 1 gam X thì thể tích khí CO2 thu được vượt quá 0,7 lít (ở
đktc). Công thức cấu tạo của X là
A. O=CH-CH2-CH2OH. B. HOOC-CHO.
C. CH3COOCH3. D. HCOOC2H5.
Câu 18: Số đipeptit tối đa có thể tạo ra từ một hỗn hợp gồm alanin và glyxin là
A. 3. B. 1. C. 2. D. 4.
Câu 19: Hỗn hợp khí X gồm H2 và một anken có khả năng cộng HBr cho sản phẩm hữu cơ duy nhất.
Tỉ khối của X so với H2 bằng 9,1. Đun nóng X có xúc tác Ni, sau khi phản ứng xảy ra hoàn toàn, thu
được hỗn hợp khí Y không làm mất màu nước brom; tỉ khối của Y so với H2 bằng 13. Công thức cấu
tạo của anken là
A. CH2=C(CH3)2. B. CH2=CH2.
C. CH2=CH-CH2-CH3. D. CH3-CH=CH-CH3.
Câu 20: Nung nóng m gam hỗn hợp gồm Al và Fe3O4 trong điều kiện không có không khí. Sau khi
phản ứng xảy ra hoàn toàn, thu được hỗn hợp rắn X. Cho X tác dụng với dung dịch NaOH (dư) thu
được dung dịch Y, chất rắn Z và 3,36 lít khí H2 (ở đktc). Sục khí CO2 (dư) vào dung dịch Y, thu được
39 gam kết tủa. Giá trị của m là
Trang 2/6 – Mã đề thi 148
A. 45,6. B. 48,3. C. 36,7. D. 57,0.
Câu 21: Hoà tan hoàn toàn 2,9 gam hỗn hợp gồm kim loại M và oxit của nó vào nước, thu được 500 ml
dung dịch chứa một chất tan có nồng độ 0,04M và 0,224 lít khí H2 (ở đktc). Kim loại M là
A. Na. B. Ca. C. Ba. D. K.
Câu 22: Cho các hợp chất hữu cơ:
(1) ankan; (2) ancol no, đơn chức, mạch hở;
(3) xicloankan; (4) ete no, đơn chức, mạch hở;
(5) anken; (6) ancol không no (có một liên kết đôi C=C), mạch hở;
(7) ankin; (8) anđehit no, đơn chức, mạch hở;
(9) axit no, đơn chức, mạch hở; (10) axit không no (có một liên kết đôi C=C), đơn chức.
Dãy gồm các chất khi đốt cháy hoàn toàn đều cho số mol CO2 bằng số mol H2O là:
A. (1), (3), (5), (6), (8). B. (3), (4), (6), (7), (10).
C. (3), (5), (6), (8), (9). D. (2), (3), (5), (7), (9).
Câu 23: Dãy gồm các chất đều có khả năng tham gia phản ứng trùng hợp là:
A. stiren; clobenzen; isopren; but-1-en.
B. 1,2-điclopropan; vinylaxetilen; vinylbenzen; toluen.
C. buta-1,3-đien; cumen; etilen; trans-but-2-en.
D. 1,1,2,2-tetrafloeten; propilen; stiren; vinyl clorua.
Câu 24: Cho dung dịch chứa 6,03 gam hỗn hợp gồm hai muối NaX và NaY (X, Y là hai nguyên tố có
trong tự nhiên, ở hai chu kì liên tiếp thuộc nhóm VIIA, số hiệu nguyên tử ZX < ZY) vào dung dịch AgNO3
(dư), thu được 8,61 gam kết tủa. Phần trăm khối lượng của NaX trong hỗn hợp ban đầu là
A. 58,2%. B. 41,8%. C. 52,8%. D. 47,2%.
Câu 25: Cho 61,2 gam hỗn hợp X gồm Cu và Fe3O4 tác dụng với dung dịch HNO3 loãng, đun nóng
và khuấy đều. Sau khi các phản ứng xảy ra hoàn toàn, thu được 3,36 lít khí NO (sản phẩm khử duy
nhất, ở đktc), dung dịch Y và còn lại 2,4 gam kim loại. Cô cạn dung dịch Y, thu được m gam muối
khan. Giá trị của m là
A. 151,5. B. 137,1. C. 97,5. D. 108,9.
Câu 26: Thực hiện các thí nghiệm sau:
(I) Cho dung dịch NaCl vào dung dịch KOH.
(II) Cho dung dịch Na2CO3 vào dung dịch Ca(OH)2.
(III) Điện phân dung dịch NaCl với điện cực trơ, có màng ngăn.
(IV) Cho Cu(OH)2 vào dung dịch NaNO3.
(V) Sục khí NH3 vào dung dịch Na2CO3.
(VI) Cho dung dịch Na2SO4 vào dung dịch Ba(OH)2.
Các thí nghiệm đều điều chế được NaOH là:
A. II, III và VI. B. I, II và III. C. I, IV và V. D. II, V và VI.
Câu 27: Đốt cháy hoàn toàn một hợp chất hữu cơ X, thu được 0,351 gam H2O và 0,4368 lít khí CO2
(ở đktc). Biết X có phản ứng với Cu(OH)2 trong môi trường kiềm khi đun nóng. Chất X là
A. O=CH-CH=O. B. CH2=CH-CH2-OH. C. CH3COCH3. D. C2H5CHO.
Câu 28: Cho các phản ứng hóa học sau:
(1) (NH4)2SO4 + BaCl2 → (2) CuSO4 + Ba(NO3)2 →
(3) Na2SO4 + BaCl2 → (4) H2SO4 + BaSO3 →
(5) (NH4)2SO4 + Ba(OH)2 → (6) Fe2(SO4)3 + Ba(NO3)2 →
Các phản ứng đều có cùng một phương trình ion rút gọn là:
A. (1), (2), (3), (6). B. (1), (3), (5), (6). C. (2), (3), (4), (6). D. (3), (4), (5), (6).
Câu 29: Cho X là hợp chất thơm; a mol X phản ứng vừa hết với a lít dung dịch NaOH 1M. Mặt khác,
nếu cho a mol X phản ứng với Na (dư) thì sau phản ứng thu được 22,4a lít khí H2 (ở đktc). Công thức
cấu tạo thu gọn của X là
A. HO-C6H4-COOCH3. B. CH3-C6H3(OH)2.
C. HO-CH2-C6H4-OH. D. HO-C6H4-COOH.
Trang 3/6 – Mã đề thi 148
Câu 30: Cho m gam bột Fe vào 800 ml dung dịch hỗn hợp gồm Cu(NO3)2 0,2M và H2SO4 0,25M.
Sau khi các phản ứng xảy ra hoàn toàn, thu được 0,6m gam hỗn hợp bột kim loại và V lít khí NO (sản
phẩm khử duy nhất, ở đktc). Giá trị của m và V lần lượt là
A. 10,8 và 4,48. B. 10,8 và 2,24. C. 17,8 và 2,24. D. 17,8 và 4,48.
Câu 31: Cho một số tính chất: có dạng sợi (1); tan trong nước (2); tan trong nước Svayde (3); phản
ứng với axit nitric đặc (xúc tác axit sunfuric đặc) (4); tham gia phản ứng tráng bạc (5); bị thuỷ phân
trong dung dịch axit đun nóng (6). Các tính chất của xenlulozơ là:
A. (2), (3), (4) và (5). B. (3), (4), (5) và (6). C. (1), (2), (3) và (4). D. (1), (3), (4) và (6).
Câu 32: Dãy gồm các chất được sắp xếp theo chiều tăng dần nhiệt độ sôi từ trái sang phải là:
A. CH3COOH, C2H5OH, HCOOH, CH3CHO. B. CH3CHO, C2H5OH, HCOOH, CH3COOH.
C. CH3COOH, HCOOH, C2H5OH, CH3CHO. D. HCOOH, CH3COOH, C2H5OH, CH3CHO.
Câu 33: Phát biểu nào sau đây là đúng?
A. Photpho trắng có cấu trúc tinh thể nguyên tử.
B. Ở thể rắn, NaCl tồn tại dưới dạng tinh thể phân tử.
C. Nước đá thuộc loại tinh thể phân tử.
D. Kim cương có cấu trúc tinh thể phân tử.
Câu 34: Hòa tan hoàn toàn 20,88 gam một oxit sắt bằng dung dịch H2SO4 đặc, nóng thu được dung
dịch X và 3,248 lít khí SO2 (sản phẩm khử duy nhất, ở đktc). Cô cạn dung dịch X, thu được m gam
muối sunfat khan. Giá trị của m là
A. 52,2. B. 54,0. C. 58,0. D. 48,4.
Câu 35: Cho hỗn hợp X gồm CH4, C2H4 và C2H2. Lấy 8,6 gam X tác dụng hết với dung dịch brom
(dư) thì khối lượng brom phản ứng là 48 gam. Mặt khác, nếu cho 13,44 lít (ở đktc) hỗn hợp khí X tác
dụng với lượng dư dung dịch AgNO3 trong NH3, thu được 36 gam kết tủa. Phần trăm thể tích của CH4
có trong X là
A. 20%. B. 50%. C. 25%. D. 40%.
Câu 36: Hỗn hợp X gồm axit Y đơn chức và axit Z hai chức (Y, Z có cùng số nguyên tử cacbon).
Chia X thành hai phần bằng nhau. Cho phần một tác dụng hết với Na, sinh ra 4,48 lít khí H2 (ở đktc).
Đốt cháy hoàn toàn phần hai, sinh ra 26,4 gam CO2. Công thức cấu tạo thu gọn và phần trăm về khối
lượng của Z trong hỗn hợp X lần lượt là
A. HOOC-CH2-COOH và 70,87%. B. HOOC-CH2-COOH và 54,88%.
C. HOOC-COOH và 60,00%.
Câu 37: Phát biểu nào sau đây là đúng? |
D. HOOC-COOH và 42,86%. |
A. Tơ visco là tơ tổng hợp.
B. Trùng ngưng buta-1,3-đien với acrilonitrin có xúc tác Na được cao su buna-N.
C. Trùng hợp stiren thu được poli(phenol-fomanđehit).
D. Poli(etylen terephtalat) được điều chế bằng phản ứng trùng ngưng các monome tương ứng.
Câu 38: Cho các hợp chất sau:
(a) HOCH2-CH2OH.
(c) HOCH2-CH(OH)-CH2OH. |
(b) HOCH2-CH2-CH2OH.
(d) CH3-CH(OH)-CH2OH.
(f) CH3-O-CH2CH3. |
| (e) CH3-CH2OH. |
| Các chất đều tác dụng được với Na, Cu(OH)2 là: |
| A. (a), (b), (c). |
B. (c), (d), (f). |
C. (a), (c), (d). |
D. (c), (d), (e). |
Câu 39: Hai hợp chất hữu cơ X và Y là đồng đẳng kế tiếp, đều tác dụng với Na và có phản ứng tráng
bạc. Biết phần trăm khối lượng oxi trong X, Y lần lượt là 53,33% và 43,24%. Công thức cấu tạo của
X và Y tương ứng là
A. HO–CH2–CHO và HO–CH2–CH2–CHO.
B. HO–CH2–CH2–CHO và HO–CH2–CH2–CH2–CHO.
C. HO–CH(CH3)–CHO và HOOC–CH2–CHO.
D. HCOOCH3 và HCOOCH2–CH3.
Câu 40: Thí nghiệm nào sau đây có kết tủa sau phản ứng?
A. Cho dung dịch NaOH đến dư vào dung dịch Cr(NO3)3.
B. Cho dung dịch NH3 đến dư vào dung dịch AlCl3.
Trang 4/6 – Mã đề thi 148
C. Cho dung dịch HCl đến dư vào dung dịch NaAlO2 (hoặc Na[Al(OH)4]).
D. Thổi CO2 đến dư vào dung dịch Ca(OH)2.
_________________________________________________________________________________
II. PHẦN RIÊNG [10 câu]
Thí sinh chỉ được chọn làm một trong hai phần (phần A hoặc B)
A. Theo chương trình Chuẩn (10 câu, từ câu 41 đến câu 50)
Câu 41: Este X (có khối lượng phân tử bằng 103 đvC) được điều chế từ một ancol đơn chức (có tỉ
khối hơi so với oxi lớn hơn 1) và một amino axit. Cho 25,75 gam X phản ứng hết với 300 ml dung
dịch NaOH 1M, thu được dung dịch Y. Cô cạn Y thu được m gam chất rắn. Giá trị m là
A. 27,75. B. 24,25. C. 26,25. D. 29,75.
Câu 42: Hiđro hoá hoàn toàn m gam hỗn hợp X gồm hai anđehit no, đơn chức, mạch hở, kế tiếp nhau
trong dãy đồng đẳng thu được (m + 1) gam hỗn hợp hai ancol. Mặt khác, khi đốt cháy hoàn toàn cũng
m gam X thì cần vừa đủ 17,92 lít khí O2 (ở đktc). Giá trị của m là
A. 17,8. B. 24,8. C. 10,5. D. 8,8.
Câu 43: Cho hiđrocacbon X phản ứng với brom (trong dung dịch) theo tỉ lệ mol 1 : 1, thu được chất
hữu cơ Y (chứa 74,08% Br về khối lượng). Khi X phản ứng với HBr thì thu được hai sản phẩm hữu
cơ khác nhau. Tên gọi của X là
A. but-1-en. B. xiclopropan. C. but-2-en. D. propilen.
Câu 44: Phát biểu nào sau đây là đúng?
A. Saccarozơ làm mất màu nước brom.
B. Xenlulozơ có cấu trúc mạch phân nhánh.
C. Amilopectin có cấu trúc mạch phân nhánh.
D. Glucozơ bị khử bởi dung dịch AgNO3 trong NH3.
Câu 45: Nhúng một thanh sắt nặng 100 gam vào 100 ml dung dịch hỗn hợp gồm Cu(NO3)2 0,2M và
AgNO3 0,2M. Sau một thời gian lấy thanh kim loại ra, rửa sạch làm khô cân được 101,72 gam (giả
thiết các kim loại tạo thành đều bám hết vào thanh sắt). Khối lượng sắt đã phản ứng là
A. 1,40 gam. B. 2,16 gam. C. 0,84 gam. D. 1,72 gam.
Câu 46: Ứng dụng nào sau đây không phải của ozon?
A. Tẩy trắng tinh bột, dầu ăn. B. Chữa sâu răng.
C. Điều chế oxi trong phòng thí nghiệm. D. Sát trùng nước sinh hoạt.
Câu 47: Cho sơ đồ chuyển hoá giữa các hợp chất của crom:
Cr(OH)3 ⎯⎯⎯⎯ + KOH→X ⎯+ (Cl + KOH) ⎯⎯⎯⎯⎯ 2 → Y ⎯+ H SO ⎯⎯⎯ 2 4→ Z ⎯+ (FeSO + H SO ⎯⎯⎯⎯⎯⎯ 4 2 4 )→ T
Các chất X, Y, Z, T theo thứ tự là:
A. K2CrO4; KCrO2; K2Cr2O7; Cr2(SO4)3. B. KCrO2; K2Cr2O7; K2CrO4; Cr2(SO4)3.
C. KCrO2; K2Cr2O7; K2CrO4; CrSO4. D. KCrO2; K2CrO4; K2Cr2O7; Cr2(SO4)3.
Câu 48: Đốt cháy hoàn toàn 1 mol hợp chất hữu cơ X, thu được 4 mol CO2. Chất X tác dụng được với
Na, tham gia phản ứng tráng bạc và phản ứng cộng Br2 theo tỉ lệ mol 1 : 1. Công thức cấu tạo của X là
A. HO-CH2-CH2-CH=CH-CHO. B. HOOC-CH=CH-COOH.
C. HO-CH2-CH=CH-CHO. D. HO-CH2-CH2-CH2-CHO.
Câu 49: Cho 100 ml dung dịch KOH 1,5M vào 200 ml dung dịch H3PO4 0,5M, thu được dung dịch
X. Cô cạn dung dịch X, thu được hỗn hợp gồm các chất là
A. KH2PO4 và K3PO4. B. KH2PO4 và K2HPO4.
C. KH2PO4 và H3PO4. D. K3PO4 và KOH.
Câu 50: Hoà tan hoàn toàn 24,4 gam hỗn hợp gồm FeCl2 và NaCl (có tỉ lệ số mol tương ứng là 1 : 2)
vào một lượng nước (dư), thu được dung dịch X. Cho dung dịch AgNO3 (dư) vào dung dịch X, sau
khi phản ứng xảy ra hoàn toàn sinh ra m gam chất rắn. Giá trị của m là
A. 57,4. B. 28,7. C. 10,8. D. 68,2.
Trang 5/6 – Mã đề thi 148
B. Theo chương trình Nâng cao (10 câu, từ câu 51 đến câu 60)
Câu 51: Hỗn hợp X gồm hai ancol no, đơn chức, mạch hở, kế tiếp nhau trong dãy đồng đẳng. Oxi hoá
hoàn toàn 0,2 mol hỗn hợp X có khối lượng m gam bằng CuO ở nhiệt độ thích hợp, thu được hỗn hợp
sản phẩm hữu cơ Y. Cho Y tác dụng với một lượng dư dung dịch AgNO3 trong NH3, thu được 54 gam
Ag. Giá trị của m là
A. 15,3. B. 13,5. C. 8,1. D. 8,5.
Câu 52: Cho 0,04 mol một hỗn hợp X gồm CH2=CH-COOH, CH3COOH và CH2=CH-CHO phản
ứng vừa đủ với dung dịch chứa 6,4 gam brom. Mặt khác, để trung hoà 0,04 mol X cần dùng vừa đủ
40 ml dung dịch NaOH 0,75 M. Khối lượng của CH2=CH-COOH trong X là
A. 0,56 gam. B. 1,44 gam. C. 0,72 gam. D. 2,88 gam.
Câu 53: Phát biểu nào sau đây không đúng?
A. Glucozơ tác dụng được với nước brom.
B. Khi glucozơ ở dạng vòng thì tất cả các nhóm OH đều tạo ete với CH3OH.
C. Glucozơ tồn tại ở dạng mạch hở và dạng mạch vòng.
D. Ở dạng mạch hở, glucozơ có 5 nhóm OH kề nhau.
| Câu 54: Cho các thế điện cực chuẩn: |
`
6V; |
3+ |
Trong các pin sau đây, pin nào có suất điện động chuẩn lớn nhất?
4V. |
2+ |
o
E 1,6 A /Al l = – 6V; E 0,7 oZn /Zn 2+ = – E 0,13V; oPb /Pb 2+ = –
o
E 0,3 Cu /Cu = +
A. Pin Zn – Cu. B. Pin Zn – Pb. C. Pin Al – Zn. D. Pin Pb – Cu.
Câu 55: Khi hoà tan hoàn toàn 0,02 mol Au bằng nước cường toan thì số mol HCl phản ứng và số
mol NO (sản phẩm khử duy nhất) tạo thành lần lượt là
A. 0,03 và 0,02. B. 0,06 và 0,01. C. 0,03 và 0,01. D. 0,06 và 0,02.
Câu 56: Người ta điều chế anilin bằng sơ đồ sau:
Benzen 3
2 4
+ HNO ®Æc
⎯⎯⎯⎯⎯⎯ H SO ®Æc → Nitrobenzen ⎯⎯⎯⎯⎯ Fe + HCl to → Anilin
Biết hiệu suất giai đoạn tạo thành nitrobenzen đạt 60% và hiệu suất giai đoạn tạo thành anilin đạt
50%. Khối lượng anilin thu được khi điều chế từ 156 gam benzen là
A. 186,0 gam. B. 55,8 gam. C. 93,0 gam. D. 111,6 gam.
Câu 57: Phân bón nào sau đây làm tăng độ chua của đất?
A. KCl. B. NH4NO3. C. NaNO3. D. K2CO3.
Câu 58: Cho dung dịch X chứa hỗn hợp gồm CH3COOH 0,1M và CH3COONa 0,1M. Biết ở 25 oC,
Ka của CH3COOH là 1,75.10-5 và bỏ qua sự phân li của nước. Giá trị pH của dung dịch X ở 25 oC là
A. 1,00. B. 4,24. C. 2,88. D. 4,76.
Câu 59: Hòa tan hoàn toàn 1,23 gam hỗn hợp X gồm Cu và Al vào dung dịch HNO3 đặc, nóng thu
được 1,344 lít khí NO2 (sản phẩm khử duy nhất, ở đktc) và dung dịch Y. Sục từ từ khí NH3 (dư) vào
dung dịch Y, sau khi phản ứng xảy ra hoàn toàn thu được m gam kết tủa. Phần trăm về khối lượng
của Cu trong hỗn hợp X và giá trị của m lần lượt là
A. 21,95% và 2,25. B. 78,05% và 2,25. C. 21,95% và 0,78. D. 78,05% và 0,78.
Câu 60: Cho sơ đồ chuyển hoá:
Butan-2-ol
o
H SO ®Æc, t 2 4
⎯⎯⎯⎯⎯⎯→ X (anken) ⎯⎯⎯⎯ + HBr →Y ⎯⎯⎯⎯⎯⎯⎯ + Mg, ete khan → Z
Trong đó X, Y, Z là sản phẩm chính. Công thức của Z là
A. (CH3)3C-MgBr. B. CH3-CH2-CH2 -CH2-MgBr.
C. CH3-CH(MgBr)-CH2-CH3. D. (CH3)2CH-CH2-MgBr.
———————————————————- HẾT ———-
Trang 6/6 – Mã đề thi 148
O2 Education gửi các thầy cô link download đề thi
DA KA-09
DA KB-09
Hóa A 2009
Hóa B 2009
Xem thêm