SKKN Phát triển năng lực tư duy và thực hành cho học sinh lớp 11 THPT thông qua dạy học tích hợp chuyên đề Nitơ và Photpho
- ĐIỀU KIỆN HOÀN CẢNH TẠO RA SÁNG KIẾN
Để đáp ứng các yêu cầu đổi mới của thời đại và đất nước, đặc biệt yêu cầu của sự nghiệp công nghiệp hoá, hiện đại hoá thì phát triển giáo dục và đào tạo là một trong những động lực quan trọng nhất thúc đẩy sự nghiệp công nghiệp hoá, hiện đại hoá, là điều kiện phát huy nguồn lực con người, yếu tố phát triển xã hội, tăng trưởng kinh tế nhanh và bền vững. Bên cạnh năng lực về chuyên môn, người lao động phải có năng lực hành động, tự chủ, năng động sáng tạo, có năng lực giải quyết các vấn đề thường gặp và luôn luôn theo kịp được với sự tiến bộ nhanh chóng của khoa học kỹ thuật, có đạo đức, biết giữ gìn bản sắc văn hóa truyền thống dân tộc.
Chiến lược phát triển giáo dục 2011 – 2020 được thủ tướng chính phủ ban hành theo quyết định số 711/QĐ – TTg ngày 13/06/2012 đã ghi rõ: “Đổi mới căn bản, toàn diện nền giáo dục theo hướng chuẩn hóa, hiện đại hóa, xã hội hóa, dân chủ hóa, hội nhập quốc tế và thích ứng với nền kinh tế thị trường định hướng xã hội chủ nghĩa …, tập trung vào nâng cao chất lượng, đặc biệt là chất lượng giáo dục, giáo dục đạo đức, kỹ năng sống, năng lực sáng tạo, kỹ năng thực hành,…”.
Mục đích của việc đổi mới phương pháp dạy học ở trường phổ thông nói chung và dạy học phần Hóa học vô cơ 11 nói riêng là thay đổi lối dạy học truyền thụ một chiều sang dạy học theo “phương pháp dạy học tích cực” nhằm giúp học sinh phát huy tính tích cực, tự giác, sáng tạo, thực hành rèn luyện thói quen và khả năng tự học, tinh thần hợp tác, kỹ năng vận dụng kiến thức vào những tình huống khác nhau trong học tập và thực tiễn, tạo niềm tin, niềm vui hứng thú trong học tập.
Hiện nay khoa học và công nghệ phát triển với sức mạnh thần tốc, kỳ diệu, đó là sự ra đời của máy tính và internet. Nhưng bộ não là một phần lãnh thổ lớn nhất chưa được khám phá hết trên thế giới. Bộ não giúp chúng ta tự học và học tập suốt đời, từ khi sinh ra cho đến khi không còn có mặt trên trái đất này. Do đó việc phát triển năng lực sáng tạo và thực hành cho học sinh ngay từ khi ngồi trên ghế nhà trường là điều rất cần thiết. Sự thực hành và sáng tạo trong cuộc sống chính là biết đề ra những ý tưởng mới, độc đáo, hữu ích, phù hợp với hoàn cảnh. Nói cách khác là dám thách thức những ý kiến và phương pháp đã được mọi người chấp nhận để tìm ra những giải pháp hoặc khái niệm mới có tính đột biến cao hoặc mang tính kế thừa tích cực trên nền tảng cái cũ. Cũng có thể hiểu đơn giản sáng tạo chỉ là tìm ra một cách mới để làm việc hoặc làm cho công việc đó trôi chảy hơn. Một trong hai bán cầu não chi phối tới hoạt động thực hành và sáng tạo có cơ sở sinh lý thần kinh và tư duy của con người. Tâm lý học đã nghiên cứu và đi đến kết luận rằng tất cả mọi người đều có khả năng sáng tạo và thực hành, sáng tạo nhỏ hay lớn. Nếu được rèn luyện thì sự sáng tạo sẽ phát triển không ngừng cùng với năng lực thực hành khoa học và ngược lại nếu không rèn luyện thì sự sáng tạo và những kỹ năng thực hành sẽ dần bị mai một đi.
Năng lực thực hành của học sinh chính là khả năng các em thực hiện được những điều mới mẻ trong bài học và thực tiễn cuộc sống. Đó là biết làm thành thạo và luôn đổi mới, có những nét độc đáo riêng phù hợp với thực tế. Luôn biết và đề ra những cái mới khi chưa được học, nghe giảng, đọc tài liệu hay tham quan về việc đó nhưng vẫn đạt kết quả cao. Vì thế đối với học sinh nói chung và học sinh trung học phổ thông nói riêng, tất cả những gì mà họ “tự nghĩ ra“ khi giáo viên chưa dạy, học sinh chưa biết từ các nguồn khác nhau thì đều được coi là sáng tạo thực nghiệm. Sáng tạo và thực hành trong cuộc sống là bước nhảy vọt trong sự phát triển nhận thức của học sinh. Không có con đường logic để dẫn đến sự thực nghiệm, bản thân mỗi học sinh phải tự tìm lấy kinh nghiệm thông qua các hoạt động thực tiễn của mình hoặc dưới sự hướng dẫn của giáo viên, gia đình, nhà trường và xã hội. Do đó, để phát triển năng lực nhận thức, sự chủ động thực hành và sáng tạo của học sinh thì người giáo viên phải biết đặt học sinh vào vị trí chủ thể để các em phải tự lực, chủ động, tự giác, tích cực, cố gắng để chiếm hữu được tri thức, rèn luyện đạo đức, phát triển tư duy sáng tạo thực hành của bản thân. Trách nhiệm này đặt ra cho người giáo viên phải tìm ra được giải pháp hữu hiệu để rèn luyện năng lực cho học sinh ngay từ khi các em còn ngồi trên ghế nhà trường. Ở đây thì học sinh cần phải làm chủ những hệ thống kiến thức, kỹ năng, thái độ… phù hợp với lứa tuổi và kết nối chúng một cách hợp lý vào thực hiện thành công nhiệm vụ học tập, giải quyết hiệu quả những vấn đề đặt ra cho chính các em trong cuộc sống. Phát triển năng lực, đặc biệt là năng lực thực hành sáng tạo của người học chính là mục tiêu của quá trình dạy học. Vì thế vai trò quan trọng nhất của giáo dục chính là định hướng và giúp cho học sinh phát triển toàn diện các năng lực để giải quyết vấn đề một cách tư duy độc lập, có định hướng và tính sáng tạo trong thực nghiệm đột biến mà đặc biệt là đối với học sinh giỏi.
Từ những lý do trên, với mong ước góp phần vào việc nâng cao chất lượng dạy học nói chung và chất lượng dạy học môn Hóa học nói riêng đồng thời góp phần đào tạo cho đất nước một thế hệ trẻ năng động, thực hành sáng tạo đáp ứng được yêu cầu của xã hội hiện nay, tôi đã chọn đề tài: “Phát triển năng lực tư duy và thực hành cho học sinh lớp 11 THPT thông qua dạy học tích hợp chuyên đề Nitơ và Photpho”
- Mô tả giải pháp
- Mô tả giải pháp trước khi tạo ra sáng kiến
Hiện nay việc dạy và học cũng như quá trình đào tạo ở nước ta vẫn còn mang nặng tính hàn lâm kinh viện về lý thuyết mà thiếu đi tính thực tiễn, chưa hình thành được năng lực hành động và sáng tạo linh hoạt cho học sinh. Vì thế các em lĩnh hội tri thức một cách thụ động chỉ qua bài vở do thầy cô giảng dạy mà xa vời với đời sống thực tiễn và sản xuất. Cách học này sẽ khiến cho bài học thiếu sôi động, cứng nhắc và hiệu quả của việc phát huy tính tích cực, chủ động và thực hành sáng tạo của học sinh rất hạn chế. Do đó việc đổi mới một cách triệt để và mạnh mẽ cả chương trình cũng như phương pháp dạy và học là chìa khóa mấu chốt nhất đối với kết quả của sự nghiệp giáo dục nước nhà. Với tinh thần cải cách giáo dục thật triệt để và toàn diện cả trong dạy và học cùng với việc đổi mới cách thức kiểm tra và đánh giá hiện nay trong kỳ thi THPT quốc gia (bao gồm cả xét tốt nghiệp THPT và tuyển sinh đầu vào đại hoc) bắt đầu từ năm học 2010 – 2011 cũng như trong các kỳ thi học sinh giỏi các cấp thì môn Hóa học luôn hướng người học tới khả năng vận dụng, suy luận, áp dụng kiến thức lý thuyết vào thực tế đời sống và sản xuất, các kỹ năng thực hành của học sinh chứ không nặng nề tính toán, đánh đố học sinh, không yêu cầu học sinh “học tủ, học vẹt” các dạng bài tập. Sự liên hệ thực tế cùng khả năng thực hành sáng tạo của các em là thước đo quan trọng để đánh giá hiệu quả của quá trình dạy và học.
Thực tế hiện nay tôi thấy rằng học sinh Việt Nam đi thi thì rất giỏi, đạt kết quả rất cao trong các kỳ thi trong nước, khu vực và quốc tế nhưng kĩ năng vận dụng thực hành trong thực tiễn thì kém hơn học sinh, sinh viên các nước đã và đang phát triển rất nhiều Vì thế khi các em ra trường rồi đi làm thường bỡ ngỡ, thụ động, máy móc, kỹ năng lao động và làm việc cực kỳ hạn chế. Đây cũng là tình trạng chung về chất lượng nguồn nhân lực của nước ta hiện nay. Chính vì thế để đào tạo ra một lực lượng lao động tốt, có năng lực làm việc đạt hiệu quả cao, sáng tạo thì nhất thiết phải thay đổi toàn diện, triệt để các cơ chế, chính sách về giáo dục và đào tạo. Người giáo viên phải đổi mới phương pháp dạy học, vận dụng các phương pháp tích cực để rèn luyện cho học sinh các kĩ năng vận dụng kiến thức lí thuyết vào thực tế trong mọi tình huống. Kĩ năng này rất cần thiết và quan trọng khi các em trưởng thành. Để đem lại niềm vui, tạo hứng thú trong học tập cho học sinh thì giáo viên cần tạo ra môi trường học tập thật thoải mái để mỗi học sinh có thể phát huy tối đa được tính tích cực, chủ động thực hành sáng tạo, tăng khả năng tự học, sự tự tin làm chủ các vấn đề phát sinh và nâng cao khả năng hợp tác, làm việc theo nhóm, từ đó nâng cao chất lượng và hiệu quả dạy học. Phần Hóa học 11 THPT là cầu nối rất quan trọng cho học sinh học tiếp lên lớp 12 và cũng có ứng dụng thực tiễn vô cùng to lớn bởi dân số nước ta chủ yếu làm nông nghiệp nên nhu cầu về lượng phân bón để cung cấp cho cây trồng là rất lớn. Việc nghiên cứu học phần Nitơ và Photpho là đòn bẩy để phát triển công nghiệp sản xuất phân bón hiện nay. Việc dậy và học tốt phần này gây nhiều khó khăn cho cả giáo viên và học sinh bởi lượng kiến thức là rất phong phú và có phần trừu tượng. Các thầy cô giáo thường phải dậy theo phân phối chương trình trong thời lượng có hạn trong khi phần Nitơ và Photpho có nhiều ứng dụng thực tiễn và kiến thức quan trọng mà bất kỳ đề thi nào cũng thường xuyên hỏi tới, đặc biệt về axit HNO3, muối nitrat, phân bón Hóa học, độ dinh dưỡng của phân đạm, phân lân …. Với các em học sinh, để tiếp thu lượng kiến thức thực tiễn này cần phải có thời gian nhất định trải nghiệm, suy nghĩ, phân tích, đánh giá rồi vận dụng và vận dụng thành thạo trong khi giải các bài tập Hóa học. Vì vậy với cách dạy và học có phần cứng nhắc, thiếu sự sáng tạo linh hoạt và thực nghiệm như hiện nay thì kết quả thu được còn rất hạn chế. Các em thường chỉ nắm được phần nào lý thuyết còn phần thực nghiệm rất sơ sài và chung chung, khi làm những bài tập vận dụng và vận dụng mức độ nâng cao còn thiếu tính tổng quát, thực hành sáng tạo độc lập. Để đạt kết quả cao nhất đòi hỏi cả người dạy và người học cần phải chủ động và có những giải pháp linh hoạt và sáng tạo.
Qua nhiều năm công tác giảng dạy và học tập, tôi mạnh dạn được viết ra sáng kiến kinh nghiệm giảng dạy này để nâng cao năng lực tư duy và thực hành sáng tạo cho các em học sinh lớp 11 THPT mà đặc biệt là các em học sinh giỏi để giúp các em đạt kết quả cao trong kỳ thi học sinh giỏi toàn tỉnh, thi quốc gia, quốc tế và thi THPT quốc gia năm lớp 12.
- Mô tả giải pháp sau khi có sáng kiến
Trước hết chúng ta cần xem xét và đón nhận những xu hướng đổi mới về phương pháp dạy học hiện nay gồm:
+ Hướng 1: Tăng cường tính tích cực, tìm tòi sáng tạo, tiềm năng trí tuệ nói riêng và nhân cách nói chung ở người học, khả năng thích ứng với thực tiễn cuộc sống luôn đổi mới.
+ Hướng 2: Tăng cường khả năng tự vận dụng kiến thức đã học vào thực tiễn luôn biến đổi.
+ Hướng 3: Chuyển dần trọng tâm của phương pháp dạy học từ tính chất thông báo, tái hiện đại trà chung cho cả lớp sang tính chất phân hoá cá thể cao độ, tiến lên theo nhịp độ cá nhân. Hướng 1, 2, 3 để hoàn thiện chất lượng các phương pháp dạy học hiện có.
+ Hướng 4: Liên kết nhiều phương pháp dạy học riêng rẽ thành tổ hợp phương pháp dạy học phức hợp.
+ Hướng 5: Liên kết phương pháp dạy học với các phương tiện kỹ thuật dạy học hiện đại như phương tiện nghe nhìn, máy vi tính,…để tạo ra các tổ hợp phương pháp dạy học có dùng kỹ thuật.
+ Hướng 6: Chuyển hóa phương pháp khoa học thành phương pháp dạy học đặc thù của môn học, dạy học tích hợp và liên môn . . .
+ Hướng 7: Đa dạng hóa các phương pháp dạy học, cấp học, bậc học, các loại hình trường và các môn học. Hướng 4, 5, 6, 7 để thực hành sáng tạo nên những phương pháp dạy học mới.
Việc đổi mới phương pháp dạy học bộ môn Hóa học cũng tuân theo bẩy hướng nêu trên, nhưng trước mắt là tập trung vào hai hướng chính là dạy học lấy người học làm trung tâm (dạy học định hướng vào người học) và dạy học theo hướng hoạt động hóa người học. Phương pháp dạy học Hoá học phải đặt người học vào vị trí chủ thể của hoạt động nhận thức, làm cho họ hoạt động trong giờ học, rèn luyện cho học sinh tập giải quyết các vấn đề của khoa học từ dễ đến khó, có như vậy họ mới có điều kiện tốt để tiếp thu và vận dụng kiến thức một cách chủ động, thực hành sáng tạo. Do đặc thù bộ môn Hoá học là một môn khoa học thực nghiệm nên phương pháp dạy học phải tăng cường thí nghiệm thực hành và sử dụng thật tốt các thiết bị dạy học giúp mô hình hoá, giải thích chứng minh các quá trình hoá học để phát huy tính tích cực, sáng tạo, nâng cao hứng thú của người học. Phương pháp dạy học tích cực hướng tới việc hoạt động hóa, tích cực hóa hoạt động nhận thức của người học, nghĩa là tập trung vào phát huy tính tích cực của học sinh, làm sao trong quá trình học tập, người học được hoạt động nhiều hơn, thảo luận cùng nhau nhiều hơn và quan trọng hơn là được suy nghĩ nhiều hơn. Trong phương pháp dạy học tích cực, người học – đối tượng của hoạt động “dạy”, đồng thời là chủ thể của hoạt động “học” được cuốn hút vào các hoạt động học tập do giáo viên tổ chức và chỉ đạo, qua đó tự lực khám phá những kiến thức mới. Được đặt vào những tình huống thì người học sẽ trực tiếp quan sát, thảo luận, làm thí nghiệm và giải quyết các vấn đề đặt ra. Nhờ vậy, học sinh vừa khám phá ra kiến thức kĩ năng mới, vừa biết được phương pháp “tìm ra” kiến thức, kĩ năng đó mà không rập theo những khuôn mẫu sẵn có. Dạy học theo hướng này thì giáo viên không chỉ truyền đạt tri thức mà còn hướng dẫn hành động và học sinh được bộc lộ, phát huy hết tiềm năng sáng tạo của mình.
Dạy học tích hợp và tích cực xem việc rèn luyện phương pháp học tập cho học sinh không chỉ là một biện pháp nâng cao hiệu quả dạy học mà còn là một mục tiêu dạy học. Nếu rèn luyện cho người học có được phương pháp, kĩ năng, thói quen, ý chí tự học thì sẽ tạo cho họ lòng ham học, khơi dậy nội lực vốn có trong họ, kết quả học tập sẽ được nhân lên, giúp họ dễ dàng thích ứng với cuộc sống của xã hội phát triển. Vì vậy, hiện nay, người ta nhấn mạnh mặt hoạt động học trong quá trình dạy học, nỗ lực tạo ra sự chuyển biến từ học tập thụ động sang tự học chủ động, đặt vấn đề phát triển tự học ngay trong trường phổ thông, không chỉ tự học ở nhà sau bài lên lớp mà tự học cả trong tiết học có sự hướng dẫn của giáo viên. Giáo viên cần tạo điều kiện thuận lợi để học sinh được tham gia đánh giá lẫn nhau, tự đánh giá đúng và điều chỉnh hoạt động kịp thời là năng lực rất cần cho sự thành đạt trong cuộc sống mà nhà trường phải trang bị cho học sinh.
Theo hướng phát triển các phương pháp tích cực để đào tạo những con người năng động, sớm thích nghi với đời sống xã hội, thì việc kiểm tra, đánh giá không thể dừng lại ở yêu cầu tái hiện các kiến thức, lặp lại các kĩ năng đã học mà phải khuyến khích trí thông minh, óc sáng tạo trong việc giải quyết những tình huống thực tế. Với sự trợ giúp của các thiết bị kĩ thuật, kiểm tra đánh giá sẽ không còn là một công việc nặng nhọc đối với giáo viên, mà lại cho nhiều thông tin kịp thời hơn để linh hoạt điều chỉnh hoạt động dạy, chỉ đạo hoạt động học.
Trong phạm vi của đề tài này tôi xin mạnh dạn đề cập tới một số biện pháp dạy học nhằm phát triển năng lực tư duy và thực hành sáng tạo cho học sinh thông qua dạy học phần Nitơ và Photpho lớp 11 THPT. Hi vọng rằng từ đây các quý thầy (cô) giáo có thể tham khảo để thay đổi cách thức truyền tải kiến thức tới các em học sinh nhằm hình thành năng lực tư duy và hoạt động thực hành sáng tạo để phát huy tính tích cực, chủ động, thực hành sáng tạo và linh hoạt của các em.
2.1. Tích hợp liên môn cho học sinh phát hiện và giải quyết các vấn đề thực tiễn trong khi nghiên cứu bài mới khi không sử dụng thí nghiệm hóa học.
Mở đầu, giáo viên có thể thuyết trình nêu vấn đề, giới thiệu hoặc cho học sinh xem phim về thí nghiệm hóa học hay phim về hiện tượng thức tế, về một vấn đề nào đó để dẫn dắt học sinh vào các tình huống có vấn đề. Các em sẽ nhận được vấn đề mà mình hoặc nhóm học tập của mình phải giải quyết. Sau đó giáo viên để thời gian cho các nhóm thảo luận thực nghiệm. Đối với những bài không sử dụng thí nghiệm giáo viên cần hướng dẫn, rèn luyện cho học sinh biết phân tích, so sánh, đối chiếu để nêu bật được mối liên hệ bản chất của các kiến thức để dẫn đến tình huống có vấn đề mà việc giải quyết vấn đề sẽ hình thành được những hiểu biết và kiến thức mới.
Quy trình dạy học sinh nêu và giải quyết vấn đề đối với những bài học nghiên cứu về chất mà không sử dụng thí nghiệm hóa học.
Bước 1: Đặt vấn đề
Thông qua hệ thống kiến thức đã học, giáo viên yêu cầu học sinh phân tích và so sánh về các mối quan hệ giữa cấu tạo với tính chất vật lý và tính chất hóa học, mối quan hệ giữa cấu tạo – tính chất – điều chế, tính chất hóa học – hiện tượng tự nhiên,… để phát hiện ra mâu thuẫn, lôi cuốn học sinh vào vấn đề nghiên cứu một cách tự giác.
Bước 2: Phát biểu vấn đề
Giáo viên hướng dẫn học sinh phát biểu các vấn đề cần giải quyết.
Bước 3: Xác định phương hướng giải quyết – đề xuất giả thuyết
Giáo viên đưa ra phương hướng giải quyết, nêu giả thuyết hoặc đưa ra các câu hỏi để học sinh tự đề xuất giả thuyết.
Bước 4+5: Lập kế hoạch giải và giải theo giả thuyết
Giáo viên hướng dẫn học sinh nghiên cứu tài liệu, phân tích, tổng hợp, so sánh, và trả lời các câu hỏi, phủ nhận điều này, xác định điều kia để đi đến thống nhất một vấn đề.
Bước 6: Đánh giá kế hoạch giải quyết
Kiểm tra hệ thống câu trả lời về nội dung và logic lập luận để xác định xem giả thuyết đúng hay sai.
Bước 7: Kết luận về lời giải
Giáo viên nêu lên các kiến thức cần lĩnh hội, kiến thức cần hệ thống và ghi nhớ.
Bước 8: Kiểm tra lại kiến thức vừa tiếp thu ở các ví dụ khác
Trong chương trình hóa học vô cơ lớp 11 THPT có nhiều bài học không thể nêu vấn đề thông qua việc tiến hành các thí nghiệm thực hành được do nhiều nguyên nhân khác nhau. Chẳng hạn như có thể tạo ra các hợp chất không có lợi cho cơ thể con người và môi trường như NH3, N2O; NO2, NO, CO2, CO,…nhiều phản ứng không xảy ra được ở nhiệt độ thường mà yêu cầu nhiệt độ rất cao, điều kiện khắc nghiệt, thời gian lâu mới xảy ra phản ứng… Vì thế có thể sử dụng những hiện tượng xảy ra trong tự nhiên để nêu vấn đề cho học sinh, giúp các em giải thích được các hiện tượng thực tế, trong các câu ca dao, tục ngữ, tránh mê tín dị đoan (hiện tượng ma chơi, mưa axit,…).
VÍ DỤ 1: Trong tục ngữ Việt Nam có câu
“Lúa chiêm lấp ló đầu bờ
Nghe thấy tiếng sấm phất cờ mà lên”
Câu này mang ý nghĩa về hóa học như thế nào?
Giáo viên có thể đặt câu hỏi này khi dạy bài “ Nitơ” hoặc khi giải thích phần chu trình của Nitơ trong tự nhiên ở bài giảng “axit HNO3” hoặc trong bài “ Phân bón hóa học” tạo tình huống có vấn đề cho học sinh và hướng dẫn các em cách giải quyết.
Bước 1: Đặt vấn đề
Giáo viên đặt vấn đề: tại sao vụ chiêm khi lúa đang trổ đòng mà có sấm chớp, kèm theo mưa rào sẽ rất tốt và cho năng xuất mùa màng cao?
Bước 2: Xác định phương hướng giải quyết
– Trong không khí có những chất khí nào? Các chất khí này có phản ứng được với nhau không?
– Tại sao có sấm chớp, kèm mưa rào thì năng suất lúa lại cao?
– Ta đã biết lúa tốt nhờ có các chất dinh dưỡng, vậy có gì chứng tỏ sấm chớp tạo ra chất dinh dưỡng?
Bước 3: Lập kế hoạch giải quyết vấn đề
– Học sinh: trong không khí khoảng 80% là khí N2 và khoảng 20% khí O2. Trong điều kiện thường thì các chất này không phản ứng với nhau.Trong bài tính chất hóa học của N2 thì N2 chỉ phản ứng với O2 nếu trong điều kiện khoảng 30000C hoặc tia lửa điện. Trong cơn giông gió, sấm sét đã tạo ra năng lượng cho phản ứng giữa Nitơ và oxi tạo khí NO: N2 + O2 → 2NO
– Trong không khí có sẵn oxi nên khí NO không màu sinh ra hoàn toàn có thể phản ứng ngay với oxi trong không khí tạo nitơ đioxit (NO2), sau đó NO2 hóa hợp với oxi và nước tạo ra axit HNO3.
2NO + O2 → 2NO2
4NO2 + O2 + 2H2O → 4HNO3
HNO3 → H+ + NO3–
– Nhờ có sấm chớp ở các cơn mưa giông mà mỗi năm trung bình mỗi mẫu đất được cung cấp 6 – 7 kg Nitơ. Ion NO3– tạo ra chính là phân đạm cung cấp dưỡng chất cho cây.
Bước 4 : Đánh giá việc thực hiện kế hoạch giải:
Việc thực hiện kế hoạch giải dựa trên tính chất hóa học của N2, NO, NO2 và dựa vào thuyết điện ly để áp dụng cho HNO3 là đúng đắn và logic.
Bước 5: Mở rộng hướng phát triển vấn đề
Trong thực tế, người ta đã điều chế đạm Ure [(NH2)2CO] từ CO2 và NH3 ở nhiệt độ và áp suất cao để chủ động bón cho cây trồng theo phương trình:
2NH3 + CO2 → (NH2)2CO + H2O
(NH2)2CO + 2H2O → (NH4)2CO3.
(NH4)2CO3 → 2NH4+ + CO32-
Như vậy khi bón đạm Ure cho cây thì (NH2)2CO bị hòa tan trong nước tạo ra ion NH4+ và ion CO32-. Cây trồng sẽ hấp thụ được ion NH4+ để sinh trưởng và phát triển còn gốc axit yếu CO32- sẽ không làm thay đổi môi trường của đất và nước. Do đó đạm Ure hay được sử dụng phổ biến và rộng rãi nhất. Người ta thường bón đạm Ure vào lúc buổi chiều tối mặt trời vừa lặn và thường bón cùng với phân lân và phân hữu cơ để tạo ra hiệu quả cao nhất, tránh cho đất không bị rửa trôi và bạc màu. Với nước ta thì gần 70% dân số làm nông nghiệp nên vai trò và tầm ảnh hưởng của ngành công nghiệp sản xuất phân bón với nông nghiệp là vô cùng to lớn bởi nó sẽ quyết định trực tiếp đến năng xuất của cây trồng. Trong nền nông nghiệp hiện đại ngày nay cần phải đặc biệt quan tâm tới câu nói “ nhất nước, nhì phân, tam cần, tứ giống”. Thực tế thì nhu cầu sử dụng phân bón là rất lớn mà cung không đủ cầu nên nước ta thường phải nhập khẩu phân bón từ Indonesia, Malaysia, Thailand, Trung quốc …. Từ đây giáo viên có thể gợi mở cho học sinh hiểu rõ hơn vai trò của nước, phân bón, giống cây trồng và các hóa chất sử dụng để bảo vệ và chăm sóc cho cây trồng trong ngành nông nghiệp. Các em sẽ nhận thức được trách nhiệm cũng như có ý chí vươn lên, đóng góp công sức để nghiên cứu, phát triển khoa học kỹ thuật phục vụ cho sự nghiệp công nghiệp hóa và hiện đại hóa của nước nhà.
VÍ DỤ 2: Khi dạy phần “Luyện tập về Nitơ và hợp chất của Nitơ” hoặc bài “phân bón hóa học” để tiết dạy thêm phần thực tế, thực hành sáng tạo và đặc biệt tạo sự hứng thú, sôi động cùng với việc tăng cường tính chất liên môn. Giáo viên có thể cho học sinh đọc “ Chuyện tình cô gái Nitơ”, sau đó yêu cầu từng nhóm giải thích và viết các phương trình phảhanhfn thực nghiệm đã xảy ra:
Chuyện tình cô gái Nitơ
Em là cô gái Nitơ
Tên thật Azốt anh ngờ làm chi?
Không mùi cũng chặng vị gì
Sự cháy, sự sống chẳng duy trì trong em
Cho dù không giống Halogen
Mà ai cũng bảo sao hiền thế em?
Nhà em ở chu kì hai
Có năm điện tử ngoài cùng bao che
Mùa đông cũng như mùa hè
Nhớ ô số bảy, nhớ về thăm em.
Bình thường em ít người quen
Người ta cứ bảo em hiền thế cơ?
Cứ như dòng họ khí trơ
Ai mà ngỏ ý làm ngơ sao đành.
Tuổi em mười bốn xuân xanh
Nghĩ chi tới chuyện ái ân làm gì?
Thế rồi ngày tháng qua đi,
Có anh bạn trẻ Oxi gần nhà
Bình thường anh chẳng lân la
Những khi giông tố đến nhà tìm em
Dần lâu rồi cũng sinh quen,
Nitơ Oxit sinh liền ra ngay.
Không màu là chất khí này,
Bị oxi hoá liền ngay tức thì.
Thêm một nguyên tử oxi,
Thêm màu nâu đỏ, chất nào đậm hơn?
Bơ vơ cuộc sống cô đơn,
Thuỷ Tề thấy vậy rước ngay về nhà.
Gọi ngay hoàng tử nước ra
Ghép luôn chồng vợ thật là ác thay.
Hờn căm, khói bốc dâng đầy,
Nên tim em chịu chua cay trăm bề.
Những khi gió rét, đêm về,
Oxi chẳng được gần kề bên em.
Vì chung dòng họ Á Kim,
Cho nên cô bác hai bên bực mình.
Oxi từ đó buồn tình,
Bỏ em cô độc, một mình bơ vơ.
Đầu xóm có anh Hidrô,
Một hôm nắng đẹp viết thư tỏ tình.
Phòng riêng lạnh lẽo một mình,
Nhìn gương chỉ thấy bóng mình trong gương.
Hidrô tỏ ý muốn thương,
Làm sao nỡ để đôi đường cách xa?
Sớm đào tối mận lân la,
Hidrô thường đến chơi nhà em luôn.
Thấy em vẫn tỏ ý buồn,
Rủ luôn anh Sắt cùng trường sang chơi.
Anh Sắt miệng lưỡi nhất đời,
Đến chơi hôm ấy thì trời nóng ran.
Lựa lời khuyên nhủ hỏi han,
Bảo em nên sánh cùng chàng Hidrô.
Chuyện tình hò hẹn mấy khi,
Để người nhòm ngó làm chi cho phiền.
Từ đây chồng thảo vợ hiền,
Cùng em ra đồng để lúa tốt xanh.
Đừng quên em nhé các anh,
Amoniac chính danh chất này.
Đành rằng em có mùi khai,
Làm phân bón ruộng chẳng ai phiền lòng.
Sau khi cho từng nhóm trình bầy thì giáo viên sẽ cho các em tự đánh giá nhau rồi củng cố và khắc sâu cho các em nắm vững hơn kiến thức thực tiễn trong đời sống hằng ngày. Tại sao người ta có thể dùng nước tiểu để tưới cho cây và nên tưới phân vào thời điểm nào là tốt nhất?
VÍ DỤ 3: Khi dạy phần tính chất và ứng dụng của muối amoni trong bài “Amoniac và muối amoni”, giáo viên có thể tạo tình huống có vấn đề liên quan đến thực tế và dạy học sinh quy trình giải quyết vấn đề: Tại sao trên thực tế người ta dùng muối amoni clorua để tẩy sạch bề mặt của kim loại trước khi hàn?
Bước 1: Nêu vấn đề
GV đặt vấn đề: Tại sao trên thực tế người ta dùng muối amoni clorua để tẩy sạch bề mặt của kim loại trước khi hàn?
Bước 2: Xác định phương hướng giải quyết
GV có thể hướng dẫn học sinh giải quyết vấn đề bằng hệ thống câu hỏi:
* Tại sao phải tẩy sạch bề mặt kim loại trước khi hàn?
* Khi ở nhiệt độ cao, muối NH4Cl bị phân hủy thành các chất gì?
* Các chất thu được phản ứng như thế nào với oxit kim loại?
Bước 3: Lập kế hoạch giải quyết vấn đề
HS giải quyết vấn đề dựa trên những gợi ý trên:
* Vì bề mặt kim loại luôn luôn có một lớp gỉ là các oxit, các muối bazơ của kim loại, bởi nó bị oxi hóa khi để trong không khí. Khi hàn kim loại ta phải loại bỏ lớp gỉ này để cho mối hàn được chắc và bền hơn.
* Khi ở nhiệt độ cao thì muối NH4Cl bị phân hủy thành NH3 và HCl
NH4Cl → NH3 (k) + HCl (k)
* HCl tác dụng được với các oxit và các muối của kim loại, NH3 có tính khử mạnh có thể khử được oxit kim loại thành kim loại.
Bước 4: Đánh giá việc thực hiện kế hoạch giải
Việc thực hiện kế hoạch giải dựa trên tính chất hóa học của muối NH4Cl, NH3 và HCl là đúng đắn, hợp logic.
Bước 5: Mở rộng hướng phát triển vấn đề
Trên thực tế người ta còn có những cách nào để tẩy gỉ trên bề mặt kim loại nữa? Liệu có thể dùng dung dịch nào để thay thế, giải thích? Các em hãy trao đổi tìm hiểu, giải thích các cách làm đó để thảo luận trong tiết học sau. Như vậy, người giáo viên có thể sử dụng các bài tập thực nghiệm khi nghiên cứu tài liệu mới để hình thành một số khái niệm, giải quyết một số tình huống có vấn đề, để củng cố, khắc sâu kiến thức, tạo niềm tin cho học sinh vào những gì đã được học.
VÍ DỤ 4: Khi dạy về bài Photpho (Hóa học lớp 11 THPT), giáo viên có thể liên hệ thực tế khi mở bài như sau :
+ GV: Trong “Văn tế thập loại chúng sinh”, đại thi hào Nguyễn Du đã viết:
“Lập lòe ngọn lửa ma chơi
Tiếng oan văng vẳng tối trời còn thương”
Thế “ma chơi” là cái gì vậy ? Các nhà văn tưởng tượng ra chăng ? Không phải, “ma chơi” quả là có thật. Nếu các em có dịp đi qua các nghĩa trang vào ban đêm thì các em sẽ thấy tại một số ngôi mộ tỏa ra những ngọn lửa màu xanh lãng đãng lập lòe mà dân gian thường gọi là “ma chơi”. Bài học ngày hôm nay sẽ giúp các em hiểu được hiện tượng này. Đó là bài Photpho.
+ Sau khi học xong bài Photpho giáo viên sẽ giúp học sinh hiểu được hiện tượng trên là do: Trong cơ thể (xương động vật) có chứa một hàm lượng photpho, khi chết phân hủy tạo một phần thành khí PH3 (photphin), khi có lẫn một chút khí P2H4 (điphotphin). Khí PH3 tự bốc cháy ngay trong điều kiện thường tạo thành khối cầu khí (lửa “ma chơi”) bay trong không khí. Bất kể ngày hay đêm đều có PH3 bay ra ở các nghĩa trang, chỉ có điều là ban ngày ánh sáng mặt trời quá mạnh nên ta không thấy được ma chơi.
2PH3 + 4O2 → P2O5 + 3H2O
Điều trùng lặp ngẫu nhiên là : Người ta thường gặp “ma chơi” ở các nghĩa địa vào ban đêm càng tăng thêm tính thần bí và sự mê tính dị đoan.
2.2 . Giáo viên hướng dẫn và rèn luyện cho học sinh phát hiện, giải quyết các vấn đề thực nghiệm trong các bài học có sử dụng thí nghiệm hóa học.
Với đặc thù của môn Hóa học là môn khoa học thực nghiệm, có ứng dụng rất phổ biến trong đời sống và thực tiễn nên việc giảng dạy môn này nhất thiết phải gắn liền với các thí nghiệm thực hành trong một số bài học cụ thể. Thông qua các ví dụ về sử dụng thí nghiệm để giải quyết các tình huống có vấn đề sẽ giúp cho học sinh học tập chủ động, tích cực, hiểu rõ hơn bản chất lí thuyết và thực nghiệm để từ đó hình thành năng lực hành động, giải quyết sáng tạo thực tế trong mọi tình huống mà các em gặp trong đời sống thường ngày.
VÍ DỤ 1: Vấn đề cho dung dịch amoniac tác dụng với muối
GV nêu vấn đề: Tại sao khi cho dung dịch muối nhôm tác dụng với dung dịch amoniac thì thấy sản phẩm tạo thành có xuất hiện kết tủa? còn khi cho dung dịch muối đồng tác dụng với dung dịch amoniac có tạo thành kết tủa hay không? Nếu không thì sản phẩm tạo thành sẽ như thế nào?
Bước 1: Đặt vấn đề để cho HS hiểu rõ bản chất.
– GV làm 2 thí nghiệm biểu diễn: Ống nghiệm 1 đựng dung dịch nhôm clorua
(AlCl3). Ống nghiệm 2 đựng dung dịch đồng sunfat (CuSO4), và lọ đựng dung dịch amoniac NH3.
GV lần lượt nhỏ từ từ dung dịch NH3 vào 2 ống nghiệm trên và yêu cầu học sinh quan sát 2 ống nghiệm và cho biết hiện tượng gì xảy ra? Sản phẩm như thế nào? Có màu gì? GV tiếp tục nhỏ NH3 vào 2 ống nghiệm trên thì thấy sản phẩm ở ống 1 và ống 2 thay đổi so với sản phẩm ban đầu hay không?
HS: phát hiện khi nhỏ từ từ dung dịch NH3 vào 2 ống nghiệm thì: ống nghiệm 1 có xuất hiện kết tủa keo trắng, ống nghiệm 2 xuất hiện kết tủa màu xanh lam. Khi tiếp tục nhỏ dung dịch NH3 đến dư vào 2 ống nghiệm trên thì: ống nghiệm 1 vẫn còn kết tủa keo trắng, ống nghiệm 2 kết tủa tan tạo ra dung dịch màu xanh lam thẫm. HS ngạc nhiên và thắc mắc tại sao có hiện tượng khác nhau đó?
Bước 2: Phát hiện vấn đề
GV nêu câu hỏi:
– Khi tiếp tục nhỏ dung dịch NH3 vào 2 ống nghiệm trên thì xảy ra hiện tượng khác như thế nào so với lúc đầu nhỏ từ từ dung dịch NH3?
– Nếu khác nhau thì chất tạo thành là gì?
– Ngoài những tính chất đã biết thì NH3 còn có thêm tính chất nào nữa?
Bước 3: Xác định phương hướng giải quyết – nêu giả thuyết
– GV yêu cầu HS so sánh 2 ống nghiệm lúc đầu khi cho từ từ dung dịch NH3 vào.
– Để giải quyết câu hỏi NH3 còn có thêm tính chất nào nữa không thì GV cho HS lập luận theo các hướng sau:
+ Màu sắc và hiện tượng giữa 2 ống nghiệm thay đổi như thế nào khi tiếp tục cho dung dịch NH3 vào?
+ Sản phẩm lúc sau có dạng dung dịch hay kết tủa
+ HS viết phương trình phản ứng. Xác định vai trò của NH3 trong phản ứng?
Bước 4: Xác định giả thuyết đúng
– Khi nhỏ từ từ dung dịch NH3 vào 2 ống nghiệm trên thì thấy ở cả 2 ống nghiệm đều xuất hiện kết tủa. Ống nghiệm 1 xuất hiện kết tủa keo trắng, đó là Al(OH)3. Ống nghiệm 2 xuất hiện kết tủa xanh lam, đó là Cu(OH)2.
– Khi ta tiếp tục nhỏ dung dịch NH3 vào thì ống nghiệm 1 thì kết tủa không bị tan đi, còn ống nghiệm 2 kết tủa bị tan ra tạo thành dung dịch màu xanh lam thẫm có dạng phức. Sau đó GV gợi ý cho HS biết dạng phức tạo thành là [Cu(NH3)4]2+.
– HS viết phương trình phản ứng:
AlCl3 + 3NH3 + 3H2O → Al(OH)3↓ + 3NH4Cl
CuSO4 + 2NH3 + 2H2O → Cu(OH)2↓ + (NH4)2SO4
Cu(OH)2 + 4NH3 → [Cu(NH3)4]2+ + 2OH–
– HS: Vậy NH3 có khả năng tạo phức với một số các ion.
Bước 5: Kết luận về lời giải
Ngoài tính chất bazơ yếu ra thì NH3 còn có khả năng tạo phức. Nhưng dung dịch NH3 chỉ có khả năng hòa tan một số hidroxit của kim loại Zn, Cu và muối Ag+ mà thôi. Sự tạo thành các ion phức [Cu(NH3)4]2+ , [Zn(NH3)4]2+, [Ag(NH3)2]+ xảy ra do phân tử amoniac kết hợp với các ion kim loại Cu2+, Zn2+, Ag+ bằng các liên kết cho nhận giữa các cặp electron chưa tham gia liên kết của Nitơ với obitan trống của kim loại.
VÍ DỤ 2: Giải quyết vấn đề tính oxi hóa mạnh của axit nitric HNO3
Trước hết GV nêu vấn đề lớn cho cả bài học: Axit nitric loãng có tác dụng với
kim loại đứng sau hidro trong dãy điện hóa của kim loại không? Nếu xảy ra thì cần điều kiện gì? Axit nitric đặc thì có phản ứng được với kim loại đứng sau hidro không? Nếu có thì điều kiện phản ứng và sản phẩm tạo thành có gì khác so với phản ứng của axit nitric loãng?
Bước 1: Đặt vấn đề để HS hiểu rõ nội dung.
– GV làm thí nghiệm biểu diễn: Ống nghiệm 1 đựng dung dịch HNO3 loãng
Ống nghiệm 2 đựng dung dịch HNO3 đặc
Và ống nghiệm 3 đựng đồng kim loại, GV nêu câu hỏi: Hãy quan sát lá đồng khi chưa cho vào axit thì có màu gì? Màu sắc của hai dung dịch axit?
– HS trả lời: lá đồng màu đỏ, dung dịch axit không màu.
– GV lần lượt cho hai lá đồng vào trong hai ống nghiệm, yêu cầu HS quan sát hiện tượng trong hai ống nghiệm, màu sắc của lá đồng và dung dịch có thay đổi gì không?
– HS: quan sát thấy ở ống nghiệm 1 thì không thấy hiện tượng gì, nhưng ở ống nghiệm 2 thì lá đồng bị xám đen dần, có khí thoát ra màu nâu đỏ, dung dịch chuyển sang màu xanh.
– GV: đun nóng ống nghiệm 1, yêu cầu HS quan sát màu của lá đồng có thay đổi như thế nào? Dung dịch axit có đổi màu gì không?
– HS: quan sát thấy màu dung dịch cũng chuyển dần sang màu xanh giống ống nghiệm 2, lá đồng cũng bị xám đen dần, nhưng khí thoát ra lại không màu, bị hóa nâu ngoài không khí.
Bước 2: Nêu vấn đề: GV nêu các câu hỏi:
– Ở nhiệt độ thường dung dịch HNO3 loãng có tác dụng với Cu không? ở điều kiện nào thì phản ứng xảy ra? Còn đối với dung dịch HNO3 đặc thì sao?
– Khí tạo thành có phải là khí H2 không? Nếu không phải thì là khí nào?
– Ngoài tính chất đã biết thì HNO3 còn có thêm tính chất nào khác?
Bước 3: Xác định phương hướng giải – nêu giả thuyết
– GV yêu cầu HS so sánh 2 ống nghiệm khi tác dụng với Cu khi không đun nóng và đun nóng?
– Hãy xác định khí sinh ra là khí gì mà có màu nâu đỏ khi cho Cu tác dụng với dung dịch HNO3 đặc, và khí nào không màu lại hóa nâu ngoài không khí khi cho Cu tác dụng với dung dịch HNO3 loãng?
– Dung dịch trong hai ống nghiệm đều có màu gì? Đó có phải màu đặc trưng của dung dịch muối đồng không?
– Hãy viết phương trình phản ứng? nhận xét bản chất của phản ứng? Chất nào là chất khử? Chất nào là chất oxi hóa? Từ đó, kết luận gì thêm về tính chất của dung dịch HNO3?
Bước 4: Xác định một giả thuyết đúng
– Dung dịch axit HNO3 loãng không tác dụng được với Cu, chỉ tác dụng khi đun nóng còn dung dịch HNO3 đặc có thể tác dụng với Cu kể cả khi không đun nóng.
– Chất khí sinh ra ở ống nghiệm 1 là khí không màu, bị hóa nâu trong không khí không phải là khí H2 mà là khí NO. Còn khí sinh ra ở ống nghiệm 2 có màu nâu đỏ là khí NO2.
– Dung dịch tạo thành màu xanh là dung dịch đồng nitrat Cu(NO3)2.
– HS viết phương trình phản ứng:
3Cu + 8HNO3 loãng, nóng → 3Cu(NO3)2 + 2NO↑ + 4H2O
Cu + 4HNO3 đặc → Cu(NO3)2 + 2NO2↑ + 2H2O
Trong cả 2 phương trình phản ứng thì Cu đóng vai trò là chất khử, HNO3 đóng vai trò là chất oxi hóa.
GV: dung dịch HNO3 là một trong những axit có tính oxi hóa mạnh. Đây là tính chất mới, khác với những tính chất của axit mà chúng ta đã biết. Phản ứng giữa kim loại với axit nitric là phản ứng oxi hóa – khử.
Bước 5: Kết luận về lời giải
GV chỉnh lý, bổ sung và đưa ra những kiến thức cần lĩnh hội:
– Ngoài tính axit mạnh thì HNO3 còn có tính oxi hóa mạnh, nó có thể oxi hóa hầu hết các kim loại (trừ Au, Pt), khi đó kim loại sẽ bị oxi hóa đến mức hóa trị cao nhất tạo thành muối nitrat.
– Tùy nồng độ axit và bản chất của chất khử mà axit HNO3 có thể bị khử đến các sản phẩm khác nhau của nitơ. Chẳng hạn: tác dụng với các kim loại có tính khử yếu như Cu, Ag,… axit HNO3 đặc bị khử đến NO2, còn axit HNO3 loãng thì bị khử đến NO. Còn đối với những kim loại mạnh hơn như Mg, Al, Zn,.. axit HNO3 loãng có thể bị khử tới N2O (khí gây cười), N2 (khí không duy trì sự cháy, nhẹ hơn không khí), NH4NO3 (không sinh ra khí, nhưng khi cho kiềm vào dung dịch sản phẩm thì có khí mùi khai thoát ra).
– Sản phẩm khí của nitơ thường rất độc nên phải dùng miếng bông tẩm xút để đậy lọ ống nghiệm.
– Đặc biệt Fe, Al, Cr bị thụ động hóa trong dung dịch axit HNO3 đặc, nguội.
Bước 6: Kiểm tra lại kiến thức cần tiếp thu và dạy cho HS vận dụng kiến thức.
– Cho HS kiểm tra vấn đề đã tiếp thu bằng cách cho HS thực hiện các thí nghiệm: Cho axit HNO3 loãng, axit HNO3 đặc tác dụng với Zn, Mg, Al. Giải thích hiện tượng và viết phương trình phản ứng.
– So sánh tính chất của axit HNO3 với axit H2SO4 đã học.
VÍ DỤ 3: Giải quyết vấn đề về sự nhiệt phân của một số muối nitrat
Bước 1: Đặt vấn đề
Muối nitrat dễ bị nhiệt phân, nhưng có phải nhiệt phân muối nào cũng cho sản phẩm như nhau?
– GV tiến hành 2 Thí nghiệm:
Thí nghiệm 1: Nung nóng ống nghiệm 1 đựng muối rắn NaNO3
Thí nghiệm 2: Nung nóng ông nghiệm 2 đựng muối rắn Cu(NO3)2
Sau đó đặt lên miệng 2 ống nghiệm que đóm đỏ, tiếp tục cho một ít axit H2SO4 loãng vào 2 ống nghiệm. GV yêu cầu HS quan sát hiện tượng xảy ra ở 2 ống nghiệm.
– HS: Cả 2 ống nghiệm đều có khí thoát ra. Ống nghiệm thứ 2 có kết tủa đen, có khí thoát ra màu nâu đỏ bay lên và que đóm đỏ bùng cháy. Khi cho một ít dung dịch axit H2SO4 loãng vào ống nghiệm 1 thì thấy có khí màu nâu đỏ thoát ra. Còn ở ống nghiệm thứ 2 thì ta thấy kết tủa đen tan ra và dung dịch có màu xanh.
Bước 2: Phát biểu vấn đề
– Khi đun nóng 2 ống nghiệm có đựng 2 muối trên và đặt que đóm đỏ trên miệng ống nghiệm thì thấy có hiện tượng gì?
– Sản phẩm tạo thành có kết tủa không? Nếu không thì dung dịch có màu gì?
– Khí thoát ra có màu gì?
– Tại sao phải cho H2SO4 loãng vào để chứng tỏ thêm điều gì?
Bước 3: Xác định phương hướng giải quyết – nêu giả thuyết
– GV yêu cầu HS so sánh xem sự nhiệt phân của 2 muối thì sản phẩm tạo thành có giống nhau không?
– Chất khí bay ra làm que đóm đỏ bùng cháy, đó là khí gì? Có phải khí oxi không? Khí khác tạo thành có màu nâu đỏ đó là khí gì?
– Kết tủa tạo thành ở thí nghiệm 2 là kết tủa nào? Màu gì?
– Khi cho một ít dung dịch axit H2SO4 loãng vào 2 ống nghiệm thì:
+ Ống nghiệm 1: xuất hiện chất khí màu nâu đỏ? Đó là khí nào?
+ Ống nghiệm 2: dung dịch có màu xanh là dung dịch gì? Có phải màu xanh đặc trưng của dung dịch muối đồng không?
Bước 4: Xác định một giả thuyết đúng
– HS: Muối nitrat khi nhiệt phân đều tạo ra 1 khí làm que đóm đỏ bùng cháy, khí đó chính là khí oxi.
– HS: Khí sinh ra có màu nâu đỏ chính là khí NO2, kết tủa đen trong ống nghiệm thứ 2 là CuO, CuO tan trong dung dịch H2SO4 loãng tạo dung dịch muối có màu xanh là muối đồng sunfat CuSO4
CuO + H2SO4 → CuSO4 + H2O
– HS: Sau khi nung nóng ở thí nghiệm 1 ta cũng cho thêm một ít axit H2SO4 thì cũng thấy xuất hiện khí màu nâu đỏ NO2 xuất hiện trên miệng ống nghiệm.
6NaNO2 + 3H2SO4 → 3Na2SO4 + 6HNO2
6HNO2 → 2HNO3 + 4NO + 2H2O
2NO + O2 → 2NO2
– HS viết phương trình phản ứng đầy đủ:
2NaNO3 → 2NaNO2 + O2
2Cu(NO3)2 → 2CuO + 4NO2 + O2
Đây là tính chất nhiệt phân của muối nitrat
Bước 5: Kết luận về lời giải
GV nêu ra lý thuyết cần lĩnh hội: Muối nitrat dễ bị nhiệt phân, sản phẩm của phản ứng tùy thuộc vào bản chất của cation tạo muối đó:
– Muối nitrat của kim loại hoạt động mạnh (đứng trước Mg) phân hủy tạo thành muối nitrit và khí oxi.
– Muối nitrat của kim loại hoạt động (Mg, Al,…, Cu) phân hủy tạo oxit kim loại, nitơ đi oxit, khí oxi.
– Muối nitrat của kim loại kém hoạt động (Hg, Ag,…) phân hủy tạo thành kim loại, nitơ đioxit và khí oxi.
Bước 6: Kiểm tra kiến thức vừa tiếp thu và dạy HS vận dụng kiến thức
GV cho HS tiến hành thí nghiệm với một số muối khác với cùng điều kiện phản ứng với thí nghiệm trên, ví dụ như KNO3, Mg(NO3)2, AgNO3,… HS quan sát hiện tượng và viết phương trình phản ứng.
VÍ DỤ 4: Nhận biết ion nitrat
Bước 1: Đặt vấn đề
Như chúng ta đã biết, axit HNO3 có tính oxi hóa mạnh do nguyên tử nitơ có độ âm điện lớn và có số oxi hóa cao nhất (+5). Vậy ion NO3– có tính oxi hóa mạnh hay không?
Bước 2: Nêu tình huống có vấn đề
+ Cho Cu tác dụng với dung dịch HCl → không xảy ra (do Cu là kim loại đứng sau H nên không khử được H+).
+ Cho Cu tác dụng với dung dịch NaNO3 → không xảy ra (do Cu là kim loại đứng sau Na nên không khử được Na+.
+ Cho Cu tác dụng với hỗn hợp dung dịch HCl và dung dịch NaNO3 → có xảy ra phản ứng
Bước 3: Hướng dẫn HS tự giải quyết vấn đề
GV yêu cầu HS viết dạng phương trình phân tử và phương trình ion thu gọn của phản ứng Cu tác dụng với dung dịch HNO3.
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
3Cu + 8H+ + 2NO3– → 3Cu2+ + 2NO + 4H2O
GV yêu cầu HS nêu các thành phần của phản ứng:
Cu + NaNO3 + HCl = Cu + Na+ + NO3– + H+ + Cl–.
HS nhận thấy cũng có Cu, NO3–, H+ nên có xảy ra phương trình:
3Cu + 2NaNO3 + 8HCl → 3CuCl2 + 2NaCl + 2NO + 4H2O
Bước 4: Kết luận
Trong môi trường axit thì ion NO3– có khả năng oxi hóa mạnh như HNO3
2.3. Giáo viên lựa chọn và xây dựng hệ thống bài tập có nhiều cách giải và có cách giải ngắn gọn, độc đáo nhất trong các tiết luyện tập, ôn tập cuối chương và trong kiểm tra đánh giá.
Việc sử dụng bài tập Hóa học nhiều cách giải trong các tiết học không những giúp học sinh củng cố kiến thức, rèn luyện kỹ năng giải bài tập Hóa học mà còn góp phần rèn luyện một số kỹ năng mềm cho học sinh như kỹ năng tư duy độc lập, kỹ năng hoạt động nhóm, kỹ năng trình bày, thuyết trình một vấn đề,… Qua thực tế giảng dạy tôi thấy rằng các tiết học sử dụng bài tập có nhiều cách giải giúp cho lớp học có không khí học tập sôi nổi, tập trung hơn và chất lượng bài dạy cao hơn. Có thể sử dụng loại bài tập này trong việc kiểm tra miệng và kiểm tra viết một tiết. Khi kiểm tra miệng, giáo viên yêu cầu học sinh giải một bài tập nào đó, sau khi hoàn thành giáo viên có thể đặt thêm câu hỏi: Bài này còn có cách giải nào khác không? Qua đó giúp giáo viên đánh giá được mức độ nắm vững kiến thức và khả năng tư duy của học sinh, tránh tình trạng đánh giá sai lệch do học sinh học thuộc một bài giải rồi lên bảng chép lại một cách máy móc.
Đối với bài kiểm tra viết một tiết, giáo viên có thể yêu cầu học sinh trình bày việc giải bài toán ít nhất 2 cách khác nhau. Đối với học sinh xuất sắc, khi làm bài kiểm tra thường làm bài xong sớm hơn nên sử dụng yêu cầu này bắt buộc học sinh phải tiếp tục tư duy và làm bài, qua đó hạn chế được sự không nghiêm túc trong kiểm tra như chỉ bài cho bạn bên cạnh. Điều này giúp giáo viên đánh giá kết quả học tập của mỗi học sinh chính xác và toàn diện hơn.
Ví dụ minh họa: Kiểm tra 15 phút phần axit HNO3 ( Hóa 11 THPT)
Đề bài:
Cho 3,90 gam hỗn hợp A gồm Mg và Al tác dụng vừa đủ với dung dịch HNO3
loãng thì thu được dung dịch X và 0,896 lít khí N2 (là sản phẩm khử duy nhất, đo
ở đktc).
- Viết phương trình phản ứng xảy ra? (2,0 điểm)
- Tính % khối lượng của Mg và Al trong A? (3,0 điểm)
- Cho dung dịch X tác dụng với 400 ml dung dịch KOH 1,05M, tính khối lượng kết tủa thu được sau phản ứng? (3,0 điểm)
- Giải bài tập trên theo các cách khác nhau? (2,0 điểm)
Đáp án:
| Các ý:
|
a. Viết phương trình phản ứng
b. Đặt ẩn, lập hệ phương trình và giải
Tính được %Mg và %Al
c. Khối lượng kết tủa
– Cách 1: giải theo phương trình phản ứng
– Cách 2: cách giải nhanh áp dụng định luật bảo toàn electron.
– Cách 3: áp dụng phương pháp quy đổi.
d. Cách khác |
2,0 đ
3,0 đ
3,0 đ
2,0 đ |
* Nhận xét: Với bài toán nhiều cách giải như trên ta có thể đánh giá được trình độ của học sinh. Học sinh trung bình có thể giải được cách 1, học sinh khá có thể giải được cách 2 hoặc cách khác, học sinh giỏi có thể giải được nhiều cách, ít nhất là 3 cách. Vì vậy kết quả điểm bài kiểm tra sẽ đánh giá đúng năng lực của học sinh, có độ tin cậy cao.
Trong các tiết tự chọn, giáo viên có thể tổ chức dạy học bằng cách sử dụng bài tập có nhiều cách giải dưới dạng tổ chức một trò chơi hoặc một cuộc thi. Chẳng hạn, giáo viên có thể sử dụng hai hình thức. Hình thức thứ nhất là trò chơi “thách đố”: Giáo viên đưa ra một bài tập, lần lượt cho học sinh “thách đố” có thể giải được bài toán đó bao nhiêu cách, học sinh giải được nhiều cách nhất sẽ thắng cuộc và được giáo viên đánh giá bằng điểm số tối đa. Hoặc có thể cho mỗi học sinh chỉ đưa ra một cách giải mà cho là hay nhất, sau đó giáo viên tổ chức cho cả tập thể bình chọn ai là người đưa ra cách giải nhanh và hay nhất.
Hình thức thứ hai là giáo viên chia lớp học thành 4 nhóm, giao nhiệm vụ cho từng nhóm là về nhà sưu tầm hoặc biên soạn bài tập có nhiều cách giải theo chủ đề kiến thức cho trước. Khi đến tiết học, lần lượt từng nhóm đưa ra bài tập và yêu cầu các nhóm còn lại giải. Giáo viên đánh giá, nhận xét về việc chuẩn bị bài tập của từng nhóm, về các cách giải khác nhau và có hình thức động viên khen thưởng phù hợp.
Ở trường phổ thông hiện nay, trong chương trình học có tổ chức dạy học các chủ đề tự chọn. Tuy nhiên, thực tế cho thấy việc tổ chức dạy học tự chọn của nhiều GV còn đơn giản và nhàm chán. Chẳng hạn như GV chỉ ra đề bài tập rồi yêu cầu học sinh giải hoặc giáo viên hướng dẫn giải. Việc làm này lặp đi lặp lại trong một tiết và qua nhiều tiết gây chán nản cho HS. Bởi vậy, việc tổ chức dạy học tự chọn kết hợp với trò chơi như trên sẽ giúp HS hứng thú, phấn khởi và qua đó hiệu qủa đạt được cao hơn. Việc lựa chọn và xây dựng hệ thống bài tập có nhiều cách giải về Nitơ – Photpho góp phần phát triển năng lực thực hành sáng tạo cho HS, đặc biệt là đối tượng học sinh giỏi. Sau đây tôi xin được giới thiệu một số ví dụ minh họa cụ thể.
Bài tập 1: Hòa tan hết m gam hỗn hợp X gồm FeO, Fe2O3, Fe3O4 bằng dung dịch HNO3 đặc nóng dư thu được 4,48 lit khí NO2 ( đktc, sản phẩm khử duy nhất) và dung dịch X. Cô cạn dung dịch X được 145,2 gam muối khan. Tính m?
Các cách giải:
Cách 1: Giải theo phương trình phản ứng:
Gọi x, y, z lần lượt là số mol của FeO, Fe3O4, Fe2O3 trong m gam hỗn hợp X
Các phản ứng xảy ra :
FeO + 4HNO3 → Fe(NO3)3 + NO2 + 2H2O (1)
Fe3O4 + 10HNO3 → 3Fe(NO3)3 + NO2 + 5H2O (2)
Fe2O3 + 6HNO3 → 2Fe(NO3)3 + 3H2O (3)
Giả thiết cho số mol NO2 = 0,2 mol và số mol Fe(NO3)3 = 0,6 mol
Theo phương trình (1) ; (2) ; (3) ta có :
x + 3y + 2z = 0,6 => 10x + 30 y + 20 z = 6 (1) và x + y = 0,2 (2)
Lấy (1) – (2), ta được : 9x + 29 y + 20 z = 5,8
=> 72x + 232 y + 160 z = 46,4 g.
Vậy m = 46,4 gam
Cách 2: Áp dụng định luật bảo toàn mol electron và bảo toàn khối lượng đối với hỗn hợp X :
Theo định luật bảo toàn khối lượng : mX = mFe + mO
Mặt khác, ta có nFe = 0,6 mol => mFe = 0,6 . 56 = 33,6 (g)
=> mX = mO + 33,6 (g) => mO = m – 33,6 (g) => số mol O = (m- 33,6)/16 mol
Áp dụng định luật bảo toàn mol e : số mol e nhường = số mol e nhận ta có
Fe – 3e à Fe3+ O + 2e à O2-
N+5 + 1e à N+4 (NO2)
=> 0,6 . 3 = (m- 33,6)/16.2 + 0,2.1
=> m = 46,4 gam
Cách 3: Áp dụng định luật bảo toàn khối lượng đối với toàn bộ quá trình và bảo toàn nguyên tố H
Ta có X + HNO3 → Fe(NO3)3 + NO2 + H2O
Theo định luật bảo toàn khối lượng, ta có :
=>
Theo bảo toàn nguyên tố H, ta lại có :
→ mX = 145,2 + 0,2.46 + 18 – 126 = 46,6 gam
Cách 4: Qui đổi hỗn hợp X thành hỗn hợp X’ : FeO và Fe2O3 hoặc Fe và Fe2O3 hoặc FeO và Fe3O4 ; hoặc Fe và FeO hoặc Fe và Fe3O4.
Ở đây ta qui đổi hỗn hợp X thành hỗn hợp X’ gồm FeO và Fe2O3.
Gọi x, y lần lượt là số mol của FeO và Fe2O3 trong X’. Phản ứng xảy ra :
FeO + 4 HNO3 → Fe(NO3)3 + NO2 + 2 H2O (1)
x → x → x
Fe2O3 + 6 HNO3 → 2 Fe(NO3)3 + 3 H2O (2)
y → 2y
Từ phương trình, ta có x + 2y = 0,6 và x = 0,2
suy ra x = 0,2 mol và y = 0,2 mol.
Vậy m = 72 x + 160 y = 0,2.72 + 160.0,2 = 46,4 gam
Cách 5: Sử dụng công thức kinh nghiệm :
Sử dụng công thức kinh nghiệm, ta có :
mX = (10mFe – 56ne)/7 = (10.0,6.56 – 56.0,2)/7 = 46,4 gam
Cách 6: Giải bằng phương pháp trung bình :
Gọi công thức chung của các oxit là : Fex Oy , ta có :
Fex Oy + (2 + 2y)H+ + NO3– → xFe3+ + NO2 + (y + 1) H2O
Áp dụng định luật bảo toàn điện tích 2 vế ta có :
2 + 2y – 1 = 3x → 3x – 2y = 1 (1)
Ta lại có : số mol Fe3+ = x. số mol NO2 → 0,6 = 0,2x → x = 3 (2)
Từ (1) và (2) suy ra x = 3 và y = 4, Vậy mX = (56x + 16y). 0,2 = 46,4 gam
Cách 7: Giải theo hóa trị trung bình của sắt :
Gọi hóa trị trung bình của sắt trong cả hỗn hợp X là x. Khi đó công thức của X là : Fe2Ox
Áp dụng định luật bảo toàn mol- e cho phản ứng của X với HNO3, ta có:
Fe+x → Fe+3 + (3 – x )e và N+5 + 1e → N+4
Ta lại có : số mol Fe+3 = 0,6 mol suy ra 0,6.(3 – x ) = 0,2.1 → x = 8/3
Mặt khác, theo bảo toàn nguyên tố Fe, ta có:
Số mol Fe2Ox = ½ .số mol Fe3+ = 0,3 mol
Vậy mX = 0,3. (56.2 + 16.8/3) = 46,4 gam
Cách 8: Giải theo bảo toàn nguyên tố oxi
Ta có số mol Fe(NO3)3 = 0,6 mol và số mol NO2 = 0,2 mol
Suy ra số mol HNO3 phản ứng = 0,6.3 + 0,2 = 2 mol → số mol H2O = 1 mol
Hỗn hợp X ( FeO,Fe2O3, Fe3O4) + HNO3 Fe(NO3)3 + NO2 + H2O
Áp dụng định luật bảo toàn nguyên tố O, ta có:
Số mol O trong X = số mol O trong Fe(NO3)3 + số mol O trong NO2 + số mol O trong H2O – số mol O trong HNO3
Suy ra : mX – mFe = 0,6.9.16 + 0,2.2.16 +1.16 – 2.3.16 = 12,8
=> mX = 12,8 + 0,6.56 = 46,4 gam
Hoặc xem bản đầy đủ trên google drive: TẠI ĐÂY
Các thầy cô cần file word liên hệ với chúng tôi tại fanpage facebook O2 Education
Hoặc xem nhiều SKKN hơn tại: Tổng hợp SKKN môn hóa học cấp THPT
Hoặc xem thêm các tài liệu khác của môn hóa





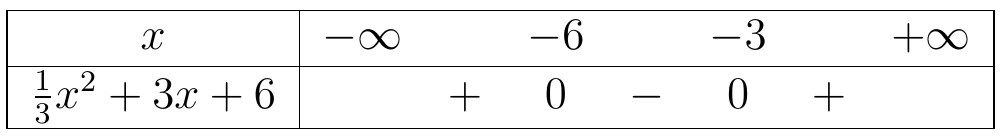
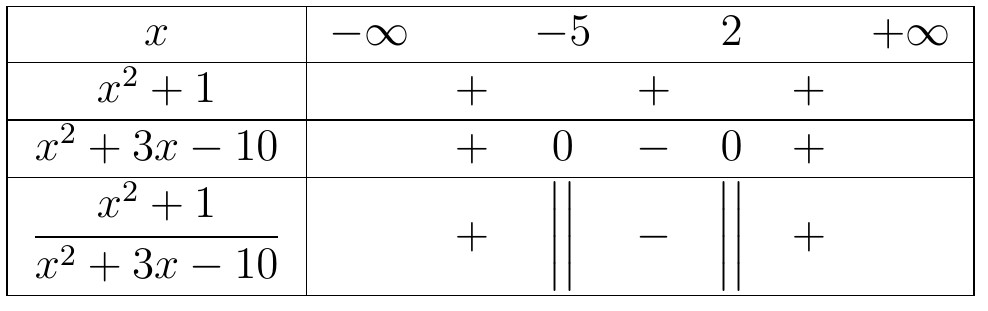 Kết luận, tập nghiệm của bất phương trình là $S=(-5;2)$.
Kết luận, tập nghiệm của bất phương trình là $S=(-5;2)$. Kết luận, tập nghiệm của bất phương trình là $S=(-5;3)$.
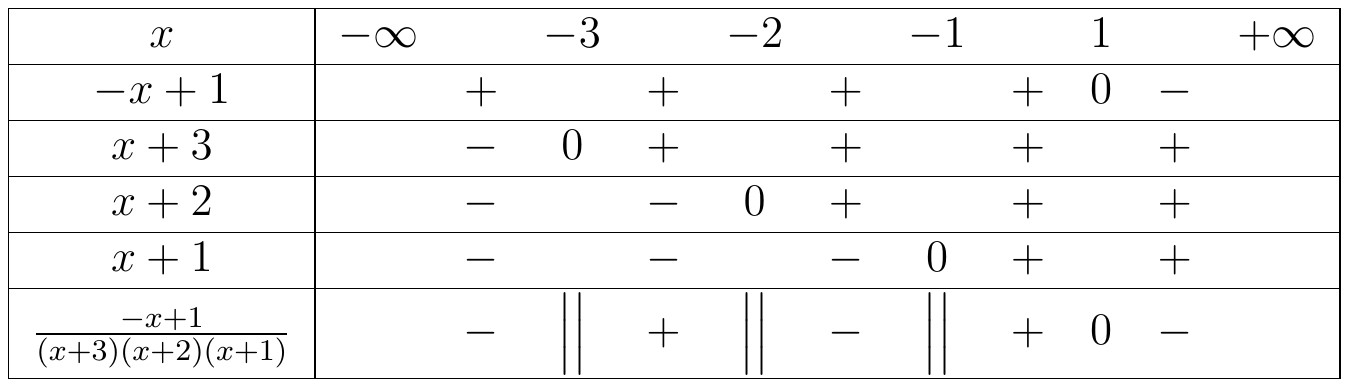
Kết luận, tập nghiệm của bất phương trình là $S=(-5;3)$.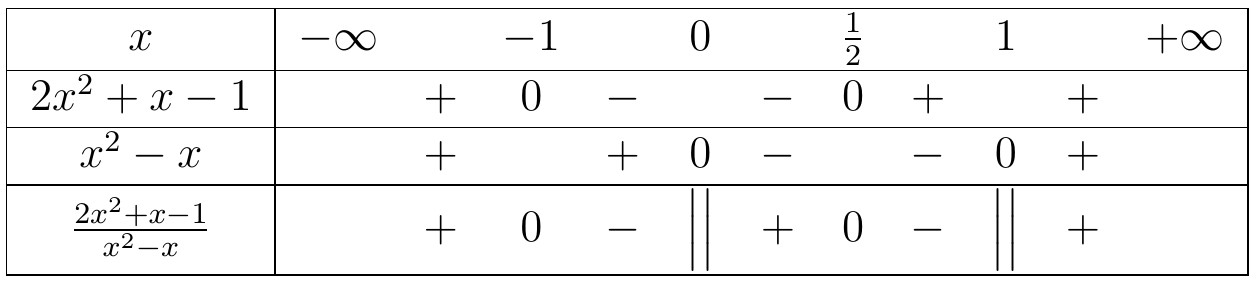 Kết luận, tập nghiệm của bất phương trình đã cho là $S= \left( -\infty ,-1\right) \cup \left( 0,\frac{1}{2}\right) \cup \left( 1,+\infty \right) $.
Kết luận, tập nghiệm của bất phương trình đã cho là $S= \left( -\infty ,-1\right) \cup \left( 0,\frac{1}{2}\right) \cup \left( 1,+\infty \right) $.