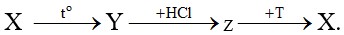Đề thi thử tốt nghiệp THPT 2022 môn hóa THPT chuyên Lê Quý Đôn Đà Nẵng Lần 1 có đáp án
chuyên Lê Quý Đôn – Đà Nẵng (Lần 1)
⇒ Mã đề: 089
| 41B | 42B | 43C | 44C | 45D | 46B | 47A | 48A | 49A | 50D |
| 51A | 52D | 53D | 54C | 55A | 56D | 57C | 58C | 59A | 60B |
| 61A | 62B | 63C | 64D | 65B | 66D | 67D | 68D | 69B | 70C |
| 71B | 72A | 73A | 74C | 75B | 76B | 77D | 78B | 79C | 80B |
Câu 41: Este nào sau đây có mùi dầu chuối?
A. etyl butyrat. B. isoamyl axetat. C. benzyl fomat. D. metyl salixylat.
Câu 42: Hỗn hống là hợp kim của thủy ngân với các kim loại khác. Để điều chế H2 người ta dùng hỗn hống
A. bạc. B. natri. C. vàng. D. đồng.
Câu 43: Natri cháy trong không khí khô tạo ra natri peoxit. Natri peoxit có công thức
A. NaOH. B. Na2O. C. Na2O2. D. NaO2.
Câu 44: Vietnam Airlines sẽ phục vụ hành khách thêm khăn lau tay kháng khuẩn để bảo vệ sức khỏe hành khách trước dịch Covid-19 trên tất cả chuyến bay của Hãng. Điểm đặc biệt của loại khăn mới này có chứa ancol isopropylic nồng độ 65%. Công thức của ancol isopropylic là
A. CH3OH. B. CH3CH2CH2OH. C. CH3-CH(OH)-CH3. D. CH3CH2OH.
Câu 45: Thạch cao nung được dùng để nặn tượng, đúc khuôn và bỏ bột khi gãy xương. Thạch cao nung có công thức
A. CaSO4. B. CaO. C. CaSO4.2H2O. D. CaSO4.H2O.
Câu 46: Kim loại M có cấu hình electron nguyên tử là [Ne] 3s2 3p1. Số electron hóa trị của M là
A. 13. B. 3. C. 1. D. 2.
Câu 47: Hệ thống túi khí (Supplementary Restraint System – SRS) là thiết bị thụ động được trang bị để hạn chế tổn thương cho người ngồi trên xe khi có tai nạn xảy ra. Khi va chạm đủ mạnh, khí X sinh ra trong túi khí bởi sự phân hủy NaN3. Khí này cũng có trong thành phần của không khí. Khí X là
A. N2. B. O2. C. CO2. D. NH3.
Câu 48: Tơ nitron dai, bền với nhiệt và giữ nhiệt tốt nên thường được dùng để dệt vải may quần áo ấm hoặc bên thành sợi “len” đan áo rét. Tơ nitron là sản phẩm trùng hợp của
A. CH2=CH-CN. B. CH2=CH2. C. CH2=CH-CH3. D. CH2=CH-Cl.
Câu 49: Chất nào sau đây không phản ứng với nước brom?
A. Hexan. B. Glucozơ. C. Phenol. D. Anilin.
Câu 50: Chất nào sau đây không tham gia phản ứng thủy phân?
A. Xenlulozơ. B. Saccarozơ. C. Tinh bột. D. Glucozơ.
Câu 51: Muối nào sau đây khi thủy phân trong nước cho dung dịch có môi trường kiềm?
A. Na2CO3. B. NaCl. C. KHSO4. D. Al2(SO4)3.
Câu 52: Chất nào sau đây có lực bazơ yếu nhất?
A. dimetylamin. B. amoniac. C. metylamin. D. anilin.
Câu 53: C7H8O có bao nhiêu chất có chứa vòng benzen?
A. 3. B. 4. C. 6. D. 5.
Câu 54: Chất nào cho dưới đây, khi phản ứng với dung dịch HCl hoặc dung dịch NaOH đều giải phóng khí?
A. Al(OH)3. B. Al2O3. C. Al. D. NaHCO3.
Câu 55: DHA (docosahexaenoic acid) là một loại axit béo không no có 6 liên kết đôi C=C. Công thức phân tử của DHA là.
A. C22H32O2. B. C20H34O2. C. C22H34O2. D. C22H32O4.
Câu 56: Polyme nào dưới đây không có nhóm chức este?
A. poly(metyl metacrylat). B. Poly (vinyl axetat).
C. Poli(etylen terephtalat). D. poli(hexametylen adipamit).
Câu 57: Cho dãy chuyển hóa:
Chất T là
A. propyl fomat. B. axit butyric. C. etyl axetat. D. metyl propionat.
Câu 58: Nạp đầy khi amoniac vào bình thuỷ tinh trong suốt, đậy bình NH3 bằng nút cao su có ống thuỷ tinh vuốt nhọn xuyên qua. Nhúng đầu ống thuỷ tinh vào một chậu thuỷ tinh chứa nước có pha thêm dung dịch phenolphtalein. Một lát sau, nước trong chậu phun vào bình thành những tia có màu hồng. Thí nghiệm này chứng tỏ được
A. NH3 tan nhiều trong nước. B. NH3 là chất khí.
C. NH3 có tính bazơ và tan nhiều trong nước. D. NH3 có mùi khai.
Câu 59: Xét sơ đồ chuyển hóa:
Tên của Z là
A. axit stearic. B. axit panmitic. C. axit linoleic. D. Glyxerol.
Câu 60: Khi điện phân NaCl nóng chảy (điện cực trơ), tại catot xảy ra
A. sự oxi hóa ion Cl-. B. sự khử ion Na+. C. sự oxi hóa ion Na+. D. sự khử ion Cl-.
Câu 61: Xét sự ăn mòn gang trong không khí ẩm, phát biểu nào sau đây không đúng?
A. Fe là cực dương, electron dịch chuyên từ cực dương đến cực âm.
B. Gỉ sắt có thành phần chủ yếu là Fe2O3.nH2O.
C. Tại catot, O2 hòa tan trong nước bị khử thành ion hiđroxit.
D. Tại anot, sắt bị oxi hóa thành ion sắt.
Câu 62: Xét các dung dịch NaCl, NaOH, NaHCO3 và Na2CO3. Phát biểu nào dưới đây là đúng?
A. Có hai dung dịch tạo kết tủa với BaCl2 (không đun nóng).
B. Có hai dung dịch tạo kết tủa với Ca(OH)2.
C. Có hai dung dịch có môi trường kiềm.
D. Có hai chất phản ứng với dung dịch HCl.
Câu 63: Cho chất X có công thức phân tử C6H16O4N2 tác dụng hết với dung dịch NaOH thu được muối (COONa)2; và giải phóng amin C2H7N. Số công thức cấu tạo của X:
A. 2. B. 5. C. 3. D. 4.
Câu 64: Cho 25 ml dung dịch FeSO4 2M tác dụng vừa đủ với V ml dung dịch KMnO4 0,5M trong môi trường H2SO4. Giá trị của V là:
A. 80. B. 40. C. 100. D. 20.
Câu 65: Xà phòng hóa hoàn toàn 8,8 gam este E có công thức C4H8O2 bằng dung dịch NaOH, đun nóng thu được 6,8 gam muối và m gam một ancol. Giá trị của m bằng
A. 4,6. B. 6,0. C. 2,3. D. 3,2.
Câu 66: Phát biểu nào sau đây là sai?
A. Glucozơ tồn tại chủ yếu ở hai dạng mạch vòng α-glucozơ và β-glucozơ.
B. Khi có enzim xúc tác, glucozơ trong dung dịch lên men cho ancol etylic và khí CO2.
C. Dẫn khí H2 vào dung dịch glucozơ đun nóng, có Ni làm xúc tác, thu được sobitol.
D. Dung dịch AgNO3 trong NH3 khử glucozơ thành amoni gluconat.
Câu 67: Cho m gam hỗn hợp X gồm etylen glicol và glyxerol tác dụng hết với kim loại Na dư, khi phản ứng xảy ra hoàn toàn thu được 13,44 lít khí H2 (đktc). Giá trị m chỉ có thể là
A. 37,2. B. 38,4. C. 36,0. D. 36,9.
Câu 68: Cho 4,6 gam Na vào 100 ml dung dịch HCl 1M được dung dịch X, cô cạn dung dịch X được m gam chất rắn khan. Giá trị m bằng
A. 7,85. B. 5,85. C. 11,7. D. 9,85.
Câu 69: Điện phân dung dịch 200 ml dung dịch CuSO4 1M trong thời gian 2 giờ với cường độ dòng điện l = 1,34A thu được dung dịch X. Cho 14 gam Fe vào dung dịch X, khi phản ứng xảy ra hoàn toàn, thu được m gam kim loại. Giá trị của m bằng
A. 9,6. B. 12,4. C. 2,8. D. 9,2.
Câu 70: Xét các phát biểu sau
(1) Trong máu người bình thường có một lượng nhỏ glucozơ với nồng độ khoảng 0,1%.
(2) Saccarozơ thủy phân cho glucozơ và fructozơ.
(3) Xenlulozơ trinitrat rất dễ cháy và nổ mạnh không sinh khói nên được dùng làm thuốc súng không khói.
(4) Mononatri glutamat dùng là gia vị thức ăn (gọi là mì chính hay bột ngọt)
(5) Hòa tan lòng trắng trứng vào nước, sau đó đun sôi, lòng trắng trứng sẽ đông tụ lại.
Số phát biểu đúng là
A. 4. B. 3. C. 5. D. 2.
Câu 71: Hòa tan hoàn toàn 21 gam hỗn hợp X gồm Al2O3 và Al vào 600 ml dung dịch NaOH 2M, được V lít khí H2 (đktc) và dung dịch Y có chứa hai chất tan có cùng nồng độ mol. Giá trị V là
A. 20,16. B. 13,44. C. 11,2. D. 8,96.
Câu 72: Hòa tan 17,24 gam hỗn hợp X gồm Ca, CaC2, Al và Al4C3 vào nước (dư), sau phản ứng xảy ra hoàn toàn, thu được hỗn hợp khí Y và dung dịch Z trong suốt, chỉ chứa 2 chất tan có cùng nồng độ mol. Đốt cháy hoàn toàn Y cần vừa đủ 12,768 lít O2 (đktc), thu được m gam hỗn hợp CO2 và H2O. Giá trị của m là
A. 23,08. B. 18,58. C. 18,68. D. 22,0.
Câu 73: Tiến hành thí nghiệm theo các bước sau:
Bước 1: Cho 1 ml dung dịch AgNO3 1% vào ống nghiệm sạch.
Bước 2: Thêm từ từ từng giọt dung dịch NH3, lắc đều cho đến khi kết tủa tan hết.
Bước 3: Thêm tiếp khoảng 1 ml dung dịch glucozơ 1% vào ống nghiệm; đun nóng nhẹ.
Phát biểu nào sau đây sai?
A. Sản phẩm hữu cơ thu được sau bước 3 là sobitol.
B. Thí nghiệm trên chứng minh glucozơ có tính chất của anđehit.
C. Sau bước 3, có lớp bạc kim loại bám trên thành ống nghiệm.
D. Ở bước 3, có thể thay việc đun nóng nhẹ bằng cách ngâm ống nghiệm trong nước nóng.
Câu 74: Xét các thí nghiệm sau:
(1) Cho khí H2S vào dung dịch FeCl3.
(2) Cho dung dịch AgNO3 vào dung dịch FeSO4.
(3) Cho dung dịch H3PO4 và dung dịch AgNO3.
(4) Cho CO2 vào dung dịch nước vôi trong dư.
Số thí nghiệm có kết tủa tạo ra là
A. 4. B. 2. C. 3. D. 1.
Câu 75: Cho m gam Mg vào dung dịch chứa 0,2 mol AgNO3 và 0,25 mol Cu(NO3)2, sau một thời gian thu được 33,6 gam kết tủa và dung dịch X chứa 2 muối. Tách lấy kết tủa, thêm 8,4 gam bột sắt vào dung dịch X, sau khi các phản ứng xảy ra hoàn toàn thu được 9,2 gam kết tủa. Giá trị của m bằng
A. 6. B. 8,4. C. 12. D. 10,8.
Câu 76: Hỗn hợp X gồm tất cả các hiđrocacbon mạch hở của C3Hy. Tỉ khối hơi của X so với H2 bằng 20,5. Trộn 3,36 lít hỗn hợp X với 2,24 lít H2 trong bình kín (có mặt xúc tác Ni) rồi đun nóng đến khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp Z. Toàn bộ lượng Z trên phản ứng được với tối đa m gam Br2 trong CCl4. Biết thể tích các khí đo ở điều kiện tiêu chuẩn. Giá trị của m bằng
A. 24. B. 20. C. 16. D. 36.
Câu 77: Hòa tan hoàn toàn 19,2 gam hỗn hợp X gồm Fe, FeO, Fe2O3, Fe3O4 vào 80 gam dung dịch H2SO4 98% dư, đun nóng, thu được dung dịch Y và V lít khí SO2 (sản phẩm khử duy nhất, ở điều kiện tiêu chuẩn). Thêm từ từ đến hết 350 ml dung dịch NaOH 2M vào dung dịch Y, kết thúc phản ứng thu được 21,4 gam kết tủa và dung dịch Z. Các phản ứng xảy ra hoàn toàn, giá trị của V là
A. 7,84. B. 8,96. C. 5,60. D. 6,72.
Câu 78: Có m gam phèn chua KAl(SO4)2.12H2O tách ra từ 400 gam dung dịch KAl(SO4)2 bão hòa ở 20°C, nếu như có 200 gam H2O bay hơi ở cũng ở nhiệt độ đó. Biết ở 20°C, dung dịch KAl(SO4)2 bào hòa có 5,5% KAl(SO4)2 về khối lượng. Giá trị m gần nhất với giá trị
A. 18,5. B. 22,5. C. 20,5. D. 24,5.
Câu 79: Hỗn hợp X gồm Gly-Lys (a mol) và 0,03 mol amino axit Y mạch hở. Cho X tác dụng với dung dịch gồm 0,05 mol NaOH và 0,02 mol KOH đun nóng, thu được dung dịch Z. Dung dịch Z phản ứng vừa đủ với 80 ml dung dịch HCl 1M và H2SO4 0,5 M thu được dung dịch Y chứa 15,29 gam chất tan đều là muối. Các phản ứng xảy ra hoàn toàn, giá trị của a bằng:
A. 0,03. B. 0,02. C. 0,01. D. 0,015.
Câu 80: Hỗn hợp M gồm 3 este X, Y, Z đều no, mạch hở, trong đó Y và Z là este hai chức và đồng phân cấu tạo của nhau. Cho 44,4 gam M tác dụng vừa đủ với 750 ml dung dịch NaOH 1M đun nóng, thu được hỗn hợp hai muối và 0,55 mol hỗn hợp gồm ancol đơn chức và hai chức. Đốt cháy hỗn hợp muối trên thu được Na2CO3, H2O và 0,375 mol CO2. Mặt khác, nếu đốt cháy 44,4 gam M, thu được 1,5 mol CO2. Các phản ứng xảy ra hoàn toàn, % khối lượng của X có trong M gần nhất với
A. 50%. B. 20%. C. 40%. D. 30%.
O2 Education gửi các thầy cô link download đề thi
Các thầy cô có thể tham khảo thêm nhiều đề thi hơn tại
Tổng hợp đề thi thử TN THPT môn hóa năm 2022 có đáp án
Tổng hợp đề thi TN THPT 2021 môn hóa file word có lời giải
Hoặc xem thêm các tài liệu khác của môn hóa